
6.(08山东临沂质量检测一)(10 分)
将不同量的H2O(气) 和CO
气体分别通入到一体积为l L的恒容密闭容器中进行反应:H2O (g) +
CO( g) 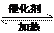 CO2
(g) +H2(g);得到以下三组数据,据此回答下列问题:
CO2
(g) +H2(g);得到以下三组数据,据此回答下列问题:
实验组
温度
起始量
平衡量
达到平衡所需时间
H2O
CO
H2
CO
1
1 mol
2 mol
③加入催化剂 (2分) 移去0.2molNH3(或使0.2molNH3液化 (2分)
(3)①c+(d/2)或(
② A (1分) 因为保持容器不变时比保持容器的容积可变(恒压)体系的压强小,当压强减小时有利于逆向反应,故反应达到平衡后生成氨气的物质的量减小,因此c>d。(2分)
(2)①320/3 (1分) 不变 (1分) ②0.0075mol/(L?min) (1分)
答案(1)<(1分) 由于该反映是可逆反应,1molN2和3molH2不能完全反应生成2molNH3,因此反应放出的热量少于92.4kJ。(2分)
|