
5、式子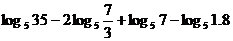 的値是( )
的値是( )
A.1 B.2 C.3 D. 4
4、 函数
函数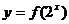 的定义域为[1,2],则函数
的定义域为[1,2],则函数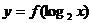 的定义域为( )
的定义域为( )
A.[0,1] B.[1,2] C.[2,4] D.[4,16]
3、“龟兔赛跑”讲述了这样的故书:领先的兔子看着慢慢爬行的乌龟,骄傲起来. 睡了一觉,当它醒来时.发现乌龟快到终点了,于是急忙追赶,但为时已晚,乌龟还是先到达了终点…….用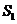 、
、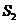 分别表示乌龟和兔子所行的路程(
分别表示乌龟和兔子所行的路程(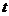 为时问),则下图与故事情节相吻合的是( )
为时问),则下图与故事情节相吻合的是( )
2、集合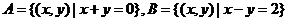 ,则A∩B是( )
,则A∩B是( )
A.(1,-1) B.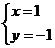 C.
C.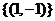 D.{1,-1}
D.{1,-1}
1、设全集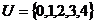 ,
,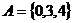 ,
,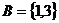 ,则
,则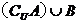 =( )
=( )
A.{2} B.{1,2,3} C.{1,3} D.{0,1,2,3,4}
(二)注意不同范围产物的变化
1、n(Fe)/n(HNO3)≤1/4,产物仅有Fe(NO3)3,HNO3可能有剩余。
2、n(Fe)/n(HNO3)≥3/8,产物仅有Fe(NO3)2,Fe可能有剩余。
3、1/4<n(Fe)/n(HNO3)<3/8,产物为Fe(NO3)3和Fe(NO3)2。
[思考感悟]铁化学性质活泼,为什么可以用铁罐贮存和运输浓H2SO4和浓HNO3?
常温下,铁遇浓H2SO4、浓HNO3发生钝化,在铁表面形成一层致密的氧化膜,阻止内部的金属继续与酸反应,因而常温下可用铁罐来贮存或运输浓H2SO4、浓HNO3,但在加热的条件下,铁能与浓H2SO4、浓HNO3剧烈反应。
[基础训练]
1、下列关于铁的叙述正确的是( B )
①铁能被磁铁吸引,但纯铁易被腐蚀;②在人体内的血红蛋白中含有铁元素;③铁位于元素周期表中第4周期第ⅧB族;④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧;⑤铁与强氧化剂硝酸反应的产物仅是Fe(NO3)3;⑥不能通过化合反应制得FeCl2和Fe(OH)3。
A、①③ B、②④ C、②⑤ D、④⑥
2、能正确表示下列反应的离子方程式的是( C )
A、铁跟盐酸反应:2Fe+6H+=2Fe3++3H2↑
B、铜片跟稀硝酸反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O
C、NaAlO2溶液中通入足量的二氧化碳:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
D、溴化亚铁溶液中加入少量的氯水:4Br-+3Cl2+2Fe2+=2Br2+2Fe3++6Cl-
3、向含有a gHNO3的稀溶液中,加入b g铁粉充分反应全部溶解。已知有a/4 gHNO3被还原,则a︰b不可能是( A )
A、2︰1 B、3︰1 C、4︰1 D、9︰2
[高考模拟]
4、(2007宁夏高考)a g铁粉与含有H2SO4的CuSO4溶液完全反应后,得到a g铜,则参与反应的CuSO4与H2SO4的物质的量之比为( B )
A、1︰7 B、7︰1 C、7︰8 D、8︰7
5、(2007江苏高考)(多选)某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a,将其全部投入50mL b mol·L-1的硝酸溶液中,加热使其充分反应(假设NO是惟一的还原产物)。下列说法正确的是( AD )
A、若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解
B、若金属全部溶解,则溶液中一定含有Fe3+
C、若金属全部溶解,且产生336mL气体(标准状况),则b=0.3
D、当溶液中金属离子只有Fe3+、Cu2+时,则a和b的关系为:b≥80y(1-a/3)
(一)审清两种物质的量
1、明确哪种物质过量;
2、根据两种物质的量分析讨论判断,根据反应方程式:
HNO3过量时:Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O ①
Fe过量时:Fe+2Fe(NO3)3=3Fe(NO3)2 ②
①×2+②得总方程式:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,
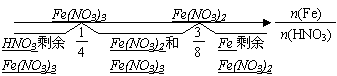 可以用数轴表示:
可以用数轴表示:
(五)钢铁的用途
用于制造各种钢铁制品等。
(四)铁的冶炼
1、设备:炼铁高炉。
2、

 原料:铁矿石、焦炭、空气、石灰石。
原料:铁矿石、焦炭、空气、石灰石。
3、反应原理:C+O2 CO2;CO2+C 2CO;Fe2O3+3CO 2Fe+3CO2。
4、
 产品:生铁(含杂质较多),进一步炼制得钢。
产品:生铁(含杂质较多),进一步炼制得钢。
5、炉渣的形成:CaCO3 CaO+CO2↑;CaO+SiO2 CaSiO3。
(三)化学性质
1、
 与非金属反应
与非金属反应

 Fe与O2、Cl2、I2、S反应的化学方程式分别为:3Fe+2O2 Fe3O4;2Fe+3Cl2 2FeCl3;Fe+I2 FeI2;Fe+S FeS。
Fe与O2、Cl2、I2、S反应的化学方程式分别为:3Fe+2O2 Fe3O4;2Fe+3Cl2 2FeCl3;Fe+I2 FeI2;Fe+S FeS。
2、 与水蒸气反应
与水蒸气反应
反应的化学方程式为:3Fe+4H2O Fe3O4+4H2。
3、与酸反应
(1)与非氧化性酸:如与稀H2SO4、盐酸等反应,其离子方程式为:Fe+2H+=Fe2++H2↑。
(2)与氧化性酸:如与稀HNO3反应,一般不产生H2,常温下,可被浓HNO3、浓H2SO4钝化。
A、稀HNO3过量时生成Fe3+,其离子方程式:Fe+4H++NO3-=Fe3++NO↑+2H2O。
B、铁过量时生成Fe2+,其离子方程式:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O。
4、与盐溶液反应
(1)能与活动性较弱的金属盐溶液反应,如Fe和CuSO4溶液反应的离子方程式为:Fe+Cu2+=Fe2++Cu。
(2)与FeCl3溶液反应,其离子方程式为:2Fe3++Fe=3Fe2+。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com