
3、(2006北京,12.) R、W、X、Y、Z为原子序数依次递增的同一短周期元素,下列说法一定正确的是(m、n均为正整数)( )
A.
若 为强碱,则
为强碱,则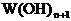 也为强碱
也为强碱
B.
若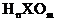 为强酸,则Y是活泼非金属元素
为强酸,则Y是活泼非金属元素
C.
若Y的最低化合价为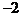 ,则Z的最高正化合价为
,则Z的最高正化合价为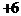
D. 若X的最高正化合价为+5,则五种元素都是非金属元素
2、(2005,四川,9)下列说法中正确的是
A 最外层有2个电子的原子都是金属原子
B 非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数
C 非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
D 最外层有5个电子的原子都是非金属原子
1、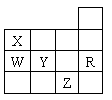 (2005,北京,8).右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
(2005,北京,8).右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
A 常压下五种元素的单质中Z单质的沸点最高
B Y、Z的阴离子电子层结构都与R原子的相同
C W的氢化物沸点比X的氢化物的沸点高
D Y元素的非金属性比W元素的非金属性强
8、(2008,北京,12)工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)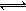 Si(s)+4HCl(g);△H=+QkJ/mol(Q>0)
Si(s)+4HCl(g);△H=+QkJ/mol(Q>0)
某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达平衡时,吸收热量为QkJ
C.反应至4min时,若HCl浓度为0.12mol/L,则H2的反应速率为0.03mol/(L min)
min)
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/L的NaOH溶液恰好反应
解题思路总结:
选择题型六--元素周期律的应用
解题指导:
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7、(2008,四川,7)下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热
ΔH=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的
ΔH=2×283.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热
6、(2008,重庆,13)化学反应N2+3H2 = 2NH3的能量变化如题13图所示,该反应的热化学方程式是
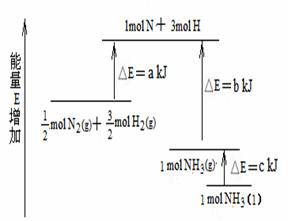 A、N2(g)+3H2(g) = 2NH3(l);
A、N2(g)+3H2(g) = 2NH3(l);
⊿H = 2(a-b-c)kJ/mol
B、N2(g)+3H2(g) = 2NH3(g) ;
⊿H = 2(b-a)kJ/mol
C、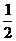 N2(g)+
N2(g)+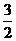 H2(g) = NH3(l) ;
H2(g) = NH3(l) ;
⊿H = (b+c-a)kJ/mol
D、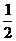 N2(g)+
N2(g)+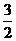 H2(g) =NH3(g) ;
H2(g) =NH3(g) ;
⊿H = (a+b)kJ/mol
5、(2008,宁夏,13)已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为
A.-44.2 kJ·mol-1 B.+44.2 kJ·mol-1
C.-330 kJ·mol-1 D.+330 kJ·mol-1
4、(2007,黑龙江9)已知:①1 mol H2分子中化学键断裂时需要吸收436kJ的能量
②1 mol Cl2分子中化学键断裂时需要吸收243kJ的能量
③由H原子和Cl原子形成1 mol HCl分子时释放431kJ的能量
下列叙述正确的是
A.氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)=2HCl(g)
B.氢气和氯气反应生成2 mol氯化氢气体,反应的△H=183kJ/mol
C.氢气和氯气反应生成2 mol氯化氢气体,反应的△H=-183kJ/mol
D.氢气和氯气反应生成1 mol氯化氢气体,反应的△H=-183kJ/mol
3、(2006,重庆,10)25℃、101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol,则下列热化学方程式正确的是
A C(s)+1/2O2(g)=CO(g);△H=-393.5kJ/mol
B 2H2(g)+O2(g)=2H2O(g);△H=+571.6kJ/mol
C CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-890.3kJ/mol
D 1/2C6H12O6(g)+3O2(g)=3CO2(g)+3H2O(l);△H=-1400kJ/mol
2、(2006,天津,13)已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol
下列结论正确的是
A 碳的燃烧热大于110.5kJ/mol
B ①的反应热为221kJ/mol
C 稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D 稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com