
3.益阳市某年6月上旬日最高气温如下表所示:
|
日
期 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
最高气温(℃) |
30 |
28 |
30 |
32 |
34 |
32 |
26 |
30 |
33 |
35 |
那么这10天的日最高气温的平均数和众数分别是
A.32,30 B.31,30 C.32,32 D.30,30
2.下列计算正确的是
A.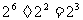 B.
B.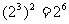 C.
C.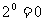 D.
D.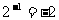
1.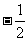 的绝对值是
的绝对值是
A. 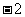 B. 2 C.
B. 2 C.  D.
D. 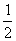
21.(09全国卷Ⅱ 29) (15分)
29) (15分)
 现有A、B、C、D、E、F六种化合物,已知它们的阳离子有
现有A、B、C、D、E、F六种化合物,已知它们的阳离子有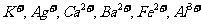 ,
, 阴离子有
阴离子有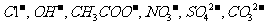 ,现将它们分别配成
,现将它们分别配成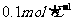 的溶液,进行如下实验:
的溶液,进行如下实验:
①

 测得溶液A、C、E呈碱性,且碱性为A>E>C;
测得溶液A、C、E呈碱性,且碱性为A>E>C;
②

 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③

 向D溶液中滴加
向D溶液中滴加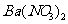 溶液,无明显现象;
溶液,无明显现象;
④

 向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。

 根据上述实验现象,回答下列问题:
根据上述实验现象,回答下列问题:
(1) 
 实验②中反应的化学方程式是
实验②中反应的化学方程式是

 ;
;

 (2)E溶液是 ,判断依据是
(2)E溶液是 ,判断依据是

 ;
;

 (3)写出下列四种化合物的化学式:A 、C
、
(3)写出下列四种化合物的化学式:A 、C
、

 D
、F
.
D
、F
.
 答案:(1)
答案:(1)
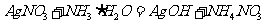

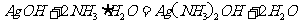
(2) 碳酸钾 由①中碱性减弱的顺序可知,E是碳酸盐。六种阳离子中可以与碳酸根形成可溶性盐的只有钾离子,所以E是碳酸钾
碳酸钾 由①中碱性减弱的顺序可知,E是碳酸盐。六种阳离子中可以与碳酸根形成可溶性盐的只有钾离子,所以E是碳酸钾
(3)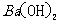
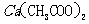
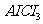
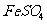
 解析:
解析: 本题考查离子共存、盐类水解综合运用。根据溶液的性质,确定CO32-只能与K+形成显碱性的溶液,另外可能形成的碱性溶液为碱Ba(OH)2
。
本题考查离子共存、盐类水解综合运用。根据溶液的性质,确定CO32-只能与K+形成显碱性的溶液,另外可能形成的碱性溶液为碱Ba(OH)2
。
由于醋酸的酸性大于碳酸,所以醋酸盐水解的碱性小于碳酸盐,因此A为Ba(OH)2,E为K2CO3,C为醋酸盐,由②可得B中阳离子为Ag+,则肯定为AgNO3,由③可得D中无SO42-,则F中的阴离子为SO42-,D中的阴离子为Cl-。
由④可得F中的阳离子为Fe2+,即F为FeSO4,而CH3COO-若与Al3+形成溶液时,Al3+也发生水解,所以C为醋酸钙,而D为AlCl3。
20. (09天津卷 7)(14分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
7)(14分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
 (2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
 (3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
 (4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
 a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
 (5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

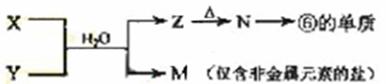
 X溶液与Y溶液反应的离子方程式为_____________________,
X溶液与Y溶液反应的离子方程式为_____________________,
 N→⑥的单质的化学方程式为________________。
N→⑥的单质的化学方程式为________________。
 常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至_________________。
常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至_________________。
 答案:
答案: 

 解析:
解析: 本题以周期表为题材,考查原子半径比较,酸性强弱,电子式,离子方程式以及盐类水解等知识。
本题以周期表为题材,考查原子半径比较,酸性强弱,电子式,离子方程式以及盐类水解等知识。
(1)⑤⑥位于同一周期,且⑤排在⑥的前面,原子半径大,而④在上一周期,比⑤、⑥少一个电子层,故半径最小。
(2)②⑦位于同一主族,上面的非金属性强,最高价含氧酸酸性强,②③位于同一周期,且③在后,非金属性强,对应的酸性强。
(3)四种元素分别为氢、氧、钠和氯,离子键显然必须是钠盐,极性共价键则应有两种非金属组成。
(4)液态H2O2可以在MnO2、FeCl3等催化剂作用下发生分解反应。
(5)⑥为Al,可推断Z为Al(OH)3,受热分解可产物Al2O3,再电解即可得单质铝。M仅含非金属的盐,显然铵盐,所以X与Y应为AlCl3与NH3·H2O的反应,生成NH4Cl。由于NH4+ 水解,故要使其浓度与Cl-相等,则要补充NH3·H2O。由电荷守恒知:C(NH4+ )+ C(H+) C(Cl-)+C(OH-),若C(NH4+ )
C(Cl-)+C(OH-),若C(NH4+ )  C(Cl-),则C(H+)= C(OH-),即pH=7。
C(Cl-),则C(H+)= C(OH-),即pH=7。
19.(09宁夏卷 11)将氢氧化钠稀溶液滴加到醋酸稀溶液中,下列各图示意混合溶液有关量或性质的变化趋势,其中错误的是
11)将氢氧化钠稀溶液滴加到醋酸稀溶液中,下列各图示意混合溶液有关量或性质的变化趋势,其中错误的是

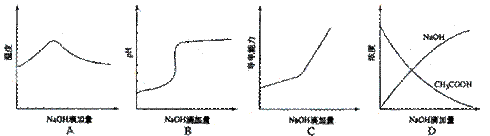
 答案:D
答案:D

 解析:
解析: mA选项氢氧化钠和醋酸发生中和反应,反应放热,当酸反应完成后,再加碱,相当于往热水中加入冷水,温度降低。
mA选项氢氧化钠和醋酸发生中和反应,反应放热,当酸反应完成后,再加碱,相当于往热水中加入冷水,温度降低。
B选项醋酸中滴加氢氧化钠酸性减弱pH增大。
C选项醋酸中滴加氢氧化钠,相当于弱电解质溶液变成强电解质溶液,因此导电能力增加。
D选项醋酸中滴加氢氧化钠,氢氧化钠和醋酸发生反应了,因此氢氧化钠开始时为0.
18.(09海南卷 6)已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
6)已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
 A.该溶液的pH=4
A.该溶液的pH=4
 B.升高温度,溶液的pH增大
B.升高温度,溶液的pH增大
 C.此酸的电离平衡常数约为1×10-7
C.此酸的电离平衡常数约为1×10-7
 D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
答案:B
解析:c(H+)=c(HA)α=0.1×0.1%=10-4,因此pH=4,A正确;弱电解质电离是吸热的,因此升温HA电离程度增大,酸性增强,溶液的pH减小,B错;K=c(A-)·c(H+)/ c(HA)= 10-4×10-4/(0.1- 10-4)= 1×10-7 ,C正确;由HA电离出的c(H+)=10-4 mol/L,水电离出的c(H+)=10-10 mol/L ,因此D正确。
点评:本题综合程度较大,主要考查学生pH计算,电离平衡,影响弱电解质平衡的因素等相关知识。
17. (09重庆卷10)物质的量浓度相同的下列溶液,pH由大到小排列正确的是
A.Ba(OH)2、 Na2SO3、FeCl3、KCl
B.Na2SiO3、Na2SO3、KNO3、NH4Cl
C.NH3·H2O、H3PO4、Na2SO4、H2SO4
D.NaHCO3、C6H5COOH、C2H5OH、HCl
答案:B
解析:A项FeCl3是强酸弱碱盐溶液呈酸性,KCl是强碱强酸盐溶液呈中性,A错误;C项H3PO4显酸性,C错误;D项C2H5OH呈中性,C6H5COOH呈酸性,D错误;答案选B。
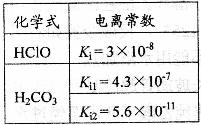
16.(09上海卷 17)根据右表提供的数据,判断在等浓度的
17)根据右表提供的数据,判断在等浓度的
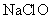 、
、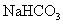 混合溶液中,各种离子浓度关系正确的是
混合溶液中,各种离子浓度关系正确的是
 A.
A.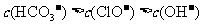
 B.
B.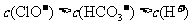
 C.
C.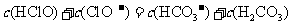
 D.
D.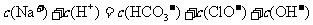
答案:A
[解析]由表中数据可知,H2CO3的酸性大于HClO,HClO的酸性大于HCO3-的酸性,则ClO-的水解程度大于HCO3-,故A项正确, B项错误。根据物料守恒和电荷守恒判断,C项和D项等式右边都漏掉了CO32-的浓度,故均错误。
15. (09四川卷12)关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是
H+4):③>①
B.水电离出的c(H+):②>①
C.①和②等体积混合后的溶液:c(H+)=c(OH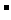 )+c(NH3·H2O)
)+c(NH3·H2O)
D.①和③等体积混合后的溶液:c(NH+4)>c(Cl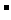 )>c(OH
)>c(OH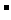 )>c(H+)
)>c(H+)
答案:B
 [解析]A项,氯化铵为强电解质完全电离后产生大量的NH4+;氨水为弱电解质只有少量的NH4+产生。B项在水中加入酸和碱都抑制水的电离,但是盐类水解促进水的电离,B项不正确。盐酸和氨水混合后恰好完全反应,但因生成的盐为强酸弱碱盐,溶液显酸性,而多余的H+为水解产生,C项正确。D项。①和③等体积混合,溶液呈碱性,即氨水的电离大于氯化铵的水解,这样不难得到D正确。
[解析]A项,氯化铵为强电解质完全电离后产生大量的NH4+;氨水为弱电解质只有少量的NH4+产生。B项在水中加入酸和碱都抑制水的电离,但是盐类水解促进水的电离,B项不正确。盐酸和氨水混合后恰好完全反应,但因生成的盐为强酸弱碱盐,溶液显酸性,而多余的H+为水解产生,C项正确。D项。①和③等体积混合,溶液呈碱性,即氨水的电离大于氯化铵的水解,这样不难得到D正确。
 [点评]
[点评] 本题综合考查弱电解质的电离、盐类的水解以及离子浓度大小比较等相关知识,对于考生的要求较高。
本题综合考查弱电解质的电离、盐类的水解以及离子浓度大小比较等相关知识,对于考生的要求较高。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com