
| A、KHSO4、Na2CO3、(NH4)2SO4、FeCl3 |
| B、K2CO3、MgCl2、Al2(SO4)3、KOH |
| C、NaCl、KCl、CuCl2、AgNO3 |
| D、NaOH、(NH4)2SO4、Na2SO4、BaCl2 |


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
+ 4 |
2- 3 |
2- 4 |
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | K+ Al3+ Fe2+ Ba2+ |
| 阴离子 | OH- Cl- SO42- HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
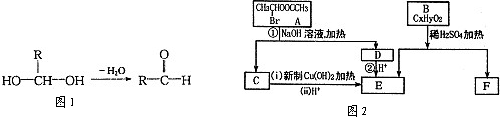
查看答案和解析>>
科目:高中化学 来源: 题型:
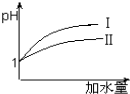
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | K+ Na+ Fe2+ Ba2+ NH4+ |
| 阴离子 | OH- NO3- I- HCO3- AlO2- HSO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若a+b<c+d,则反应一定能自发向右进行 |
| B、若从正反应开始,起始时A、B的物质的量之比为a:b,则平衡时A、B的转化率之比也为a:b |
| C、若a+b=c+d,在平衡体系中共有气体m mol,再向其中充入n mol B,则达到平衡时气体总物质的量小于(m+n)mol |
| D、若a+b=c+d,则对于体积不变的容器,升高温度,平衡向左移动,容器中气体的压强一定不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com