
题目列表(包括答案和解析)
7.共价键、离子键和分子间作用力是构成物质的微粒间的不同作用方式,下列物质中,只含有上述一种作用的是( )
A.干冰 B.氯化钠 C.氢氧化钠 D.碘
6.分子间作用力为a,化学键为b,则a、b的大小关系是( )
A. a>b B.a<b C.a=b D.无法确定
5.下列物质在变化过程中,只需克服分子间作用力的是( )
A.食盐溶解 B.干冰升华
C.氯化铵受热,固体消失 D.石墨熔化
4.下列说法中不正确的是( )
A.金属和非金属原子之间一定形成离子键
B.两个非金属原子之间形成的化学键一定是共价键
C.含有离子键的物质不可能是单质
D.单质中不一定含有共价键
3.下列过程中,共价键被破坏的是( )
A.碘升华 B.溴蒸气被木炭吸附
C.NaCl溶于水 D.HCl气体溶于水
2.下列物质中,只含有共价键的化合物是( )
A.碘化氢 B.烧碱 C.液溴 D.食盐
1.下列电子式书写正确的是( )
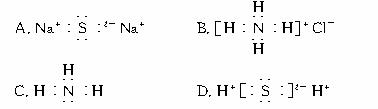
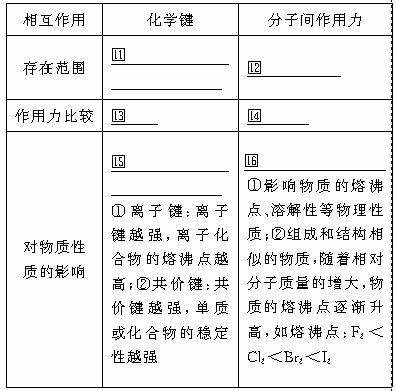
3.化学键、分子间作用力
巩固练习
2.用电子式、结构式表示下列共价分子
HCl:电子式:[3] ,结构式:[4] ;
H2O:电子式:[5] ,
结构式:[6] ;
NH3:电子式:[7] ,
结构式:[8] ;
CH4:电子式:[9] ,
结构式:[10] 。
13.已知氮化钠(Na3N)在熔融时能导电,与水作用能产生氨气。试回答下列问题:
(1)氮化钠属于 化合物。
(2)比较Na3N中离子的半径: > 。
(3)Na3N与水反应的方程式为 ,该反应属于 反应。(填四种基本反应类型)
资料卡片
决定离子键强弱的主要因素
使带相反电荷的阴、阳离子结合的相互作用,叫做离子键。可见,离子键的强弱取决于静电作用的大小,而静电作用的大小与阴、阳离子所带的电荷多少及阴、阳离子半径的大小有关。根据公式F=k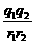 可知,阴、阳离子所带的电荷越多,半径越小,相互作用就越强。离子键的强弱决定着该离子化合物的熔沸点高低。
可知,阴、阳离子所带的电荷越多,半径越小,相互作用就越强。离子键的强弱决定着该离子化合物的熔沸点高低。
轻松一题: 下列离子化合物的熔点最高的是( C )
A.NaCl B.KCl C.MgO D.Na2O
自我反馈
导学园地

第二课时 共价键、分子间作用力
导学园地

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com