
题目列表(包括答案和解析)
2.下列有关有机物的叙述正确的是
A.均难溶于水易溶于有机溶剂 B.都属于非电解质,水溶液不导电
C.熔点低、受热易分解且能燃烧 D.多数反应速率慢、复杂且副产物多
1.通常用来衡量一个国家石油化工发展水平标志的是
A.甲烷的产量 B.乙烯的产量
C.乙醇的产量 D.苯的产量
16、(26分)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0 mL、大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
|
实验编号 |
T/K |
大理石规格 |
HNO3浓度/mol·L-1 |
实验目的 |
|
① |
298 |
粗颗粒 |
2.00 |
(Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 探究温度对该反应速率的影响; (Ⅲ)实验①和 探究大理石规格(粗、细)对该反应速率的影响。 |
|
② |
|
|
|
|
|
③ |
|
|
|
|
|
④ |
|
|
|
(2)实验①中CO2质量随时间变化的关系见下图:
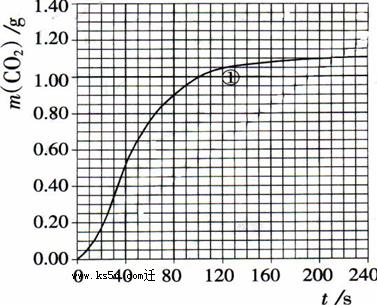
请在图中画出实验②和④中CO2质量随时间变化关系的预期结果示意图。
15、(10分)单斜硫和正交硫转化为二氧化硫的能量变化图如右,回答下列问题:
(1)正交硫的稳定性比单斜硫 (填“好”或“差”), 相同物质的量的正交硫比单斜硫所含有的能量 (填“高”或“低”),
①式表示断裂lmol单斜硫和 lmol O2中的共价键所吸收的能量比形成1mol SO2中的共价键所放出的能量 (填“多”或“少”297.16kJ。
(2)写出单斜硫转化为正交硫的热化学方程式:
14、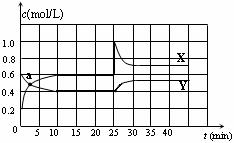 已知NO2和N2O4可以相互转化:N2O4(g)
已知NO2和N2O4可以相互转化:N2O4(g) 2NO2(g)
△H <0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图。下列说法不正确的是
2NO2(g)
△H <0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图。下列说法不正确的是
A.图中的两条曲线,X是表示NO2浓度随时间的变化曲线
B.a点时v(N2O4) = v(NO2)
C.25 min时改变了影响速率的一个因素,使得NO2转变为N2O4,该改变是将密闭容器的体积缩小,增大压强
D.前10 min内用v(N2O4)表示的化学反应速率为0.02 mol/(L·min)
12、
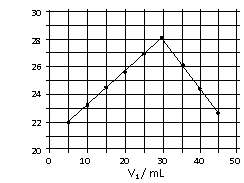 将V1mL1.0mol/L HCl溶液和V2mL未知
将V1mL1.0mol/L HCl溶液和V2mL未知
浓度的NaOH溶液混合均匀后测量并记录溶
液温度,实验结果如右图所示(实验中始终
保持V1+V2=50mL)。下列叙述正确的是
A.做该实验时环境温度为22℃
B.该实验表明化学能可能转化为热能
C.NaOH溶液的浓度约为1.5mol/L
D.该实验表明有水生成的反应都是放热反应
13下图所示的直型石英玻璃封管中充有CO气体,左端放置不纯的镍(Ni)粉。在一定条件下,Ni可以与CO(g)发生如下反应:

但Ni粉中的杂质不与CO(g)发生反应。玻璃管内左右两端的温度分别稳定在350K和470K,经过足够长时间后,下列说法正确的是
A.在石英管右端主要物质是Ni(CO)4(g)
B.在石英管右端主要物质是纯Ni(s)和CO(g)
C.在石英管左端主要物质是纯Ni(s)和CO(g)
D.整个过程可以看作CO(g)将Ni(s)从石英管左端转移到右端,从而达到提纯目的
11.右图是373K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是
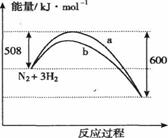 A.该反应的热化学方程式为:
A.该反应的热化学方程式为:
N2+3H2 2NH3
△H=-92kJ·mol-1
2NH3
△H=-92kJ·mol-1
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热不变
D.在相同温度的条件下,在体积相同I、II两个容器中分别通入1mol N2和3 mol H2,容器I体积恒定,容器II体积可变保持恒压,则反应过程中两容器内的反应速率V(I)<V(II)
10.100 mL 6 mol·L-1 H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量
A.碳酸钠溶液 B.水 C.硫酸钾溶液 D.硝酸钠溶液
9.在4L的密闭容器中充入6mol A气体和5mol B气体,在一定条件下发生如下反应:3A(g) + B(g)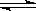 2C(g) + xD(g)。若经10s后测得生成2 molC,D的浓度为0.5 mol·L-1,下列几种说法正确的是
2C(g) + xD(g)。若经10s后测得生成2 molC,D的浓度为0.5 mol·L-1,下列几种说法正确的是
A.x =1 B.B的转化率为20%
C.反应的10s内A的反应速率为0.3 mol·L-1 ·s-1
D.反应进行到10s时,在相同温度下容器内混合气体的压强是反应前的85%
8.化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P:198 P-O:360 O=O:498则反应P4(白磷)+3O2= P4O6的反应热ΔH为
A.-1638 kJ·mol-1 B.+1638 kJ·mol-1
C.-126 kJ·mol-1 D.+126 kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com