
题目列表(包括答案和解析)
31.把由NaOH、AlCl3和MgCl2三种固体组成的混合物溶于足量水中,有1.16g白色沉淀析出,向所得溶液里逐滴加入1 mol/L的盐酸,加入盐酸的体积和沉淀的质量如图所示:
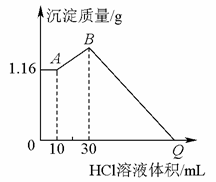
(1)A点的沉淀物的化学式为____________________;
B点的沉淀物的化学式为____________________。
(2)原混合物中MgCl2的质量是__________g,AlCl3的质量是__________g,NaOH的质量是__________g。
(3)Q点HCl溶液的体积为__________mL。
30.用中和滴定测定某烧碱的纯度,试根据实验回答下列有关问题:
(1)配制待测溶液:将准确称量的4.10g含有少量中性易溶杂质的固体烧碱,配成250ml待测溶液,主要用到的仪器是 。(至少填2个)
(2)滴定时,用0.2mol/L的盐酸来滴定待测溶液,带有玻璃活塞的滴定管盛放 ;进行滴定时, 手旋转滴定管的玻璃活塞, 手不停轻摇锥形瓶,眼睛看着 。
(3)根据下表的数据,计算被测烧碱溶液的物质的量浓度是 ,烧碱的纯度是 ;
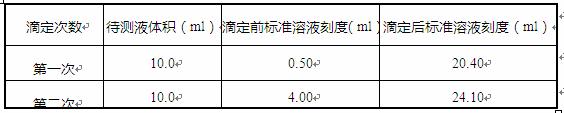
(4)若将锥形瓶用待测液润洗,然后再盛放待测液10ml,滴定(其它操作无误)结果 ;(填“偏高”或“偏低”或“正常”,下同)
(5)观察酸式滴定管内液面时,开始平视,滴定终点俯视,则结果 。
29.相同浓度的NH4HSO4和(NH4)2SO4 溶液,都呈 性,前者显此性的主要原因是 ,后者显此性的原因是 。(用离子反应方程式表示。)
28.要除去下列物质中所含杂质(括号内为杂质),请将选用的试剂及分离方法填在题后的横线上,并写出有关反应的化学方程式(是离子反应的写出离子方程式)。
(1)Al2O3[Al(OH)3]________________________________________。
(2) Fe(Al)____________________ ____________________。
(3)Fe2O3(Al2O3)________________________________________。
27.在固定容器的密闭容器中,有可逆反应nA(g)+mB(g)pC(g)处于平衡状态(已知n+m>p,△H>0既吸热反应)。升高温度时c(B)/c(C)的比值 ,混合气体的密度 ;降温时,混合气体的平均式量 ;加入催化剂,气体的总物质的量 ;充入C,则A、B的物质的量 。(填“增大”,“减小”或“不变”。)
26.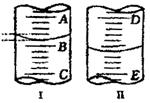 如图:
如图:
(1)图I表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为4,量筒中液体体积是
mL。
(2)图II表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号) 。
A.是a mL B.是(50-a)mL
C.一定大于a mL D.一定大于(50-a)mL
25.向某晶体的水溶液中加入含Fe2+的溶液后,无明显变化,当滴加几滴溴水后,混合液出现红色,那么由此得出的下列结论中,错误的是( )
A.该晶体中一定含有SCN-
B.Fe3+的氧化性比Br2的氧化性强
C.Fe2+被Br2氧化为Fe3+
D.Fe2+与SCN-不能形成红色的化合物
第Ⅱ卷(选择题,共50分)
24.表示0.1mol/LNaHCO3溶液中有关微粒浓度(mol/L)的关系式,正确的是()
a+)>c(HCO3-)>c(CO32-)>(H+)>(OH-)
a+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
a+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
a+)=c(HCO3-)+c(CO32-)
23、下列叙述中,正确的是
A、含金属元素的离子不一定都是阳离子
B、在氧化还原反应中,非金属单质一定是氧化剂
C、某元素从化合态变为游离态时,该元素一定被还原
D、金属阳离子被还原一定得到金属单质
22.在FeCl3、CuCl2混合液中加铁屑,反应后可滤出固体,滤液中阳离子可能是( )
A、只有Fe3+ B、Fe2+和Fe3+ C、Cu2+和Fe3+ D、Fe2+和Cu2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com