
题目列表(包括答案和解析)
4.下列物质溶于水,由于水解而使溶液显酸性的是
A.NH3 B.Na2CO3 C.FeCl3 D.CO2
3.下列仪器中没有“0”刻度线的是
A.托盘天平的游码刻度尺 B.温度计
C.酸式滴定管 D.量筒
2.实验室制备下列气体,可以使用HNO3的是
A.H2 B.O2 C.NO2 D.NH3
1.下列物质不会污染环境的是
A.NO B.N2 C.Cl2 D.SO2
24.(5分) 将16.1g氯化铵固体与足量熟石灰混合加热,使之充分反应,能制得氨气多少升(标准状况)?将此气体通入100mL氯化铝溶液,恰好将溶液中的Al3+完全沉淀,求氯化铝溶液的物质的量浓度。(要有计算过程)
册亨民族中学2010~2011学年度第一学期期末考试
23.下图是铜锌原电池装置。其电池的总反应是:
Zn(s) + CuSO4(aq)== ZnSO4(aq) + Cu(s)。
R是盐桥,其作用是使两个烧杯中的溶液连成通路。

请回答以下问题:
⑴B中是ZnSO4溶液,电极Y的材料是________。
⑵R中的阳离子移向_______(填A或B)中的溶液。
⑶X为原电池的______极,其电极反应式是____________________________。(2分)
22. 某课外活动小组在实验室用下图所示的装置进行实验,验证氨的某些性质并收集少量纯净氮气。试回答:
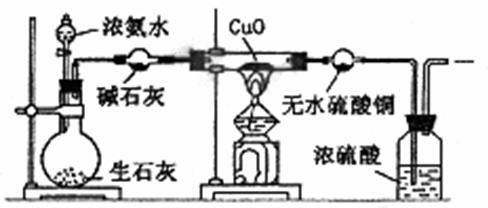
⑴实验前先将仪器按图连接好,然后 ,再开始实验。
⑵实验进行一段时间后,可以观察到硬质试管内黑色的CuO粉末变成 色,
盛无水CuSO4的干燥管内出现 色,并在最后的出气导管处收集到纯净、干燥的N2。根据这些现象,硬质试管中的反应方程式为 (2分),这个反应说明氨气具有 性。
⑶洗气瓶中浓硫酸的主要作用是 。
⑷在最后出气管口收集干燥、纯净的氮气,收集方法是 (填编号)
A.向上排空气法 B.向下排空气法 C.排水法 D.用塑料袋或球胆收集
20.(4分) 合成氨工业对国民经济和社会发展具有重要的意义。向2L密闭容器中通入2mol 气体N2 和6mol气体H2,在一定条件下发生反应:N2(g)+3H2(g)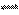 2NH3(g);已知:反应2min达到平衡 ,此时N2的浓度减少了2/3。
回答下列问题:
⑴反应2min内,用NH3表示该反应的速率是________________;
⑵反应平衡时,N2的转化率为
;
⑶如果只升高反应温度,其他反应条件不变,平衡时NH3浓度为 1.1 mol/L,则该反应的ΔH
0;(填“>”、“<”或“=”)
⑷合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是________(填序号)。
2NH3(g);已知:反应2min达到平衡 ,此时N2的浓度减少了2/3。
回答下列问题:
⑴反应2min内,用NH3表示该反应的速率是________________;
⑵反应平衡时,N2的转化率为
;
⑶如果只升高反应温度,其他反应条件不变,平衡时NH3浓度为 1.1 mol/L,则该反应的ΔH
0;(填“>”、“<”或“=”)
⑷合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是________(填序号)。
①20 MPa-50 MPa ②500℃的高温 ③铁触媒作催化剂
④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中 ⑸如果其他条件不变,将容器的容积变为 1L,进行同样的实验,则与上述反应比较: 反应速率 (填“增大”、“减小”或“不变”),理由是 ; 21.(3分) 某金属X,为了确定其成分,进行一系列实验,实验过程和发生的现象如下图所示:
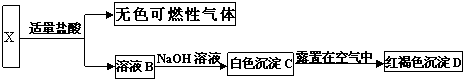

⑴写出金属X的化学式 。
⑵写出溶液B中溶质的化学式 。
⑶写出白色沉淀C转变为红褐色沉淀D的化学方程式 。(2分)
19.实验室配制有0.1mol/L的Na2CO3溶液,根据电离平衡和水解知识,回答下列有关问题:
⑴写出H2CO3的电离方程式为 ;
⑵Na2CO3溶液显碱性,原因是(用离子方程式表示)
;(2分)
⑶在该溶液中,c(Na+)、c(CO32-) 、c(H+)、c(HCO3-)、c(OH-)的大小关系为
;(2分)
⑷根据电荷守恒原理,该溶液中离子浓度关系有:
c(Na+)+c(H+)= ;(2分)
⑸根据物料守恒原理,该溶液中离子浓度关系有:
c(Na+)= 。(2分)
18. ⑴有A、B、C3种烃,各取1mol充分燃烧后,A、B、C所产生的二氧化碳均为44.8L(标准状况);在镍催化剂的作用下B、C都能和氢气发生加成反应,其中B可以转变为A或C,C可以转变为A;B或C都能使高锰酸钾酸性溶液褪色,而A无此性质。
试推断出3种烃的结构简式:
A是 ,B是 ,C是
写出B在一定条件反应生成氯乙烯的化学方程式: 该反应的类型是 。
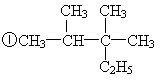
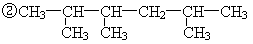
⑵
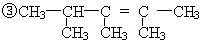
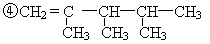
以上四种有机物中互为同系物的是 (填序号,下同),互为同分异构体的是 ,能发生加成和加聚反应的是 ,请用系统命名法命名①的名称
(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com