
题目列表(包括答案和解析)
7.下列过程或现象与盐类水解无关的是
A.铁在潮湿的环境下生锈 B.纯碱溶液去油污
C.加热氯化铁溶液颜色变深 D.草木灰不宜与用作氮肥的铵盐使用
6.将纯水加热至较高温度,下列叙述正确的是:
A. 水的离子积变大、pH变小、呈酸性 B. 水的离子积不变、pH不变、呈中性
C. 水的离子积变小、pH变大、呈碱性 D. 水的离子积变大、pH变小、呈中性
5.在2 L的密闭容器中发生反应:2SO2
+ O2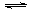 2SO3,如果2 min内SO2的量由12
mol
2SO3,如果2 min内SO2的量由12
mol
下降为4 mol,则下列说法正确的是
A.用SO2的浓度变化表示的反应速率为4 mol/(L·min)
B.用O2的浓度变化表示的反应速率为2 mol/(L·min)
C.增大压强,正反应速率增大,逆反应速率减小
D.升高温度,正反应速率和逆反应速率都增大
4.实验室用足量镁粉与一定量的某浓度的盐酸反应来制得氢气。由于反应速率太快,不易操作。为减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质是
A.CH3COONa固体 B.NaOH溶液 C.(NH4)2SO4粉末 D. K2SO4固体
3.进行化学实验,观测实验现象,通过分析推理得出正确的结论是学习化学的方法之一。对下列实验事实的解释正确的是
A.在KI淀粉溶液中通入Cl2,溶液变蓝,说明氯气能与淀粉发生显色反应
B.浓硝酸在光照条件下变黄,说明浓硝酸不稳定,有有色产物生成且能溶于浓硝酸
C.在某溶液中加入HNO3酸化的BaCl2溶液有白色沉淀产生,说明溶液中含有SO42-
D.将铜片放入浓硫酸中无明显实验现象,说明铜在冷的浓硫酸中发生钝化
2.下列气体的制备可采用右图装置的是
A.铜与浓硝酸反应制NO2
B.铜与稀硝酸反应制NO
C.乙醇与浓硫酸反应制乙烯
D.氯化钠与浓硫酸反应制HCl
1.下列试剂的储存方法正确的是
A.浓硝酸存放在棕色广口试剂瓶中 yjw
B.少量白磷存放在煤油中
C.盛溴的试剂瓶里加少量水以减少溴的挥发
D.将浓盐酸与浓氨水存放在同一层药品橱里
25.(8分)将0.05mol/l的盐酸和未知浓度的氢氧化钠溶液以1:2的体积比混合,所得溶液pH值为12,用上述氢氧化钠溶液滴定pH=3的某一元弱酸溶液20ml,达到终点时,消耗氢氧化钠溶液12.5ml,试求:
(1) 氢氧化钠溶液的物质的量浓度?
(2) 此一元弱酸的物质的量浓度?
www.k@s@5@ 高#考#资#源#网
24. (12分)有pH均为2的盐酸、硫酸、醋酸三瓶溶液:
(1)设三种溶液的物质的量浓度依次为c1、c2、c3,则其关系是 (用“>、<、=”表示,下同)。
(2)取同体积的三种酸溶液分别加入足量的锌粉,反应开始放出H2的速率依次为a1、a2、a3,则其关系是 ;反应过程中放出H2的速率依次为b1、b2、b3,则其关系是
(3)完全中和体积和物质的量浓度均相同的三份NaOH溶液时,需三种酸的体积依次为V1、V2、V3,则其关系是 。
23.(12分)用实验确定某酸HA是弱电解质。两同学的方案是: 甲:①称取一定质量的HA配制0.l mo1·L-1的溶液100mL; ②用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。 乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=l的两种酸溶液各100mL; ②分别取这两种溶液各10mL,加水稀释为100mL; ③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。 (1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=) 乙方案中,说明HA是弱电解质的现象是 (多选扣分) (a)装HCl溶液的试管中放出H2的速率快; (b)装HA溶液的试管中放出H2的速率快; (c)两个试管中产生气体速率一样快。 (3)请你评价:乙方案中难以实现之处和不妥之处 、 (4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com