
题目列表(包括答案和解析)
16. 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:下列叙述不正确的是 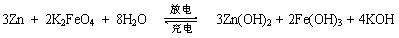
A. 放电时负极反应为:Zn - 2e- + 2OH- == Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3 - 3e- + 5OH- == FeO42- + 4H2O
C. 放电时每转移3moL电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
15. 某温度下向20mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,混合液的pH随NaOH溶液的体积(V)的变化关系如图(忽略温度变化)。下列说法中正确的是( )
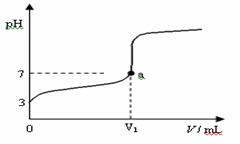
A.该温度下醋酸的电离平衡常数约为1×10-6mol·L-1
B.图中V1 > 20mL,且a点对应的溶液中:c (Na+)+ c (H+) = c (OH-)+ c (CH3COO-)
C.图中V1 < 20mL,且a点对应的溶液中:c (CH3COOH) + c (CH3COO-) > c (Na+)
D.当加入Na OH溶液的体积为20mL时,溶液中:c (CH3COOH) + c (H+) > c (OH-)
14.有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:
①CH3COONa与HCl; ②CH3COONa与NaCl③CH3COONa与NaOH④CH3COONa与Na2CO3下列各项排序正确的是( )
A.pH:②>③>④>①
B 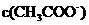 :②>④>③>①
:②>④>③>①
C.溶液中C(H+):①>②>④>③
D 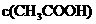 :①>④>③>②
:①>④>③>②
13. 下列实验现象正确、所得结论合理的是( )
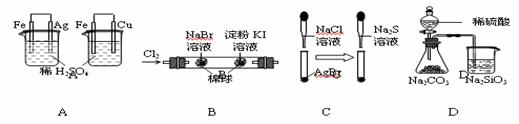
|
实验 |
实验现象 |
结论 |
|
A |
左烧杯中银表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Fe>Cu>Ag |
|
B |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
|
C |
淡黄色固体先变为白色,后变为黑色 |
溶解性:AgCl>AgBr>Ag2S |
|
D |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:S>C>Si |
12.在1LK2SO4和CuSO4的混合溶液中,c(SO42-)=2 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L(标准状况)气体,则原溶液中K+的物质的量浓度为( )
A. 2.0 mol·L-1 B. 1.5 mol·L-1 C. 1.0 mol·L-1 D. 0.5 mol·L-1
11.用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1mol CuO后恰好恢复到电解前的浓度和PH。则电解过程中转移的电子数为( ) A、0.1mol B、0.2mol C、0.3mol D、0.4mol
10.下列图示中关于铜电极的连接错误的是 ( )
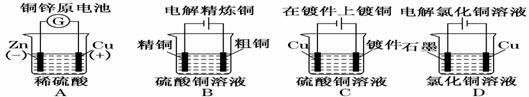
9.100 mL浓度为2 mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是( )
A.加入适量的6 mol/L的盐酸 B.加入数滴氯化铜溶液 C.加入适量蒸馏水 D.加入适量的醋酸钠溶液
8.用惰性电极电解M(NO3)x的水溶液,当阴极上增重ag时,在阳极上同时产生bL氧气(标准状况):从而可知M的原子量为 ( )
A.22.4ax/b B.11.2ax/b C.5.6ax/b D.2.5ax/b
7.用惰性电极电解下列溶液一段时间后,再加入一定量的另一种物质(括号内),溶液能恢复到与原溶液完
全一样的是( )
A.CuCl2 (CuSO4) B.NaOH (NaOH) C.NaCl (HCl) D.CuSO4(Cu(OH)2)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com