
题目列表(包括答案和解析)
1、许多环境问题是跨国界的,甚至是全球性的。根据《蒙特利尔议定书》的有关要求,我国政府采取了一系列措施来保护地球环境,如2002年起我国汽车业就全面禁用氟里 昂(Freon)空调、2005年开始停止生产“哈龙(Halons)1211灭火器”等。这主要是由于氟里昂、哈龙等物质都是
A.有机化合物 B.极易挥发的物质 C.破坏臭氧层的物质 D.是有毒的物质2、下列有机物命名正确的是
A.3,3-二甲基丁烷 B.2,2 -二甲基丁烷
C.2-乙基丁烷 D.2,3,3-三甲基丁烷
22.(10分)如图所示,通电5min后,电极5的质量增加2.16 g,已知1、2、3、4是石墨电极,5和6是Ag电极。


请完成下列填空:
(1)电极5是 极,a是 极。
(2)A池的阴极反应式为: ;
B池的阳极反应式为: 。
(3)此时如果B槽中共收集到224mL气体(标准状况),且溶液体积为200mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为 。
21.(8分)高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g) Fe(s)+CO2(g)
△H>0。
Fe(s)+CO2(g)
△H>0。
(1)此反应的平衡常数表达式为:K= ;
(2)温度升高,达到新的平衡后,高炉内CO2与CO的体积比 将 (填“增大”、“减小”或“不变”);
将 (填“增大”、“减小”或“不变”);
(3)1100℃时,K=0.28。某时刻测得高炉(此时炉温为1100℃)中c(CO2)=0.025mol·L-1,c(CO)=0.1mol·L-1,在这种情况下,该反应 (填“是”或“不是”)处于化学平衡状态。如果“不是”,此时化学反应向 方向进行(填“正反应”或“逆反应”);如果“是”,此空不填。
20.(8分)用标准HCl溶液滴定未知浓度的NaOH溶液,由于实验中某些操作不当,讨论其对所测NaOH溶液浓度的影响。(填“偏高”、“偏低”或“无影响”)
(1)酸式滴定管水洗后,未用标准液润洗就直接注入标准盐酸溶液。
(2)滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没干燥。
(3)酸式滴定管在滴定前尖嘴处有气泡,滴定后气泡消失。
(4)读取盐酸体积时,滴定前平视读数,滴定结束时俯视读数。
19.(10分)常温下,将0.1mol CH3COONa和0.02mol HCl溶于水,形成1L的混合溶液。
(1)该溶液中,存在三个平衡体系。请用电离方程式或离子方程式表示其中任意的两个平衡体系: 、 。
(2)溶液中共有 种不同的粒子。
(3)这些粒子中,浓度为0.1mol/L的是 。(填粒子符号)
(4) 和 两种粒子的物质的量之和等于0.1mol。(填粒子符号)
18.(8分)物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种。请根据所学化学知识回答下列问题:
(1)0.1 mol·L-1的(NH4)2SO4溶液中,各离子的物质的量浓度由大到小的顺序为 。
(2)0.1 mol·L-1的NaHCO3溶液中,c(H2CO3) c(CO32-)。(填“>”、“<”或“=”)
(3)含有足量AgCl固体的饱和溶液中,存在如下平衡:AgCl(s) Ag+(aq)+Cl-(aq)。在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水、②100
mL 0.3 mol·L-1 AgNO3溶液、③100 mL 0.1 mol·L-1MgCl2溶液。充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为__________________
(填序号),此时溶液②中Cl-的物质的量浓度为
。
Ag+(aq)+Cl-(aq)。在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水、②100
mL 0.3 mol·L-1 AgNO3溶液、③100 mL 0.1 mol·L-1MgCl2溶液。充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为__________________
(填序号),此时溶液②中Cl-的物质的量浓度为
。
17.(8分)请回答:
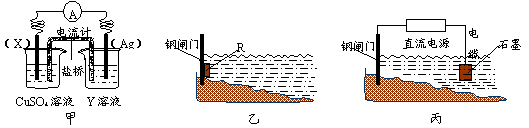
(1)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如下图甲所示。
①电极X是 ;
②外电路中的电子是从 电极流向 电极(填电极材料名称)。
③在电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向CuSO4溶液一端扩散的离子是 (填离子符号)。
(2)①金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生电
化学腐蚀而生锈。请写出铁锅生锈过程的正极反应式:_____________________ 。
②为了减缓某水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案,其中焊接在铁闸门上的固体材料R可以采用____________(填写字母序号)。
A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的 极。

16.在0.1mol/LNH4Cl溶液中,下列关系式中不正确的是 ( )
A.c(Cl-)>c(NH4+)>c(H+)>c(NH3·H2O)>c(OH-)
B.c(Cl-)=c(NH4+)+c(NH3·H2O)
C.c(Cl-)>c(H+)=c(NH3·H2O)>c(NH4+)>c(OH-)
D.c(Cl-)+c(H+)=2c(NH3·H2O)+c(OH-)+c(NH4+)
第Ⅱ卷 非选择题(共52分)
15.在某一电能与化学能的转化装置(电解池或原电池)中,发生的总反应的离子方程式为:Cu+2H+=Cu2++H2↑,则下列关于该装置的有关说法正确的是 ( )
A.该装置可能是原电池,也可能是电解池
B.该装置只能是原电池,且电解质溶液为硝酸
C.该装置只能是电解池,且金属铜为该电解池的阳极
D.该装置只能是原电池,电解质溶液不可能是盐酸
14.室温下,等体积的下列酸和碱的溶液,混合后pH一定小于7的是 ( )
A.pH=3的HNO3和pH=11的KOH溶液
B.pH=3的HNO3和pH=11的NH3·H2O
C.pH=3的H2SO4和pH=11的NaOH溶液
D.pH=3的CH3COOH和pH=11的Ba(OH)2溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com