
题目列表(包括答案和解析)
4.(6分)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种,请回答后面问题:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)上述关系一定不正确的是 (填序号)
(2)若溶液中只有一种溶质,则该溶质为 ,该溶液中离子浓度的大小关系为 (填序号)
(3)若关系③正确,则溶液中溶质为 。
(4)若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显
(填“酸性”、“碱性”、“中性”)。
(5)25℃,pH=a的盐酸Va mL与pH=14-a的氨水Vb mL混合,若溶液显中性,
则Va Vb(填>、<、=、无法确定)
3.(4分)(1)将等质量的Zn粉分别投入:试管A: 10mL 0.1mol·L-1 HCl和试管B: 10mL 0.1mol·L-1醋酸中:开始时,反应速率A B(填>,=或<,下同),若Zn过量,产生H2的体积A B。
(2)将等质量Zn粉分别投入pH=1体积均为10mL的试管A: 盐酸和试管B: 醋酸中:开始时,反应速率A B(填>,=或<,下同),若Zn过量,产生 H2的体积A B。
2.(6分)已知0.1mol·L-1 CH3COONa溶液PH=8
(1)按物质的量浓度由大到小顺序排列该溶液中各种微粒
(水分子除外)
[来源:]
(2)精确表达下列算式的数学结果
C(Na+)-C(CH3COO-)= C(OH-)-C(CH3COOH)=
1.按要求填空。(6分)(说明:(1)(2)(3)均写离子方程式)
(1)AlCl3 水解方程式
(2)Na2CO3水解方程式
(3)泡沫灭火剂的原理是
(4)Ag2SO4电离方程式
(5)Ag2SO4沉淀溶解平衡方程式
其Ksp的表达式
26.被称之为“软电池”的纸质电池,其电池总反应为Zn+2MnO2+H2O ZnO+2MnO(OH)。
ZnO+2MnO(OH)。
下列说法正确的是 ( )
A.该电池的正极为锌
B.该电池反应中二氧化锰起催化剂作用
C.当65 g Zn完全溶解时,流经电极的电子1mol
D.电池正极反应式为2MnO2+2e-+2H2O 2MnO(OH)+2OH-
2MnO(OH)+2OH-
25.科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入以磷酸为电解质的燃料电池发电。电池正极反应为 ( )
A.H2+2OH- =2H2O+2e- B.O2+4H+=2H2O-4e-
C. 2H++2e- =H2 D.O2+2H2O+4e- =4OH-
24.铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为
Pb+PbO2+2H2SO4===2PbSO4+2H2O,下列结论正确的是( )
A.电池放电时,PbO2为正极,被氧化
B.电池放电时,负极反应式为Pb-2 e-=Pb2+
C.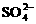 只向PbO2处移动
只向PbO2处移动
D.电解质溶液pH不断增大
23.将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
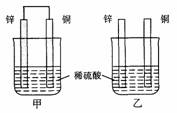 A.两烧杯中铜片表面均无气泡产生
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
22.等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,下列各图中表示其产生氢气总体积(V)与时间(t)的关系正确的是 ( )
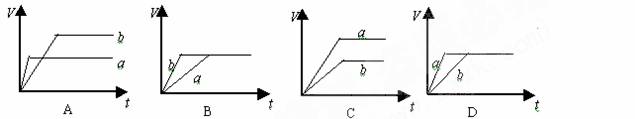
21.有a、b、c、d四种金属,将a与b用导线连接起来,浸入电解质溶液中,b不易腐蚀;将a、d分别投入等浓度盐酸中,d比a反应激烈;将铜浸入b的盐溶液中,无明显变化;若将铜浸入c的盐溶液中,有金属c析出,据此判断它们的活动性由强到弱的顺序是( )
A.d>c>a>b B.d>a>b>c
C.d>b>a>c D.b>a>d>c
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com