
题目列表(包括答案和解析)
6.用0.10 mol·L-1的盐酸滴定0.10 mol·L-1的氨水,滴定过程中不可能出现的结果是( )
A.c(NH4+)>c(Cl-),c(OH-)>c(H+)
B.c(NH4+)=c(Cl-),c(OH-)=c(H+)
C.c(Cl-)> c(NH4+), c(OH-)>c(H+)
D.c(Cl-)> c(NH4+),c(H+)> c(OH-)
5.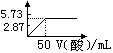 已知H+(aq)+OH-(aq)= H2O(l);ΔH= -57.kJ/mol,向50mL2mol/L的NaOH溶液中加入1mol/L的某种酸,测得加入酸的体积与反应放出的热量关系如右图所示(不考虑热量损失),则该酸可能是 (
)
已知H+(aq)+OH-(aq)= H2O(l);ΔH= -57.kJ/mol,向50mL2mol/L的NaOH溶液中加入1mol/L的某种酸,测得加入酸的体积与反应放出的热量关系如右图所示(不考虑热量损失),则该酸可能是 (
)
A.盐酸 B.醋酸
C.草酸(HOOC-COOH) D.硫酸
4.A、B、C三种物质,每个分子中都含有18个电子且B、C均为两种元素组成的化合物。其中A的分子属于非极性分子,且只有非极性键;B的分子由四个原子构成,既有极性键也有非极性键;C分子也是由四个原子构成且只有一种类型的化学键。A、B、C在常温下状态分别是 ( )
A.固、液、液 B.气、液、气 C.液、液、气 D.气、气、气
3.相同质量的下列各烃,完全燃烧后生成水最多的是 ( )
A.甲烷 B.乙烷 C.乙烯 D.乙炔
2.下列各物质中,互为同系物的是 ( )
A.
B.
C.
D.乙酸和硬脂酸
1.有机物 的名称是 ( )
的名称是 ( )
A.2,3,3-三甲基丁烷 B.2,3-三甲基丁烷
C.2,2,3-三甲基丁烷 D.2,3-三甲基丁烷
31.把由NaOH、AlCl3和MgCl2三种固体组成的混合物溶于足量水中,有1.16g白色沉淀析出,向所得溶液里逐滴加入1 mol/L的盐酸,加入盐酸的体积和沉淀的质量如图所示:
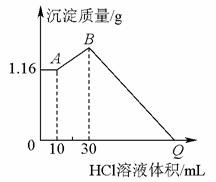
(1)A点的沉淀物的化学式为____________________;
B点的沉淀物的化学式为____________________。
(2)原混合物中MgCl2的质量是__________g,AlCl3的质量是__________g,NaOH的质量是__________g。
(3)Q点HCl溶液的体积为__________mL。Ks*5u
30.用中和滴定测定某烧碱的纯度,试根据实验回答下列有关问题:
(1)配制待测溶液:将准确称量的4.10g含有少量中性易溶杂质的固体烧碱,配成250ml待测溶液,主要用到的仪器是 。(至少填2个)
(2)滴定时,用0.2mol/L的盐酸来滴定待测溶液,带有玻璃活塞的滴定管盛放 ;进行滴定时, 手旋转滴定管的玻璃活塞, 手不停轻摇锥形瓶,眼睛看着 。
(3)根据下表的数据,计算被测烧碱溶液的物质的量浓度是 ,烧碱的纯度是 ;
|
滴定次数 |
待测液体积(ml) |
滴定前标准溶液刻度(ml) |
滴定后标准溶液刻度(ml) |
|
第一次 |
10.0 |
0.50 |
20.40 |
|
第二次 |
10.0 |
4.00 |
24.10 |
(4)若将锥形瓶用待测液润洗,然后再盛放待测液10ml,滴定(其它操作无误)结果 ;(填“偏高”或“偏低”或“正常”,下同)Ks*5u
(5)观察酸式滴定管内液面时,开始平视,滴定终点俯视,则结果 。
29.相同浓度的NH4HSO4和(NH4)2SO4 溶液,都呈 性,前者显此性的主要原因是 ,后者显此性的原因是 。(用离子反应方程式表示。)
28.要除去下列物质中所含杂质(括号内为杂质),请将选用的试剂及分离方法填在题后的横线上,并写出有关反应的化学方程式(是离子反应的写出离子方程式)。
(1)Al2O3[Al(OH)3]________________________________________。
 (2) Fe(Al)____________________ ____________________。
(2) Fe(Al)____________________ ____________________。
(3)Fe2O3(Al2O3)________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com