
题目列表(包括答案和解析)
4.在可逆反应中,平衡常数与反应进行的限度关系正确的是
A.K越大,反应程度越大 B.K越大,反应程度越小
C.K的大小与反应程度无关 D.K越大,反应程度可能变大,也可能变小
3.下列各式中,表示水解反应的是
A.H2O
+ H2O H3O++ OH- B.CO32-+ H2O
H3O++ OH- B.CO32-+ H2O  HCO3-+ OH-
HCO3-+ OH-
C.NH3
+ H2O  NH3·H2O
D.HCO3-+ H2O
NH3·H2O
D.HCO3-+ H2O  H3O++ CO32-
H3O++ CO32-
2.对于任何一个平衡体系,采用以下措施,一定会使平衡移动的是
A.加入一种反应物 B.使用催化剂
C.对平衡体系增加压 D.升高温度
1.下列变化过程中,ΔS<0的是
A.氯化钠溶于水中 B.NH3(g)和HCl(g)反应生成NH4Cl(s)
C.干冰的升华 D.CaCO3(s)分解为CaO(s)和CO2(g)
23. (9分)常温下,有PH=12的NaOH溶液100ml,若将其PH变为11 ,(溶液混合造成的误差忽略不计,计算结果保留小数点后一位)。
(1)若用蒸馏水应加入 mL
(2)若用pH=10的NaOH溶液应加入 mL (3)若用pH=2的盐酸应加入 mL;
2010-2011学年上期高2012级第二次阶段性考试
22.(11分) (1) 用pH试纸测定溶液pH的正确操作是___________________
A.将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照
B.将一小块试纸用蒸馏水润湿后放在表面皿上,用玻璃蘸取少量待测液点在试纸上,再与标准比色卡对照
C.将一小条试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照
D.将一小条试纸先用蒸馏水润湿后,在待测液中蘸一下,取出后与标准比色卡对照
(2) 分别称取0.20g的NaOH固体两份,加入适量的蒸馏水溶解,用未知浓度的盐酸滴定,如两次所耗盐酸的体积分别为:25.02mL、24.98mL。
①若选用酚酞作为指示剂,滴定终点溶液由______色变为_____色,且半分钟内不褪色;
②该盐酸的物质的量浓度为_____________________________mol·L-1;
③测定所用的主要玻璃仪器为_____________________________________;
④下列操作会使盐酸浓度偏高的是:___________________________(填序号)。
A.滴定前滴定管尖嘴部分有气体
B.滴定过程中振荡时锥形瓶内有溶液溅出
C.NaOH中混有少量的Na2CO3
D.滴定前俯视滴定管
E.滴定后俯视滴定管
F.未用盐酸溶液润洗滴定管
21.(9分)已知在水溶液中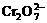 离子呈橙红色,
离子呈橙红色, 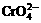 离子呈黄色, Cr3+离子呈绿色。当K2Cr2O7溶于水时,
有下列平衡:
离子呈黄色, Cr3+离子呈绿色。当K2Cr2O7溶于水时,
有下列平衡: 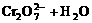
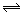
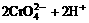 。
。
(1)若向K2Cr2O7溶液里滴加H2SO4溶液, 观察到的现象是 , 简述理由 ;
(2)若向(1)所得溶液里通入H2S气体, 观察到溶液呈绿色、并有淡黄色沉淀生成, 其原因是 , 有关反应的离子方程式为 ;
(3)另取1份K2Cr2O7溶液, 逐滴加入少量NaOH溶液, 观察到的现象是 , 其原因是 。
20.(6分)(1) 把AlCl3溶液蒸干后再灼烧,最后得到的固体产物主要是
其原因是 。
(2) Na2CO3溶液能否贮存在玻璃塞试剂瓶中? , (填“能”或“否”),原因是 _________________________(用离子方程式表达)。
19.(10分)在 2 L的密闭容器中, 充入 1 mol N2 和 3 mol H2,
在一定的条件下反应N2+ 3H2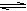 2NH3, 2 分钟后达到平衡状态,
相同温度下, 测得平衡时混合气体的压强比反应前混合气体的压强减小了 1/10, 填写下列空白:
2NH3, 2 分钟后达到平衡状态,
相同温度下, 测得平衡时混合气体的压强比反应前混合气体的压强减小了 1/10, 填写下列空白:
(1) 平衡时混合气体中三种气体的物质的量比为 _________________
(2) H2 的转化率为 _______________
(3) 2分钟内, N2的平均反应速率为 _______________
(4) 若反应温度不变,向2 L的密闭容器中再充入1mol N2 和 3 mol H2,达到新平衡后,N2 的转化率比原平衡______________(填“增大”.“减小”或“不变”)。
(5)若反应温度不变,向2 L的密闭容器中充入a mol N2 、b mol H2和C mol NH3,使反应开始时向逆反应方向进行,达到平衡后,混合气体的各物质组成浓度不变,则加入的氨气C的取值范围是______________ 。
18. (7分)在一个密闭容器中,有可逆反应SO2+NO2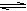 SO3(s)+NO(正反应是放热反应)达到化学平衡,改变条件化学平衡有:
SO3(s)+NO(正反应是放热反应)达到化学平衡,改变条件化学平衡有:
(1)升高温度,化学平衡向__________方向移动,气体颜色变_________
(2)缩小体积,化学平衡向__________方向移动,气体颜色变_________
(3)加入正催化剂,化学平衡_________。
(4)若保持体积不变,向平衡混合物中再充入1molHe,当反应重新达到平衡时,平衡混合物中NO2的物质的量 (填“增多”.“减少”或“不变”)
若保持压强不变,向平衡混合物中再充入1molHe,当反应重新达到平衡时,平衡混合物中NO2的物质的量 (填“增多”.“减少”或“不变”)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com