
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
26ЃЎ(12Зж)WЁЂXЁЂYЁЂZОљЮЊЖЬжмЦкжїзхдЊЫиЃЌWЕФзюЭтВуЕчзгЪ§гыКЫЭтЕчзгзмЪ§жЎБШЮЊ3:8ЃЛXЕФКЫЭтЕчзгзмЪ§гыYЕФзюЭтВуЕчзгЪ§ЯрЕШЃЌXЕФдзгађЪ§ЪЧZЕФдзгађЪ§ЕФвЛАыЃЛWЁЂYЁЂZЮЛгкЭЌвЛжмЦкЁЃ (1)WЕФЕЅжЪЪЧвЛжжЁЁЁЁЁЁЩЋОЇЬхЁЃ (2)WЁЂYЁЂZШ§жждЊЫиЕФЦјЬЌЧтЛЏЮяЮШЖЈадгЩИпЕНЕЭЕФЫГађЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (гУЛЏбЇЪНБэЪОЃЌZЕФЦјЬЌЧтЛЏЮягыЦфЭЌжїзхдЊЫиЦјЬЌЧтЛЏЮяЛЏбЇЪНаДЗЈЯрЫЦЁЃ)ЁЃ (3)вбжЊAЁЂBЁЂCЁЂDЫФжжЮяжЪДцдкШчЯТЗДгІЙиЯЕЃКA + BЁњC + D ЁЁЁЁЂйШєAЪЧYКЭZГЃМћМлЬЌЕФЛЏКЯЮяЃЌBЪЧXЕФЧтЛЏЮяЃЌDЪЧYЕФЧтЛЏЮяЃЌЗДгІЙ§ГЬжаУЛгаЛЏКЯМлБфЛЏЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ ЁЁЁЁЂкШєAЪЧZЕФЕЅжЪЃЌBЮЊКьЩЋЙЬЬхЃЌDЮЊзЯКьЩЋЙЬЬхЕЅжЪЃЌИпЮТЯТЗЂЩњИУЗДгІЃЌCЕФЛЏбЇЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃDгыXдЊЫизюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяЕФХЈШмвКЗДгІЃЌЩњГЩЕФЦјЬхЛсЖдДѓЦјдьГЩЮлШОЃЌЦфЛЏбЇЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃгУЩеМюШмвКЮќЪеИУЦјЬхЩњГЩСНжжбЮЃЌЦфжавЛжжбЮПЩгУзїЗРИЏМСЃЌЩеМюШмвКЮќЪеЦјЬхЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
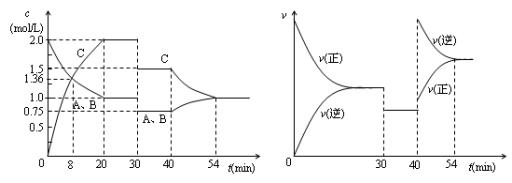
25ЃЎФГУмБеШнЦїжаГфШыЕШЮяжЪЕФСПЕФЦјЬхAКЭBЃЌвЛЖЈЮТЖШЯТЗЂЩњЗДгІA(g)+xB(g) 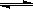 2C(g)ЃЌДяЕНЦНКтКѓЃЌжЛИФБфЗДгІЕФвЛИіЬѕМўЃЌВтЕУШнЦїжаЮяжЪЕФХЈЖШЁЂЗДгІЫйТЪЁЁЫцЪБМфБфЛЏЕФШчЯТЭМЫљЪОЁЃЯТСаЫЕЗЈжае§ШЗЪЧ
ЁЁAЃЎ30minЪБНЕЕЭЮТЖШЃЌ40minЪБЩ§ИпЮТЖШ
ЁЁBЃЎ8minЧАAЕФЦНОљЗДгІЫйТЪЮЊ0.08mol/(LЁЄmin)
ЁЁCЃЎЗДгІЗНГЬЪНжаЕФxЃН1ЃЌе§ЗДгІЮЊЮќШШЗДгІ
ЁЁDЃЎ20min-40minМфИУЗДгІЕФЦНКтвЦЖЏСЫ
2C(g)ЃЌДяЕНЦНКтКѓЃЌжЛИФБфЗДгІЕФвЛИіЬѕМўЃЌВтЕУШнЦїжаЮяжЪЕФХЈЖШЁЂЗДгІЫйТЪЁЁЫцЪБМфБфЛЏЕФШчЯТЭМЫљЪОЁЃЯТСаЫЕЗЈжае§ШЗЪЧ
ЁЁAЃЎ30minЪБНЕЕЭЮТЖШЃЌ40minЪБЩ§ИпЮТЖШ
ЁЁBЃЎ8minЧАAЕФЦНОљЗДгІЫйТЪЮЊ0.08mol/(LЁЄmin)
ЁЁCЃЎЗДгІЗНГЬЪНжаЕФxЃН1ЃЌе§ЗДгІЮЊЮќШШЗДгІ
ЁЁDЃЎ20min-40minМфИУЗДгІЕФЦНКтвЦЖЏСЫ
 Ш§ЁЂЬюПеЬт(ЙВ5ИіЬтЃЌзмМЦ50Зж)
Ш§ЁЂЬюПеЬт(ЙВ5ИіЬтЃЌзмМЦ50Зж)
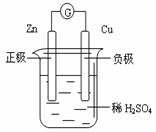
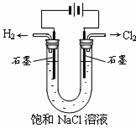
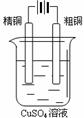
23ЃЎЯТЭМгаЙиЕчЛЏбЇЕФЪОвтЭМе§ШЗЕФЪЧ
 ЁЁ
ЁЁ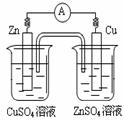 ЁЁЁЁЁЁ
ЁЁЁЁ
A.ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ
B.ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁ
ЁЁЁЁ C. ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁD.
24ЃЎЯТСаЛЏКЯЮяжаМШвзЗЂЩњШЁДњЗДгІЃЌвВПЩЗЂЩњМгГЩЗДгІЃЌЛЙФмЪЙKMn04ЫсадШмвКЭЪЩЋЕФЪЧ
ЁЁAЁЂввЭщЁЁЁЁЁЁЁЁЁЁ BЁЂввДМЁЁЁЁЁЁЁЁЁЁ CЁЂБћЯЉЁЁ ЁЁЁЁЁЁ DЁЂБН
ЁЁЁЁЁЁ
ЁЁЁЁ
A.ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ
B.ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁ
ЁЁЁЁ C. ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁD.
24ЃЎЯТСаЛЏКЯЮяжаМШвзЗЂЩњШЁДњЗДгІЃЌвВПЩЗЂЩњМгГЩЗДгІЃЌЛЙФмЪЙKMn04ЫсадШмвКЭЪЩЋЕФЪЧ
ЁЁAЁЂввЭщЁЁЁЁЁЁЁЁЁЁ BЁЂввДМЁЁЁЁЁЁЁЁЁЁ CЁЂБћЯЉЁЁ ЁЁЁЁЁЁ DЁЂБН
22ЃЎФГШмвКжаFeCl3ЕФЫЎНтЗДгІвбДяЦНКт.FeCl3+3H2O 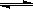 ЁЁFe(OH)3+3HClШєвЊЪЙFeCl3ЕФЫЎНтГЬЖШдіДѓЃЌгІВЩШЁЕФЗНЗЈЪЧ
ЁЁAЃЎМгШыNaHCO3 ЁЁ BЃЎМгШыAgNO3ЁЁЁЁЁЁЁЁЁЁЁЁ
CЃЎМгFeCl3ЙЬЬхЁЁ DЃЎМгШШ
ЁЁFe(OH)3+3HClШєвЊЪЙFeCl3ЕФЫЎНтГЬЖШдіДѓЃЌгІВЩШЁЕФЗНЗЈЪЧ
ЁЁAЃЎМгШыNaHCO3 ЁЁ BЃЎМгШыAgNO3ЁЁЁЁЁЁЁЁЁЁЁЁ
CЃЎМгFeCl3ЙЬЬхЁЁ DЃЎМгШШ
16ЃЎЯТСаа№Ъіе§ШЗЕФЪЧ ЁЁAЃЎSO2ФмЙЛЪЙЫсадKMnO4ШмвКЭЪЩЋЪЧвђЮЊЦфОпгаЦЏАзад ЁЁBЃЎЮэЪєгкНКЬхЃЌдкДѓЮэМАЩГГОЬьЦјвЊзЂвтГіааАВШЋ ЁЁCЃЎН№ЪєТСБШНЯЛюЦУЃЌПЩЭЈЙ§ЕчНтШлШкТШЛЏТСРДжЦБИ ЁЁDЃЎCl2ОпгаЧПбѕЛЏадЃЌФмЪЙИЩдягаЩЋВМЬѕЭЪЩЋ 17ЃЎвбжЊH2 (g)ЁЂC2H4(g)КЭC2H5OH(1)ЕФШМЩеШШЗжБ№ЪЧ285.8kJЁЄmol-1ЁЂ1411.0kJЁЄmol-1КЭ1366.8kJЁЄmol-1,дђгЩC2H4(g)КЭH2O(I)ЗДгІЩњГЩC2H5OH(I)ЕФЁїHЮЊ ЁЁ A.-44.2kJЁЄmol-1ЁЁЁЁЁЁ B.+44.2kJЁЄmol-1ЁЁЁЁC.-330kJЁЄmol-1ЁЁЁЁЁЁЁЁ D.+330kJЁЄmol-1 18ЃЎвбжЊCl2ЁЂAl2S3ЁЂCaC2ЁЂC2H5BrЁЂCH3COOCH3ЕШЮяжЪЕФОљФмгыЫЎЗЂЩњЗДгІЃЌЗДгІПЩЪгЮЊИїЮяжЪКЭЫЎОљЗжБ№РыНтГЩСНВПЗжЃЌШЛКѓдйСНСНжиаТзщКЯЃЌаЮГЩаТЕФЮяжЪЁЃЯТСаЛЏбЇЗДгІЗћКЯетвЛЬиЕуЕФЪЧЃКЂйICl+H2OЃНHIO+HClЃЛЁЁЂкCH3COCl+H2OЁњCH3COOH+HClЃЛЂлCaC2+2H2OЁњCa(OH)2+C2H2 ЁќЃЛЂмMg3N2+6H2OЃН3Mg(OH)2+2NH3ЁќЃЛЂнSiCl4+4H2OЃНH4SiO4Ё§+4HClЁќЁЃ ЁЁAЃЎжЛгаЂйЂмЂнЁЁЁЁ BЃЎжЛгаЂкЂлЂнЁЁЁЁ CЃЎжЛгаЂйЂкЂлЂмЁЁЁЁ DЃЎШЋВП 19ЃЎНЋФГаЉЛЏбЇжЊЪЖгУЪ§жсБэЪОжБЙлаЮЯѓЁЂМђУївзМЧЁЃЯТСагУЪ§жсБэЪОе§ШЗЕФЪЧ
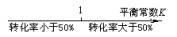 AЃЎЦНКтГЃЪ§гызЊЛЏТЪЙиЯЕЃК
AЃЎЦНКтГЃЪ§гызЊЛЏТЪЙиЯЕЃК
ЁЁ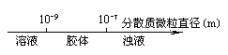
BЃЎЗжЩЂЯЕЕФЗжРргыЗжЩЂжЪСЃжБОЖДѓаЁЙиЯЕЃК ЁЁ
CЃЎAlCl3КЭNaOHЗДгІКѓТСдЊЫиЕФДцдкаЮЪНгыЗДгІЮяжаn(OHЃ)/n(Al3+)ЁЁЕФЙиЯЕЃКЁЁ
ЁЁЁЁ
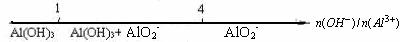
ЁЁDЃЎNaгыO2ЗДгІЕФВњЮягыЗДгІЮяn(Na)/n(O2)
ЕФЙиЯЕЃК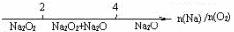 20ЃЎЖЬжмЦкдЊЫиW ЁЂXЁЂYЁЂZЕФдзгађЪ§вРДЮдіДѓЃЌЧвW ЁЂXЁЂYЁЂZЕФзюЭтВуЕчзгЪ§гыЦфЕчзгВуЪ§ЕФБШжЕвРДЮЮЊ2 ЁЂ3ЁЂ
20ЃЎЖЬжмЦкдЊЫиW ЁЂXЁЂYЁЂZЕФдзгађЪ§вРДЮдіДѓЃЌЧвW ЁЂXЁЂYЁЂZЕФзюЭтВуЕчзгЪ§гыЦфЕчзгВуЪ§ЕФБШжЕвРДЮЮЊ2 ЁЂ3ЁЂ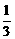 ЁЂ2(ВЛПМТЧСузхдЊЫи)ЁЃЯТСаЙигкетаЉдЊЫиЕФа№ЪіДэЮѓЕФЪЧ
ЁЁAЃЎXКЭЦфЫћШ§жждЊЫиОљПЩаЮГЩжСЩй2жжЖўдЊЛЏКЯЮя
ЁЁBЃЎWКЭXЁЂZСНжждЊЫиЗжБ№аЮГЩЕФЖўдЊЛЏКЯЮяжаЃЌОљгажБЯпаЮЗжзг
ЁЁCЃЎW ЁЂXКЭYШ§жждЊЫиПЩвдаЮГЩМюадЛЏКЯЮя
ЁЁDЃЎZКЭЦфЫћШ§жждЊЫиаЮГЩЕФЖўдЊЛЏКЯЮяЃЌЦфЫЎШмвКОљГЪЫсад
21ЃЎЯТСаШмвКжаЮЂСЃЕФЮяжЪЕФСПХЈЖШЙиЯЕе§ШЗЕФЪЧ
ЁЁAЃЎЪвЮТЯТ,Яђ0ЃЎ01 molЁЄLЃ1NH4HSO4ШмвКжаЕЮМгNaOHШмвКжСжаадЃК
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
c(Na+)ЃОc(SO42Ѓ)ЃОc(NH4+)ЃОc(OHЃ)=c(H+)
ЁЂ2(ВЛПМТЧСузхдЊЫи)ЁЃЯТСаЙигкетаЉдЊЫиЕФа№ЪіДэЮѓЕФЪЧ
ЁЁAЃЎXКЭЦфЫћШ§жждЊЫиОљПЩаЮГЩжСЩй2жжЖўдЊЛЏКЯЮя
ЁЁBЃЎWКЭXЁЂZСНжждЊЫиЗжБ№аЮГЩЕФЖўдЊЛЏКЯЮяжаЃЌОљгажБЯпаЮЗжзг
ЁЁCЃЎW ЁЂXКЭYШ§жждЊЫиПЩвдаЮГЩМюадЛЏКЯЮя
ЁЁDЃЎZКЭЦфЫћШ§жждЊЫиаЮГЩЕФЖўдЊЛЏКЯЮяЃЌЦфЫЎШмвКОљГЪЫсад
21ЃЎЯТСаШмвКжаЮЂСЃЕФЮяжЪЕФСПХЈЖШЙиЯЕе§ШЗЕФЪЧ
ЁЁAЃЎЪвЮТЯТ,Яђ0ЃЎ01 molЁЄLЃ1NH4HSO4ШмвКжаЕЮМгNaOHШмвКжСжаадЃК
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
c(Na+)ЃОc(SO42Ѓ)ЃОc(NH4+)ЃОc(OHЃ)=c(H+)
ЁЁBЃЎ0ЃЎ1 molЁЄLЃ1NaHCO3ШмвКЃКc(Na+)ЃОc(OHЃ)ЃОc(HCO3Ѓ)ЃОc(H+) ЁЁCЃЎNa2CO3ШмвКЃКc(OHЃ)Ѓc(H+)=c(HCO3Ѓ)+ 2c(H2CO3) ЁЁDЃЎ 25ЁцЪБЃЌpH=4.75ЁЂХЈЖШОљЮЊ0.1 molЁЄLЃ1ЕФCH3COOHЁЂCH3COONaЛьКЯШмвКЃК
c(CH3COOЃ)+c(OHЃ)<C(CH3COOH)+C(H+)
15ЃЎдквЛЖЈЮТЖШЯТЬхЛ§ЙЬЖЈЕФУмБеШнЦїжа,ЕБЯТСаЮяРэСП:
ЂйЛьКЯЦјЬхЕФбЙЧП Ђк ЦјЬхЕФзмЮяжЪЕФСП ЂлЛьКЯЦјЬхЕФУмЖШЂмBЕФЮяжЪЕФСПХЈЖШВЛдйБфЛЏЪБ,ФмБэУїПЩФцЗДгІA(s)+2B(g) 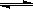 C(g)+D(g)вбДяЦНКтЕФЪЧ
ЁЁAЃЎЂйЂкЁЁЁЁЁЁ ЁЁBЃЎ ЂлЂмЁЁ ЁЁЁЁ CЃЎ ЂйЂмЁЁЁЁ ЁЁ
DЃЎжЛгаЂм
C(g)+D(g)вбДяЦНКтЕФЪЧ
ЁЁAЃЎЂйЂкЁЁЁЁЁЁ ЁЁBЃЎ ЂлЂмЁЁ ЁЁЁЁ CЃЎ ЂйЂмЁЁЁЁ ЁЁ
DЃЎжЛгаЂм
13ЃЎЯТСаНтЪЭЪЕбщЪТЪЕЕФЗНГЬЪНВЛзМШЗЕФЪЧ
ЁЁAЃЎ0.1 mol/L CH3COOHШмвКЕФpHЃО1ЃКCH3COOH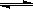 CH3COOЃ+H+
ЁЁBЃЎЁАNO2ЧђЁБНўХндкРфЫЎжаЃЌбеЩЋБфЧГЃК2NO2(g)
CH3COOЃ+H+
ЁЁBЃЎЁАNO2ЧђЁБНўХндкРфЫЎжаЃЌбеЩЋБфЧГЃК2NO2(g) 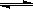 N2O4(g)
ЁЁІЄHЃМ0
ЁЁCЃЎЬњШмгкЯЁЯѕЫсЃЌШмвКБфЛЦЃК3Fe+8H++2NO3Ѓ===3Fe2++2NOЁќ+4H2O
ЁЁDЃЎЯђNa2CO3ШмвКжаЕЮШыЗгЬЊШмвКЃЌШмвКБфКьЃКCO32Ѓ+H2O
N2O4(g)
ЁЁІЄHЃМ0
ЁЁCЃЎЬњШмгкЯЁЯѕЫсЃЌШмвКБфЛЦЃК3Fe+8H++2NO3Ѓ===3Fe2++2NOЁќ+4H2O
ЁЁDЃЎЯђNa2CO3ШмвКжаЕЮШыЗгЬЊШмвКЃЌШмвКБфКьЃКCO32Ѓ+H2O 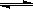 HCO3Ѓ+OHЃ
14ЃЎЯТСаИїзщЮяжЪжаЃЌФмЗЂЩњВЛЭЌЛЏбЇЗДгІЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ ЁЁЂйCгыO2
ЁЁЁЁЁЁЂкPгыCl2
ЁЁЁЁЂлFeгыCl2
ЁЁЁЁЂмNaгыO2
ЁЁЁЁЂнCO2гыNaOHШмвК
ЁЁЁЁ ЂоCuгыЯѕЫсЁЁЁЁЂпH2SгыO2ЁЁ
ЁЁЁЁЁЁЂрAlCl3ШмвКгыАБЫЎ
ЁЁAЃЎГ§ЂлЭтЁЁЁЁЁЁ
BЃЎГ§ЂлЂрЭтЁЁЁЁЁЁ ЁЁCЃЎГ§ЂлЂпЭтЁЁЁЁЁЁЁЁ ЁЁDЃЎГ§ЂоЂпЂрЭт
HCO3Ѓ+OHЃ
14ЃЎЯТСаИїзщЮяжЪжаЃЌФмЗЂЩњВЛЭЌЛЏбЇЗДгІЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ ЁЁЂйCгыO2
ЁЁЁЁЁЁЂкPгыCl2
ЁЁЁЁЂлFeгыCl2
ЁЁЁЁЂмNaгыO2
ЁЁЁЁЂнCO2гыNaOHШмвК
ЁЁЁЁ ЂоCuгыЯѕЫсЁЁЁЁЂпH2SгыO2ЁЁ
ЁЁЁЁЁЁЂрAlCl3ШмвКгыАБЫЎ
ЁЁAЃЎГ§ЂлЭтЁЁЁЁЁЁ
BЃЎГ§ЂлЂрЭтЁЁЁЁЁЁ ЁЁCЃЎГ§ЂлЂпЭтЁЁЁЁЁЁЁЁ ЁЁDЃЎГ§ЂоЂпЂрЭт
11ЃЎдкЯТСаИјЖЈЬѕМўЕФШмвКжаЃЌвЛЖЈФмДѓСПЙВДцЕФРызгзщЪЧ
ЁЁAЃЎc(Fe3+) = 0.1 mol/LЕФШмвКжаЃКK+ЁЂClOЃЁЂSO42ЃЁЂSCNЃ
ЁЁBЃЎЮоЩЋЕФШмвКЃКNa+ЁЂNH4+ЁЂFe2+ЁЂNO3Ѓ
ЁЁCЃЎМзЛљГШГЪЛЦЩЋЕФШмвКжаЃКIЃЁЂClЃЁЂNO3ЃЁЂNa+
ЁЁDЃЎ 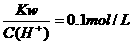 ЕФШмвКЃКNa+ЁЂK+ЁЂSiO32ЃЁЂNO3Ѓ
12ЃЎЯТСаРызгЗНГЬЪНБэДяе§ШЗЕФЪЧ
ЁЁAЃЎгУFeCl3ШмвКИЏЪДЭЯпТЗАхЃКCu + 2Fe3+ ЃНCu2+ + 2Fe2+
ЕФШмвКЃКNa+ЁЂK+ЁЂSiO32ЃЁЂNO3Ѓ
12ЃЎЯТСаРызгЗНГЬЪНБэДяе§ШЗЕФЪЧ
ЁЁAЃЎгУFeCl3ШмвКИЏЪДЭЯпТЗАхЃКCu + 2Fe3+ ЃНCu2+ + 2Fe2+
ЁЁBЃЎгУЧтбѕЛЏФЦШмвКГ§ШЅТСБэУцЕФбѕЛЏФЄЃКAl2O3+2OHЃЃН2AlO2Ѓ+H2O ЁЁCЃЎNa2O2гыH2OЗДгІжЦБИO2ЃКNa2O2 +H2O ЃН2Na+ + 2OHЃ+O2Ёќ ЁЁDЃЎЯђДЮТШЫсИЦШмвКЭЈШыSO2ЃКCa2++2ClOЃ+H2O+SO2ЃНCaSO3Ё§+2HClO
10ЃЎ4gФГжжЬњЕФбѕЛЏЮяЃЌгУзуСПЕФвЛбѕЛЏЬМдкИпЮТЯТНЋЦфЛЙдЃЌдйАбЩњГЩЕФЖўбѕЛЏЬМШЋВПЭЈШызуСПГЮЧхЕФЪЏЛвЫЎЃЌЕУЕН7.5gГСЕэЮя,ИУЬњЕФбѕЛЏЮяЪЧ ЁЁAЃЎFe3O4 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎFeOЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎFe2O3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎFeOКЭFe3O4 ЖўЁЂВЛЖЈЯюбЁдёЬт(УПИіЬтжЛгавЛжСЖўИібЁЯюЪЧе§ШЗЕФЃЌУПЬт2ЗжЃЌЙВ30Зж)
9ЃЎЯТСаа№Ъіе§ШЗЕФЪЧ
ЁЁAЃЎввЯЉКЭБНЖМЪЙфхЫЎЭЪЩЋЃЌЭЪЩЋЕФдвђВЛЯрЭЌ
ЁЁBЃЎвКЛЏЦјКЭЬьШЛЦјЕФжївЊГЩЗжЖМЪЧМзЭщ
ЁЁCЃЎ 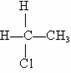 ЁЁКЭ
ЁЁКЭ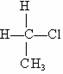 ЛЅЮЊЭЌЗжвьЙЙЬх
ЁЁDЃЎЦћгЭЁЂВёгЭКЭжВЮягЭЖМЪЧЬМЧтЛЏКЯЮя
ЛЅЮЊЭЌЗжвьЙЙЬх
ЁЁDЃЎЦћгЭЁЂВёгЭКЭжВЮягЭЖМЪЧЬМЧтЛЏКЯЮя
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com