
题目列表(包括答案和解析)
24.(共15分)
(1)① 、 ②
③ 、
(2)①
②
、 ③
(3)① ② 、
③ 、
26.(10分)工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁。
(1)工业上可用氨催化吸收法处理NOx ,反应原理如下:
4xNH3 +6 NOx  (2x
+ 3)N2 + 6xH2O
(2x
+ 3)N2 + 6xH2O
某化学兴趣小组模拟该处理过程的实验装置如下:
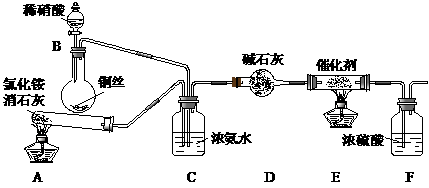
①装置A中发生反应的化学方程式为 ▲ 。
②装置C的作用是 ▲ 。
③装置F的作用是 ▲ 。
(2)工业上也常用Na2CO3溶液吸收法处理NOx 。
已知: NO不能与Na2CO3溶液反应,。
NO + NO2 + Na2CO3 = 2NaNO2 + CO2 (I)
2NO2 + Na2CO3 = NaNO2 + NaNO3 + CO2 (II)
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是 ▲ (填字母)。
A.1.3 B.1.6 C.1.8
②将1mol NOx 通入Na2CO3溶液中,被完全吸收时,溶液中生成的NO3ˉ、NO2ˉ两种离子的物质的量随x变化关系如图所示:
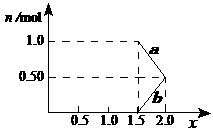
图中线段a表示 ▲ 离子随x值变化的关系;若用溶质质量分数为21.2%的 Na2CO3溶液吸收,则需要Na2CO3溶液至少 ▲ g。
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则NOx中的x值为 ▲ 。
(3)氨催化吸收法和Na2CO3溶液吸收法处理NOx尾气共同的优点是 ▲ 。
 江苏省扬州中学高二化学学业水平考试答卷纸2011.3.12
江苏省扬州中学高二化学学业水平考试答卷纸2011.3.12
25.(6分)常见金属单质A、B和非金属单质C、D以及它们化合物之间的转化关系如下。F、J既能溶于强酸M又能溶于强碱N,Z的摩尔质量为198 g·mol-1,且其中各元素的质量比为:
钾 : 金属B : 氧 =39 : 28 : 32。
请回答下列问题:
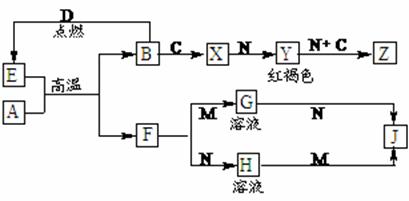
(1)Z的化学式为: ▲ 。
(2)写出检验X中阳离子的方法: ▲ 。
(3)写出E和A在高温下反应的化学方程式为: ▲ 。
(4)写出A和N反应的离子方程式: ▲ 。
24.本题有A、B两题,分别对应于《化学与生活》和《有机化学基础》两个选修模块的内容。请选择其中一题作答。
A.《化学与生活》(15分)
⑴(5分)随着生活水平的提高,人们越来越关注营养平衡和自身的健康。
①粮食中的淀粉在人体中水解最终转化成 ▲ ,该物质在人体内被氧化,最终生成CO2和H2O,该过程对人体健康的意义是 ▲ 。
②食品添加剂亚硝酸钠的外观像食盐,并有咸味,但亚硝酸钠有很强的毒性。亚硝酸钠属于 ▲ (选填“调味剂”、“防腐剂”或“着色剂”)。
③维生素C也称抗坏血酸。血液中运载氧的血红蛋白中含有Fe2+,人之所以患坏血 病,是因为人体从摄取的食物中吸收的铁主要是Fe3+,Fe3+不能被人体吸收。维生素C的主要摄入途径是 ▲ ,维生素C在抗坏血病方面的作用原理是 ▲ 。
⑵(5分)中国是世界上最早研究和生产合金的国家之一。
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点 ▲ 。
②铜锌合金外观和金(Au)相似,常被误认为黄金。试写出一种鉴别黄铜与黄金的化学方法 ▲ 。铜器表面容易生成一层薄薄的铜绿[主要成份是Cu2(OH)2CO3],请写出铜在潮湿的空气发生电化学腐蚀时的负极反应式 ▲ ;用盐酸可以除去铜器表面的铜绿,该反应的化学方程式为 ▲ 。
③下列对金属制品采取的防护方法不正确的是 ▲ (填序号)。
A.在电线的外面包上一层塑料层
B.在自行车钢圈上镀上一层金属铬
C.在海轮的铁制外壳上焊上铜块
⑶(5分)
①CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。请你写出有利于降低大气中CO2浓度的一项措施 ▲ 。
②水中含有的悬浮颗粒物等杂质,可以加入 ▲ 等混凝剂进行净化处理,利用其溶解后形成的 ▲ 具有吸附作用使水中的悬浮颗粒物沉降。
③最近,国内第一个跨区域日处理垃圾1000吨以上的垃圾焚烧发电厂在江苏如皋投入使用。下面列出了现代生活中的常见垃圾:
A.废纸 B.废电池 C.易拉罐 D.玻璃瓶 E.塑料制品
在焚烧处理前,除废电池外,还有 ▲ (填序号)应剔除并回收,随意丢弃电池造成的主要危害是 ▲ 。
23.某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取10mL废液加入足量的AgNO3溶液,生成沉淀 8.61g。(2)另取10mL废液放入铜片充分反应,铜片质量减少了0.256g。下列关于原废液组成的判断错误的是
A.一定含有Fe 2+、Fe 3+、Cu2+、Clˉ B.c(Fe2+)︰c(Cu2+) = 2︰1
C.c(Fe2+)︰c(Fe 3+) = 3︰1 D.c(Clˉ) = 6mol / L,c(Fe 2+) = 1.2mol / L
22.短周期元素A、B、C、D的原子序数依次递增,它们的原子序数之和为34,且原子最外层电子数之和为10;A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D均为同主族元素。下列叙述正确的是
A. B、D的最高价氧化物都不能和酸反应 B.最高价氧化物对应的水化物的碱性:A>C
C.A的原子半径为这四种当中最小的 D.四种元素中B形成化合物的种类最多
21. 已知离子可在琼脂中移动。某简易电池如图所示。
已知离子可在琼脂中移动。某简易电池如图所示。
放电时,下列说法错误的是
A.锌极上电极反应式为:Zn-2e-= Zn2+
B.MnO2得电子被还原
C.NH4+ 离子通过琼脂向锌极移动
D.外电路电流的方向从碳棒到锌片
20.用NA表示阿伏加德罗常数的值,下列说法正确的是
A.常温常压下,48 g O3含有的氧原子数约为3NA
B.常温常压下,11.2 L乙烯(C2H4)含有2NA个碳原子
C.1.7 g氨气所含有的电子数目为10 NA
D.2.7g铝与足量氢氧化钠溶液反应转移的电子数NA
19.国家质检总局调查结果显示:所谓毒奶粉是被三聚氰胺所污染,它可由三聚氰酸[C3N3(OH)3]制备.三聚氰酸可用于消除汽车尾气中的NO2,已知三聚氰酸中氮元素的化合价为-3价,HCNO中N为-3价,O为-2价,有关反应原理为:
① C3N3(OH)33HCNO; ② 8HCNO+6NO27N2+8CO2+4H2O
下列说法正确的是
A.反应①中的两种物质互为同素异形体 B.反应②中HCNO是氧化剂
C.反应②中NO2是还原剂 D.反应②中转移的电子数为24
18.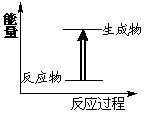 关于化学反应中的说法错误的是
关于化学反应中的说法错误的是
A.化学键断裂吸收能量,化学键生成放出能量
B.化学反应中有物质变化也有能量变化
C.右图所示的反应为放热反应
D. 需要加热的化学反应不一定是吸热反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com