
题目列表(包括答案和解析)
9.下列各组热化学方程式中,△H1>△H2的是( )
①C(s)+O2(g)===CO2(g) △H1 C(s)+O2(g)===CO(g) △H2
②S(s)+O2(g)===SO2(g) △H1 S(g)+O2(g)===SO2(g) △H2
③H2(g)+1/2O2(g)===H2O(l) △H1 2H2(g)+O2(g)===2H2O(l) △H2
④CaCO3(s)==CaO(s)+CO2(g)△H1 CaO(s)+H2O(l)==Ca(OH)2(s) △H2
A.① B.④ C.②③④ D.①②③
8.若室温时pH=a的氨水与pH=b的稀盐酸等体积混合。恰好完全反应,则该氨水电离出OH-的物质的量浓度与原氨水物质的量浓度之比为( )
A.10 a+b-14 B.10 a+b-12 C. 1012-a-b D.1014-a-b
7.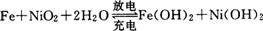 铁一镍蓄电池充电放电时发生的反应为:
铁一镍蓄电池充电放电时发生的反应为:
关于此蓄电池的下列说法中不正确的是
A.放电时Fe为负极
B.充电时阴极的电极反应式为:Ni(OH)2-2e-==Ni02+2H+
C.放电时Ni02的反应为:NiO2+2e-+2H20==Ni(OH)2+20H-
D.蓄电池的电极必须浸在碱性电解质溶液中
6.对于难溶盐MX,其饱和溶液中M+和X-的物质的量浓度之间的关系类似于水的离子积常数C(H+)·C(OH-)=KW,存在等式C(M+)·C(X-)=KSP 一定温度下,将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是( )
①20 mL O.01 mol·L-1 KCl溶液 ②30 mL O.02 moI·L-1 CaCl2溶液
③40 mL O.03 mol·L-1 HCl溶液 ④lO mL蒸馏水
⑤50 mL O.05 mol·L-1 AgN03溶液
A.①>②>③>④>⑤ B.④>①>③>②>⑤
C.⑤>④>②>①>③ D.④>③>⑤>②>①
5.在Na2C03溶液中,下列关系式错误的是 ( )
A.C(Na+)+C(H+)=C(C032一)+C(HC03一)+C(0H一)
B.C(Na+)=2C(C032一)+2C(HCO3一)+2C(H2C03)
C.C(0H一)=C(H+)+C(HCO3一)+2C(H2C03)
D.C(C032一)>C(0H一)>C(HC03一)
4.下列溶液加水稀释,溶液中每种离子的浓度都不会增加的是( )
A.CH3COOH溶液 B.NaCl溶液 C.NaOH溶液 D.FeCl3溶液
3.将金属a放入b(N03)2溶液中发生如下反应:a+b2+==a2++b,则下列说法正确的是( )
A.常温下,a或b可以与水发生反应
B.a与b用导线连接插入稀H2SO4中,则形成原电池且b极上有H2放出
C.a与b用导线连接插入b(NO3)2溶液中,一定构成原电池
D.电解a(NO3)2与b(NO3)2的混合液,在阳极先析出b(使用碳作电极)
2.下列说法中正确的是( )
A.能够使甲基橙呈现黄色的溶液一定是碱性溶液 B.绝对不溶解的物质是不存在的
C.凡需加热的反应一定是吸热反应 D.水解反应是放热反应
1.金属防护的方法错误的是 ( )
A.对健身器材涂油漆以防止生锈 B.将炊具制成铁铜合金而不用纯铁制品
C.用牺牲锌块的方法来保护船身 D.自行车的钢圈上镀上一层铬防锈
25. (8分)某同学用铅蓄电池作电源,用石墨做电极电解500 mL某浓度的CuSO4溶液,观察到A电极表面有红色固体物质生成,当溶液中原有溶质完全电解后,停止通电,取出A电极,洗涤、干燥、称量,电极增重1.6 g。已知铅蓄电池的工作原理为:
(8分)某同学用铅蓄电池作电源,用石墨做电极电解500 mL某浓度的CuSO4溶液,观察到A电极表面有红色固体物质生成,当溶液中原有溶质完全电解后,停止通电,取出A电极,洗涤、干燥、称量,电极增重1.6 g。已知铅蓄电池的工作原理为:
Pb+PbO2+2H2SO4 2PbSO4+2H2O
请按要求回答下列问题:
(1)电解CuSO4溶液的化学方程式 ,
(2)当反应过程中转移的电子为0.02mol时,铅蓄电池内消耗硫酸的物质的量为 mol。
(3)电解前CuSO4溶液的物质的量浓度为 。
(4)若电解前后溶液的体积不变,电解后溶液的pH=
(5)写出铅蓄电池负极的电极反应式:
附加题(10分)(5、6、7、8、9、10班同学必做,其他班同学选做)
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
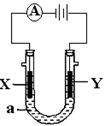 (1)若X、Y都是惰性电极,a是AgNO3溶液,实验开始时,同时在两边各滴入几滴石蕊试液,则
(1)若X、Y都是惰性电极,a是AgNO3溶液,实验开始时,同时在两边各滴入几滴石蕊试液,则
①电解池中X极上的电极反应式为 ,
②Y电极上的电极反应式为 ,
在Y极附近观察到的现象是 。
③电解总反应方程式为 。
(2)要在铁件的表面镀铜防止铁被腐蚀,则:
① Y电极的材料是 ,电极反应式是 。
电解液a选用 溶液。电解过程中其浓度 (增大、减小或不变)
② 若电镀前X、Y两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为______mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com