
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
7.вбжЊЯТСаШ§ИіШШЛЏбЇЗНГЬЪН:
ЂйЁЁЁЁ C(s)+H2O(g)== CO(g)+H2(g)ЃЛІЄHЃН+131.5KJЁЄmol-
Ђк H2(g)+Cl(g)== 2HCl(g)ЃЛІЄHЃН-92.3KJЁЄmol-
Ђл H2(g)+1/2O2(g)ЃНH2O(g)ЃЛІЄHЃНЈC241.8kJЁЄmolЃ1
дђЩЯЪіШ§ИіЗДгІЕФЗДгІШШДѓаЁЙиЯЕе§ШЗЕФЪЧЃК(ЁЁЁЁ )
A.Ђй ЁЕЂк ЁЕЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B. Ђл ЁЕЂк ЁЕЂй
C. Ђл ЁЕЂй ЁЕЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D. Ђй ЁЕЂл ЁЕЂк
6.НёгаШчЯТШ§ИіШШЛЏбЇЗНГЬЪНЃК
ЁЁH2(g)+1/2O2(g)ЃН2H2O(g)ЃЛІЄHЃНaKJЁЄmolЃ1,
H2(g)+1/2O2(g)ЃНH2O(l)ЃЛІЄH== bkJЁЄmolЃ1ЃЌ
2H2(g)+O2(g)ЃН2H2O(l)ЃЛІЄH== ckJЁЄmolЃ1ЃЌ
ЙигкЫќУЧЕФЯТСаБэЪіе§ШЗЕФЪЧ(ЁЁЁЁ )
A.ЫќУЧЖМЪЧЮќШШЗДгІ
ЁЁB.aЁЂbКЭcОљЮЊе§жЕ
ЁЁC.a== bЁЁ
ЁЁD.2b== c
5.егЦјЪЧвЛжжФмдДЃЌЫќЕФжївЊГЩЗжЪЧCH4ЁЃ0.5molCH4ЭъШЋШМЩеЩњГЩCO2КЭвКЬЌЫЎЪБЗХГі445KJЕФШШСПЃЌдђЯТСаШШЛЏбЇЗНГЬЪНжае§ШЗЕФЪЧ(ЁЁ )
A.2CH4(g)+4O2(g)== 2CO2(g)+4H2O(l); ІЄHЃН+890kJЁЄmolЃ1ЁЁ
B. CH4(g)+2O2(g)== CO2(g)+2H2O(l); ІЄHЃН+890kJЁЄmolЃ1ЁЁ
C. CH4(g)+2O2(g)== CO2(g)+2H2O(l); ІЄHЃНЈC890kJЁЄmolЃ1ЁЁ
D. 1/2CH4(g)+ O2(g)== 1/2CO2(g)+ H2O(l); ІЄHЃНЈC890kJЁЄmolЃ1ЁЁ
4.ЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁ )
A.ашвЊМгШШВХФмЗЂЩњЕФЗДгІвЛЖЈЪЧЮќШШЗДгІЁЃ
B.ШЮКЮЗХШШЗДгІдкГЃЮТЬѕМўЯТвЛЖЈФмздЗЂНјааЁЃ
C.ЗДгІЮяКЭЩњГЩЮяЫљОпгаЕФзмьЪОіЖЈСЫЗДгІЪЧЗХШШЛЙЪЧЮќШШЁЃ
D.ЮќШШЗДгІдквЛЖЈЬѕМўЯТ(ШчГЃЮТЁЂМгШШЕШ)вВФмЗЂЩњЗДгІЁЃ
3.ЯТСаЮяжЪМгШыЫЎжаЃЌЯджјЗХШШЕФЪЧ(ЁЁЁЁ )
A.ЩњЪЏЛвЁЁ B.ЙЬЬхNaOHЁЁ C.ЮоЫЎввДМЁЁ D.ЙЬЬхNH4NO3
2.ШШЛЏбЇЗНГЬЪНжаЛЏбЇЪНЧАЕФЛЏбЇМЦСПЪ§БэЪО(ЁЁ )
A.ЗжзгИіЪ§ЁЁ B.дзгИіЪ§ЁЁЁЁ C.ЮяжЪЕФжЪСПЁЁЁЁ D.ЮяжЪЕФСП
1ЃЎЯТСаЫЕЗЈжаЃЌе§ШЗЕФЪЧ(ЁЁЁЁ )
A.дкЛЏбЇЗДгІжаЃЌЗЂЩњЮяжЪБфЛЏЕФЭЌЪБВЛвЛЖЈЗЂЩњФмСПБфЛЏЁЃ
B.ІЄH ЁЕ0БэЪОЗХШШЗДгІЃЌІЄHЁД0БэЪОЮќШШЗДгІ
C.ІЄHЕФДѓаЁгыШШЛЏбЇЗНГЬЪНжаЕФМЦСПЪ§ЮоЙиЁЃ
D.ЗДгІВњЮяЕФзмьЪДѓгкЗДгІЮяЕФзмьЪЪБЃЌІЄH ЁЕ0.
17.ЧІаюЕчГиЪЧЕфаЭЕФПЩГфаЭЕчГиЃЌЫќЕФе§ИКМЋИёАхЪЧЖшадВФСЯЃЌЕчГизмЗДгІЪНЮЊЃК
Pb+PbO2+4H++2SO2-4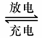 2PbSO4+2H2O
2PbSO4+2H2O
ЧыЛиД№ЯТСаЮЪЬт(ВЛПМТЧЧтЁЂбѕЕФбѕЛЏЛЙд):
(1)ЁЁЁЁЁЁ ЗХЕчЪБЃКе§МЋЕФЕчМЋЗДгІЪНЪЧ______________;ЕчНтвКжаH2SO4ЕФХЈЖШНЋБф________;ЕБЭтЕчТЗЭЈЙ§1 molЕчзгЪБЃЌРэТлЩЯИКМЋАхЕФжЪСПдіМг________gЁЃ
(2)ЁЁЁЁЁЁ дкЭъШЋЗХЕчКФОЁPbO2КЭPbЪБЃЌШєАДгвЭМСЌНгЃЌЕчНтвЛЖЮЪБМфКѓЃЌдђдкAЕчМЋЩЯЩњГЩ__________ЁЂBЕчМЋЩЯЩњГЩ________,ДЫЪБЧІаюЕчГиЕФе§ИКМЋЕФМЋадНЋ________________________ЁЃ
16. ЛЏбЇЕчГидкЭЈбЖЁЂНЛЭЈМАШеГЃЩњЛюжагазХЙуЗКЕФгІгУЃЌФПЧАГЃгУЕФФј(Ni)яг
ЛЏбЇЕчГидкЭЈбЖЁЂНЛЭЈМАШеГЃЩњЛюжагазХЙуЗКЕФгІгУЃЌФПЧАГЃгУЕФФј(Ni)яг
ЁЁ (Cd)ЕчГиЃЌЦфЕчГизмЗДгІПЩЪОЮЊЃК
ЁЁ
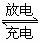
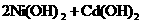
ЁЁ (1)ЯТСагаЙиФјягЕчГизмЗДгІЕФЫЕЗЈжаЃЌе§ШЗЕФЪЧ________(ЬюађКХ)ЃЛ
ЁЁЁЁЁЁ ЂйвдЩЯЗДгІЪЧПЩФцЗДгІЁЁЁЁЁЁЁЁЁЁЁЁ ЂквдЩЯЗДгІВЛЪЧПЩФцЗДгІ
ЁЁЁЁЁЁ ЂлГфЕчЪБЛЏбЇФмзЊБфЮЊЕчФмЁЁЁЁЁЁЁЁ ЂмЗХЕчЪБЛЏбЇФмзЊБфЮЊЕчФм
ЁЁ (2)вбжЊ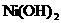 КЭ
КЭ ОљФбШмгкЫЎЃЎгазЪСЯБэУїЃЌвЛНкЗЯФјягЕчГиПЩвдЪЙвЛЦН
ОљФбШмгкЫЎЃЎгазЪСЯБэУїЃЌвЛНкЗЯФјягЕчГиПЩвдЪЙвЛЦН
ЗНУзУцЛ§ЕФИћЕиЪЇШЅЪЙгУМлжЕЃЌдкЫсадЭСШРжаетжжЮлШОгШЮЊбЯжиЃЎетЪЧвђЮЊ_ЁЁ __
_____________________________________ЃЛ
ЁЁ(3)СэвЛжжГЃгУЕФЕчГиЪЧяЎЕчГи(яЎЪЧвЛжжМюН№ЪєдЊЫиЃЌЦфЯрЖддзгжЪСПЮЊ7)ЃЌгЩгкЫќЕФБШШнСП(ЕЅЮЛжЪСПЕчМЋВФСЯЫљФмзЊЛЛЕФЕчСП)ЬиБ№ДѓЖјЙуЗКгІгУгкаФдрЦ№ВЋЦїЃЌвЛАуЪЙгУЪБМфПЩГЄДяЪЎФъЃЎЕчГизмЗДгІПЩБэЪОЮЊЃК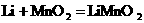 ЃЎЪдЛиД№ЃКЂйяЎЕчГиБШШнСПЬиБ№ДѓЕФдвђЪЧ_______________________________________ЃЛ
ЃЎЪдЛиД№ЃКЂйяЎЕчГиБШШнСПЬиБ№ДѓЕФдвђЪЧ_______________________________________ЃЛ
ЁЁЂкяЎЕчГижаЕФЕчНтжЪШмвКашгУЗЧЫЎШмМСХфжЦЃЌЮЊЪВУДетжжЕчГиВЛФмЪЙгУЕчНтжЪЕФЫЎШмвК?ЧыгУЛЏбЇЗНГЬЪНБэЪОЦфдвђ_______________________________________ЃЎ
15.ЛЏбЇПЮЩЯЃЌЛЏбЇбаОПаЁзщЕФЭЌбЇНЋвЛПщЭЦЌКЭвЛПщаПЦЌВхШыЮїКьЪСЃЌзіГЩЮїКьЪСЕчГиЃЌИУзщЭЌбЇЯыЬНОПЮїКьЪСЕчГиЕФЕчбЙДѓаЁгыФФаЉвђЫигаЙиЃЌаЁзщГіЯжСЫСНжжЙлЕуЃКвЛжжШЯЮЊгыСНН№ЪєжЎМфЕФОрРыгаЙиЃЌСэвЛзщШЯЮЊгыН№ЪєЦЌВхШыЮїКьЪСЕФЩюЖШгаЙиЁЃЮЊСЫбщжЄВТЯыЪЧЗёе§ШЗЃЌЫћУЧевРДЕчбЙБэЃЌНЋЭЦЌКЭаПЦЌЕФвЛЖЫЖдГЦВхШыЮїКьЪСЕФЙћШтФкЃЌСэвЛЖЫНгЩЯЕМЯпгыЕчбЙБэЯрСЌЙЙГЩБеКЯЛиТЗЁЃ
(1)ЧыФубЁдёЦфжавЛжжВТЯыЃЌВЂЬсГібщжЄЕФЗНЗЈЃК
(2)ФПЧАШЫУЧТвШгЕчГиЕФЯжЯѓЗЧГЃЦеБщЃЌЧыФуИјгаЙиВПУХЬсИіНЈвщЃК_________
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com