
题目列表(包括答案和解析)
2. 知CH4(g)+2O2(g)== CO2(g)+2H2O(l); ΔH=–Q1kJ·mol-1 ,
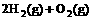 =2H2O(g);△H2=–Q2 kJ·
=2H2O(g);△H2=–Q2 kJ· ,
,
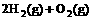 =2H2O(l);△H2=–Q3 kJ·
=2H2O(l);△H2=–Q3 kJ· 。
。
常温下,取体积比4∶1的甲烷和氢气的混合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为( )
A.0.4Q1+0.05Q3 B. 0.4Q1+0.05Q2
C. 0.4Q1+0.1Q3 D. 0.4Q1+0.2Q2
1.已知
(l)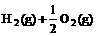 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·
(2)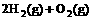 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·
(3)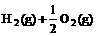 =H2O(l) △H3=c kJ·
=H2O(l) △H3=c kJ·
(4)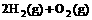 =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·
下列关系式中正确的是( )
A. a<c <0 B.b>d>0 C.2a=b<0 D.2c=d>0
15.已知下列热化学方程式:
C(s)+ O2(g)== CO2(g);△H=–393.5kJ·mol-1
CO(g)+1/2 O2(g)== CO2(g);△H=–283.0kJ·mol-1
计算1mol固态碳粉燃烧生成CO(g)放出的热量,并写出相应的热化学方程式。
拓展提高
14.已知:
C2H6O(g)+3O2(g) 2CO2(g)+3H2O (g); △H1
2CO2(g)+3H2O (g); △H1
H2O(g)== H2O(l) ;△H2
C2H6O(g)== C2H6O(l);△H3
若使23g C2H6O(l)完全燃烧生成液态水,则放出的热量为__________________。(用含△H1、△H2、△H3的式子表示)
13.将0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5KJ热量。请写出反应的热化学方程式__________________________________.
12.已知在25℃,101kPa下,lgC8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是( )
A C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(g) △H=–48.40kJ·mol-1
B C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1) △H=–5518kJ·mol-1
C C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1) △H=+5518kJ·mol-1
D C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1) △H=–48.40kJ·mol-1
11.下列反应既属于氧化还原反应,又是吸热反应的是( )
A.铝片与稀盐酸反应
B.灼热的碳与CO2反应
C.Ba(OH)2·8H2O与NH4Cl反应
D.甲烷在氧气中的燃烧反应
10.酒精燃烧的化学方程式为:C2H6O+3O2 2CO2+3H2O,完全燃烧一定量的无水酒精,放出的热量Q,为完全吸收生成的CO2,消耗8mol·L-1的NaOH溶液50mL时恰好生成正盐。则燃烧1mol无水酒精所放出的热量为( )
2CO2+3H2O,完全燃烧一定量的无水酒精,放出的热量Q,为完全吸收生成的CO2,消耗8mol·L-1的NaOH溶液50mL时恰好生成正盐。则燃烧1mol无水酒精所放出的热量为( )
A.0.2Q B.0.1Q C.5Q D.10Q
9.同温同压下,下列各热化学方程式中热量数值最小的是( )
A.2A(l)+B(l)== 2C(g);ΔH=+Q1
B. 2A(g)+B(g)== 2C(g);ΔH=+Q2
C. 2A(g)+B(g)== 2C(l);ΔH=+Q3
D. 2A(l)+B(l)== 2C(l);ΔH=+Q4
8.1gH2燃烧生成液态水放出142.9KJ的热量,表示该反应的热化学方程式正确的是( )
A. 2H2(g)+O2(g)=2H2O(l) ; ΔH=–142.9kJ·mol-1
B. 2H2(g)+O2(g)=2H2O(l) ; ΔH=–571.6kJ·mol-1
C. 2H2+O2=2H2O ; ΔH=-571.6kJ·mol-1
D. H2(g)+1/2O2(g)=H2O(g) ; ΔH= –285.8kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com