
题目列表(包括答案和解析)
8.已知:
(l)H2(g)+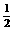 O2(g)=H2O(g)
△H1=a k
O2(g)=H2O(g)
△H1=a k J·
J·
(2)2H2(g)+ O2(g)=2H2O(g)
△H2=b kJ·
(3)H2(g)+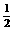 O2(
O2( g)=H2O(l)
△H3=c kJ·
g)=H2O(l)
△H3=c kJ·
(4)2H2(g)+ O2(g)=2H2O(l)
△H4=d kJ·
下列关系式中正确的是
A. a<c <0 B.b>d>0 C.2a=b<0 D.2c=d>0
7.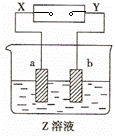 如图所示,X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色、无味气体放出。符合这一情况的是表中的
如图所示,X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色、无味气体放出。符合这一情况的是表中的
|
|
a极板 |
b极板 |
X电极 |
Z溶液 |
|
A |
锌 |
石墨 |
负极 |
CuSO4 |
B |
石墨 |
石墨 |
负极 |
NaOH |
|
C |
银 |
铁 |
正极 |
AgNO3 |
|
D |
铜 |
石墨 |
负极 |
 CuCl2 CuCl2 |
6.已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”。关于标有“+”的接线柱,下列说法中正确的是
A.充电时作阳极,放电时作负极 B.充电时作阳极,放电时作正极
C.充电时作阴极,放电时作负极 D.充电时作阴极,放电时作正极
5.用石墨作电极,电解1 mol/L下列物质的溶液,溶液的pH保持不变的是
A.HCl B.NaOH C.Na2SO4 D.NaCl
4.下列热化学方程式书写正确的是
A.C(s) + O2(g) == CO2(g) △H= +393.5kJ/mol
B.2SO2 + O2 == 2SO3 △H=-196.6kJ/mol
C.H2(g) + 1/2O2(g) == H2O(l) △H=-285.8kJ/mol
D.2H2(g) + O2(g) == 2H2O(l) △H=-571.6KJ
3.反应N2+3H2 2NH3刚开始时,N2的浓度为3 mol/L,H2的浓度为5 mol/L,3 min后测得NH3浓度为0.6 mol/L,则此时间内,下列反应速率表示正确的是
2NH3刚开始时,N2的浓度为3 mol/L,H2的浓度为5 mol/L,3 min后测得NH3浓度为0.6 mol/L,则此时间内,下列反应速率表示正确的是
A.v(NH3)=0.2
mol/( L·s) B.v(N2)=1.0 mol/(L·min)
L·s) B.v(N2)=1.0 mol/(L·min)
C.v(H2)=1.67 mol/(L·min) D.v(H2)=0.3 mol/(L·min)
2.下列说法正确的是
A.废旧电池应集中回收,并填埋处理
B.充电电池放电时,电能转变为化学能
C.放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关
D.所有燃烧反应都是放热反应,所以不需吸收能量就可以进行
1.为了建设环境友好型社会,节能减排将成为我国政府目前工作的重点,因此节约能源与建设新能源是摆在当前的一个课题。针对这一现象,某化学学习研究性小组提出如下方案,你认为不够科学合理的是
A.采用电解水法制取氢气作为新能源
B.加大开发太阳能、水能、风能、地热能等能源力度,减少化石燃料的使用
C.研制推广以乙醇为燃料的汽车
D.生产、生活中,努力实现资源的循环利用
23.自由基又称游离基,是含有未配对电子的原子、分子或基团。大多数自由基很不稳定,只能作为活性中间体瞬间存在,寿命很短,如丁烷受热分解产生三种活性很高的自由基:
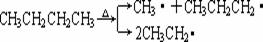
活泼自由基可诱发自由基起加成反应、加聚反应、取代反应、氧化还原反应。这些反应在有机工业、石油化工和高分子工业等方面得到广泛应用。
(1)写出自由基CH3CH2·的电子式 ;若CH3CH2·失去一个电子,则称为碳正离子,该碳正离子的电子式为 。
(2)自由基反应一般是在光和热条件下进行,如烷烃与氯气的取代为自由基取代。已知烷烃中碳原子上的氢原子越少,所形成的自由基越稳定,试完成下列方程式:
CH3-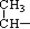 CH3+Cl2
CH3+Cl2 (主要产物)+HCl
(主要产物)+HCl
(3)不对称烯烃在过氧化物存在下,与HBr发生游离基加成反应,其反应历程是:
R-CH=CH2+Br·→R-CH-CH2Br R-CH-CH2Br+HBr→R-CH2-CH2Br+Br·
试分两步将(CH3)2CHCH=CH2转变为(CH3)2CHCH2CH2OH的反应方程式。
(4)有机物中共价键断裂时,若成键的一对电子平均分给两个原子或原子团,则形成自由基;若成键电子全分给某原子或原子团,则形成碳正离子。
①已知CH3+ 四个原子共平面,键 角相等,
角相等, 键角应是
。
键角应是
。
②(CH3)3C+ 和NaOH水溶液反应生成电中性有机分子,该分子结构简式 ,此物质能否发生消去反应 。
余姚中学第一学期高二周六第一次化学
22.2001年诺贝尔化学奖被美国的诺尔斯、夏普雷斯和日本的野依良治获得,他们发现了
某些手性分子可用作某些化学反应的催化剂,为合成对人类有用的重要化学物开辟了一个
全新的研究领域。在有机物分子中,若某个碳原子连接4个不同的原子或基团,则这种碳
原子称为“手性碳原子”,如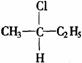 。
。
若同一个碳原子上连着2个碳碳双键(如C=C=C)时,分子极不稳定,不存在。某链烃分子式为C7H10的众多同分异构体中:
(1)处于同一平面上的碳原子数最多有 个。
(2)含有“手性碳原子”,且与足量H2发生加成反应后仍具有“手性碳原子”的有多种。它们的结构简式除2种外,再写出3种
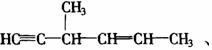
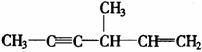
、 、 。
(3)含有“手性碳原子”,但与足量H2发生加成反应后,不具有“手性碳原子”的结构简式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com