
题目列表(包括答案和解析)
11.向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是( )。
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+
C.用硝酸铜溶液代替硫酸铜溶液进行实验,不能观察到同样现象
D.在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道
10.用价层电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是( )
A.直线形;三角锥形 B V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
9.下列分子中,中心原子以sp杂化轨道成键的是( )
A.NH3 B.BF3 C.BeCl2 D.H2O
8.已知X、Y两元素同周期,且电负性X>Y。下列说法正确的是
A、最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性
B、在元素周期表中X位于Y的左面
C、Y的气态氢化物的稳定性大于X的气态氢化物的稳定性
D、X与Y形成的化合物中,X显负价,Y显正价
7.下列规律中,明显属于经验规律的是
A、质量守恒定律 B、元素周期律
C、相似相溶原理 D、能量最低原理
6.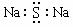 下列各项表达式正确的是
下列各项表达式正确的是
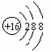
A.S2―的结构示意图: B.Na2S的电子式:
C.基态碳原子的电子排布式:ls22s12p3 D.N2的结构式::N≡N
5.下列性质中,可以证明某化合物内一定存在离子键的是( )。
A.可溶于水 B.具有较高的熔点
 C.水溶液能导电 D.熔融状态下能导电
C.水溶液能导电 D.熔融状态下能导电
4.下列叙述正确的是( )
A.2s轨道可以和3p轨道形成sp2杂化轨道
B.烯烃中的碳碳双键由l个σ键和l个π键组成
C.由极性键组成的分子,一定是极性分子
D.甲烷中心原子sp3杂化轨道有一个由孤电子对占据
3.在基态多电子原子中,关于核外电子能量的叙述错误的是( )
A.最易失去的电子能量最高 B.电离能最小的电子能量最高
C.p轨道电子能量一定高于s轨道电子能量
D.在离核最近区域内运动的电子能量最低
2.构造原理揭示的电子排布能级顺序,实质是各能级能量高低的顺序,若以E表示某能级的能量,下列能量高低顺序中正确的是
A、E(3s)>E(2s)>E(1s) B、E(3s)>E(3p)>E(3d)
C、E(4f)>E(4s)>E(3d) D、E(5s)>E(4s)>E(4f)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com