
题目列表(包括答案和解析)
29.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
|
实验编号 |
|
催化剂 |
|
① |
10ml2% H2O2溶液 |
无 |
|
② |
10mL5% H2O2溶液 |
无 |
|
③ |
10mL5% H2O2溶液 |
1mL0.1mol·L-1FeCl3溶液 |
|
④ |
10mL5% H2O2溶液+少量HCl溶液 |
1mL0.1mol·L-1FeCl3溶液 |
|
⑤ |
10mL5% H2O2溶液+少量NaOH溶液 |
1mL0.1mol·L-1FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是_ 。
(2)实验①和②的目的是__________________________________________。实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是 。
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。
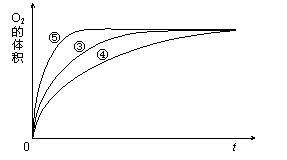

分析上图能够得出的实验结论是 。
台州市2010学年第二学期高二年级六校联考月考化学参考答案及评分标准
28.t℃时,将3molA和1molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:
3A(g)+B(g) 
 xC(g)。2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)。2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x=
(2)从反应开始至达到平衡状态,反应物A的转化率为 ;A的平均反应速率为 。
27.高炉炼铁中发生的基本反应之一如下:
FeO(固)+CO(气)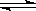 Fe(固)+CO2(气)ΔH>0
Fe(固)+CO2(气)ΔH>0
(1)则该反应中平衡常数K= 。
(2)已知1100℃时K=0.263。1100℃时测得高炉中c(CO2)=0.025mol·L-1,c(CO)=0.1mol·L-1在这种情况下,该反应是否处于平衡状态 (选填是或否),此时化学反应速率是v正 v逆(选填>,<,=)
26.用石墨电极电解100 mL H2SO4与CuSO4的混合溶液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为 mol·L-1。
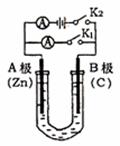
25.如右图所示,U形管内盛有100mL的溶液,按要求回答下列问题。
(1)打开K2 ,合并K1 ,若所盛溶液为CuSO4溶液:则A为 极,A极的电极反应式为  。若所盛溶液为KCl溶液:则B极的电极反应式为
,K+移向 极(填A、B)
。若所盛溶液为KCl溶液:则B极的电极反应式为
,K+移向 极(填A、B)
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则:
①A电极附近可观察到的现象是 。
②B电极的电极反应式为 。
③U形管内总反应化学方程式是 。
(3)如要用电解方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是 ,电极反应式是 。B电极的材料应换成是 ,反应一段时间后电解质溶液中Cu2+浓度 (填“增大”、“减小”、“不变”)。
23.(1)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1 = -1275.6 kJ/mol
 ② 2CO (g
② 2CO (g )+ O2(g) =
2CO2(g) ΔH2 = -566.0 kJ/mol
)+ O2(g) =
2CO2(g) ΔH2 = -566.0 kJ/mol
③  H2O(g) = H2O(l) ΔH3 = -44.0 kJ/mol
H2O(g) = H2O(l) ΔH3 = -44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
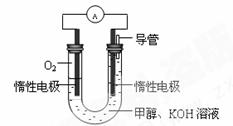
(2)某实验小组依据甲醇燃烧的反应原理,
①设计如图所示的电池装置。该电池负极的电极反应为 。
② 工作一段时间后,测得溶液的pH减小,该电池总反应的离子方
程式为 。
 24.用碳棒作电极,在H+、Na+、Cu2+、Ag+、Cl-、NO3-、SO42-等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
24.用碳棒作电极,在H+、Na+、Cu2+、Ag+、Cl-、NO3-、SO42-等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
⑴当阴极放出H2,阳极放出O2时,电解质是 ;
⑵当阴极析出金属,阳极放出O2时,电解质是 ;
⑶当阴极放出H2,阳极放出Cl2时,电解质是 ;
22.一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应: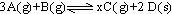 。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是
。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是
A.该条件下此反应的化学平衡常数约为0.91(L/mol)3
B.A的平均反应速率为0.3mol/(L s)
s)
C.B的转化率为60%
D.若混合气体的密度不再改变时,该反应不一定达到平衡状态
21. 某新型可充电电池,能长时间保持稳定的放电电压。该电池的总反应为:
|
|||
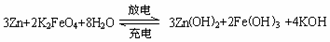 |
|||


 A.放电时负极反应为:Zn-2e–+2OH–=Zn(OH)2
B.放电时正极反应为:
A.放电时负极反应为:Zn-2e–+2OH–=Zn(OH)2
B.放电时正极反应为: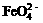 +4H2O+3e–=Fe(OH)3+5OH–
C.充电时阳极附近溶液的碱性减弱
D.放电时每转移3 mol电子,正极有1 molK2FeO4被氧化
+4H2O+3e–=Fe(OH)3+5OH–
C.充电时阳极附近溶液的碱性减弱
D.放电时每转移3 mol电子,正极有1 molK2FeO4被氧化
20.用惰性电极电解一定质量的某浓度的NaCl溶液,一段时间后停止电解。此时若加入100g36.5%的浓盐酸,所得溶液正好与原溶液完全相同,则下列说法正确的是
A .电解过程中,两极所得到的气体,在相同的条件下体积相等
.电解过程中,两极所得到的气体,在相同的条件下体积相等
B.电解过程中,在相同的条件下,阳极所得到的气体的体积比阴极的大
C.原某浓度的NaCl溶液中溶有117gNaCl
D.电解过程中转移电子的物 质的量约为8mol
质的量约为8mol
19.用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,
 如右图所示。则下列说法正确的是
如右图所示。则下列说法正确的是
A.构成原电池时b极反应为: Cu﹣2e-=Cu2+
B.构成电解池时a极质量一定减少
C.构成电解池时b 极质量可能减少也可能增加
D.构成的原电池或电解池工作后就可能产生大量气体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com