
4.可能用到的相对原子质量:H-1、C-12、O-16、Na-23、Br-80
第Ⅰ卷(选择题)
3.请将各卷答案填写在答题卷上。
2.答题前,考生务必将密封线内的项目填写清楚。
29.(15分)某化学兴趣小组欲设计使用如下装置验证:
铜和一定量的浓硝酸反应有一氧化氮产生。(假设气体体积均为标准状况,导气管中气体体积忽略不计,且忽略反应中的溶液体积变化)
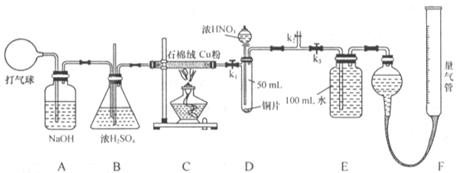
试回答下列问题:
(1)将铜粉分散在石棉绒中的原因是___________________________________。
(2)在铜和浓硝酸反应前,挤压打气球,经A、B、C反应后,进入D中的气体是______
(填化学式),通入该气体的目的是_________________________________;
进行此步操作时应关闭_________,打开_________ (填k1、k2或k3)。
(3)若C装置的硬质玻璃管中出现堵塞,则B中可能出现的现象是________________
________________________________;
(4)关闭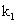 、
、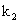 ,打开
,打开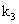 ,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入
,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入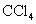 至满。则D中一定发生反应的离子方程式为:
至满。则D中一定发生反应的离子方程式为:
______________________________________________________________。
(5)若E中出现倒吸,可采取的应急操作是_________________________________。
(6)I.从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000 mol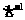 的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则E容器中所得硝酸的物质的量浓度为__________________mol·L
的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则E容器中所得硝酸的物质的量浓度为__________________mol·L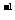 。
。
Ⅱ.若实验测得F装置所收集到的气体体积为139.00 mL,则铜和一定量的浓硝酸反应_________________(填“有”或“无”)NO生成,其依据是(请用数据和文字说明)______________________________________________________
28.(16分)已知①-④均为工业生产及应用的常见反应。其中常温下B、D、J、P气体,
E为分子中原子个数比为1:l的液体。A的相对分子质量为120。(个别反应的产物已略去)
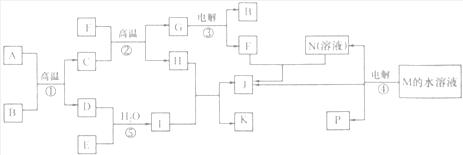
试回答下列问题:
(1)A的化学式为_____________ ;工业上反应①所用的设备名称是_____________。
(2)反应②的实验中,还需用到的药品是_____________、_____________。
(3)反应④的化学方程式为_____________;
该反应装置中使用阳离子交换膜的作用是_____________________________。
(4)P与N反应的产物之一能和K的溶液发生反应,有红褐色沉淀生成。写出该产物与K以物质的量按1:2反应的离子方程式:__________________________。
(5)硫酰氯(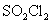 )是制造药物、染料、表面活性剂的主要原料。可由下列反应制取:
)是制造药物、染料、表面活性剂的主要原料。可由下列反应制取:
D(g)+P(g)  SO2Cl2(1);△H<0
SO2Cl2(1);△H<0
某学习小组认为,工业上为提高反应速率和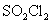 的产率,可采取下列两种方法:
的产率,可采取下列两种方法:
Ⅰ.不断移走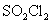
Ⅱ.采用高温
请你就生产实际对上述两种方案进行简要评价,说明是否合理及原因。
27.(16分)有机物A由C、H、O、Cl四种元素组成,其相对分子质量为198.5,Cl在侧链上。当A与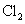 分别在Fe作催化剂和光照条件下以物质的量之比为l:1反应时,分别是苯环上一氯取代有两种和侧链上一氯取代有一种;A与
分别在Fe作催化剂和光照条件下以物质的量之比为l:1反应时,分别是苯环上一氯取代有两种和侧链上一氯取代有一种;A与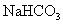 溶液反应时有气体放出。A经下列反应可逐步生成B-G。
溶液反应时有气体放出。A经下列反应可逐步生成B-G。
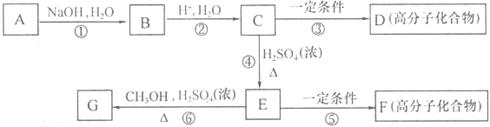
(1)A的化学式为______________;D的结构简式为______________;
(2)上述反应中属于取代反应的是______________ (填编号);
(3)C中含氧官能团的名称为______________、______________;
(4)E的同分异构体中,满足①苯环上只有一个侧链,且侧链上含有一个一CH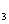 ;②能发生银镜反应;③属于酯类。则其结构简式为(写3种):_________、_______、__________
;②能发生银镜反应;③属于酯类。则其结构简式为(写3种):_________、_______、__________
(5)写化学方程式(有机物写结构简式):
A与NaOH的醇溶液共热:_____________________________________________;
E在一定条件下生成F:__________________________________________________。
26.(13分)A、B、C、D、E五种短周期元素,原子序数依次增大。A与B、C分别构成电子数相等的化合物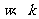 ,且
,且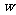 是一种能产生温室效应的气体;D元素最外层电子数是次外层电子数的3倍;A、B、C、D可形成化合物;A、D、E可形成化合物y;A、C、D可形成化合物z。
是一种能产生温室效应的气体;D元素最外层电子数是次外层电子数的3倍;A、B、C、D可形成化合物;A、D、E可形成化合物y;A、C、D可形成化合物z。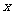 、
、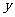 、
、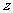 均为阳离子和阴离子个数比是1:l的离子化合物。回答下列问题:
均为阳离子和阴离子个数比是1:l的离子化合物。回答下列问题:
(1)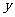 的电子式为_________;
的电子式为_________;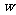 属于__________(填“极性”或“非极性”)分子;
属于__________(填“极性”或“非极性”)分子;
(2)与E同主族且为第七周期的元素原子序数为___________;
(3)在同主族氢化物的性质递变中,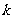 的沸点反常,,这可以用_______来解释(填字母序号);
的沸点反常,,这可以用_______来解释(填字母序号);
A.共价键 B.离子键 C.氢键 D.范德华力
(4)常温下,z与y以物质的量之比1:2反应后所得溶液显 (填“酸”、“碱”或“中”)
性;由产物分析,原因是__________________________________________________、
___________________________________(用离子方程式表示);
(5)由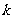 与D的单质、KOH溶液构成原电池,负极会产生
与D的单质、KOH溶液构成原电池,负极会产生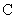 的单质。则其负极反应为
的单质。则其负极反应为
_____________________;一段时间后,溶液pH___________(填“增大”、“减小”或“不变”)。
13.一定条件下,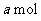 甲烷与足量水蒸气发生如下反应:
甲烷与足量水蒸气发生如下反应: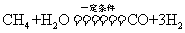 ,
,
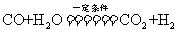 。将生成的
。将生成的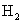 与足量氮气在一定条件下合成氨,其转化率为
与足量氮气在一定条件下合成氨,其转化率为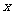 ;再将氨催化氧化后完全转化为
;再将氨催化氧化后完全转化为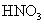 。则所得
。则所得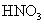 的物质的量为( )
的物质的量为( )
A.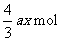 B.
B.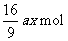 C.
C.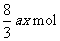 D.
D.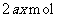
第Ⅱ卷(非选择题,共174分)
12.向甲、乙两个容积均为1L的恒容容器中分别充入2 mol A、2 molB和1 molA、l mol B。
 相同条件下发生如下反应:A(g)+G(g) xC(g);△H<0。测得两容器中
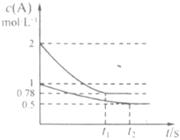
相同条件下发生如下反应:A(g)+G(g) xC(g);△H<0。测得两容器中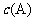 随时间t的变化如图所示。下列说法错误的是
随时间t的变化如图所示。下列说法错误的是 ( )
( )
A.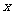 可能等于2也可能等于3
可能等于2也可能等于3
B.若向平衡后的乙容器中充入C,则再次达到平衡时A的体积分数减小
C.单独升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同
D.若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:
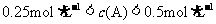
11.某溶液中存在的离子有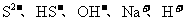 。下列对该溶液的有关叙述正确的是 ( )
。下列对该溶液的有关叙述正确的是 ( )
A.溶液中一定是: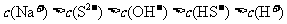
B.组成该溶液的溶质只能是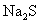 或NaHS或两者的混合物
或NaHS或两者的混合物
C.该溶液只能是碱性或酸性
D.加水稀释,溶液中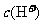 可能增大,也可能减小或不变
可能增大,也可能减小或不变
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com