
5、 化学反应中一定伴随着能量的变化,下列有关能量的说法正确的是
A.等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多
B.由C(石墨)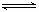 C(金刚石)-1.9KJ可知,金刚石比石墨稳定
C(金刚石)-1.9KJ可知,金刚石比石墨稳定
C.根据热化学方程式:S(s) +
O2(g)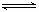 SO2(g) +
297.23 kJ,可推知1 mol
SO2 (g)的能量总和大于1 mo S(s)和1 mol O2(g)的能量总和
SO2(g) +
297.23 kJ,可推知1 mol
SO2 (g)的能量总和大于1 mo S(s)和1 mol O2(g)的能量总和
D.在稀水溶液中 H+(aq)+OH-(aq)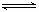 H2O(l)+57.3
kJ,将含0.5 mol
H2SO4的浓硫酸与含l mol NaOH的溶液混合时,放出的热量大于57.3 kJ
H2O(l)+57.3
kJ,将含0.5 mol
H2SO4的浓硫酸与含l mol NaOH的溶液混合时,放出的热量大于57.3 kJ
4、下列关于有机物说法正确的是
A.乙醇、乙烷和乙酸都可以与钠反应生成氢气
B.75%(体积分数)的乙醇溶液常用于医疗消毒
C.苯和乙烯都可以使溴的四氯化碳溶液褪色
D.石油分馏可获得乙酸、苯及其衍生物
3、下列说法不正确的是
A.蛋白质水解的最终产物是氨基酸
B.米饭在嘴中越咀嚼越甜的原因是淀粉水解生成甜味物质
C.油脂、乙醇是人体必需的营养物质
D.水果因含有酯类物质而具有香味
2、结构简式如下图的烷烃分子中的一个氢原子被氯原子取代后,可能形成的一氯代物的种类是
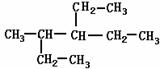
A. 6种 B.7种 C. 8种 D. 9种
1、下列各组化合物中,不论二者以什么比例混合,只要总质量一定,则完全燃烧时消耗O2的质量和生成水的质量不变的是
A.CH4 、C2H6 B.C2H6 、C3H6 C.C2H4 、C3H6 D.C2H4 、C3H4
可能用到的原子量:H 1 C 12 N 14 O 16 S 32 Cl 35.5
Ca 40 Cu 64 Ag 108 Ba 137
26.(6分)在一密闭的2L的容器里充入8mol
SO2和4mol18O2,在一定条件下开始反应:2SO2(g)+O2(g) 2SO3(g),2min末测得容器中有7.2mol
SO2。
2SO3(g),2min末测得容器中有7.2mol
SO2。
试回答:
(1)反应后18O存在哪些物质中____________________________________________;
(2)2min末SO3的浓度;
(3)用O2的浓度变化表示该时间段内的化学反应速率。
25.(14分)某研究性学习小组设计下图装置制取氯气并以氯气为原料进行实验。
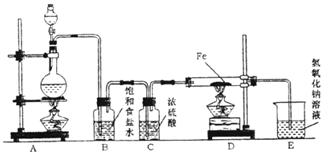
(1)装置A烧瓶中发生反应的化学方程式为___________________________________;
(2)装置B中饱和食盐水的作用是__________________________,装置C中浓硫酸的作用是___________________________________;
(3)实验时,先点燃__________处的酒精灯,再点燃__________处酒精灯,写出D中反应的化学方程式_________________________________________________________________,写出E中反应的离子方程式_____________________________________________________;
(4)若实验中用12mol·L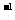 浓盐酸10mL与足量的MnO2反应,生成Cl2的物质的量总是小于0.03mol,试分析可能存在的原因是①_________________________________________,②____________________________________。欲使反应生成Cl2的物质的量最大程度的接近0.03mol,则在装置气密性良好的前提下实验中应采取的措施是______________________
浓盐酸10mL与足量的MnO2反应,生成Cl2的物质的量总是小于0.03mol,试分析可能存在的原因是①_________________________________________,②____________________________________。欲使反应生成Cl2的物质的量最大程度的接近0.03mol,则在装置气密性良好的前提下实验中应采取的措施是______________________
____________________________________________________________________________。
24.(7分)有如下规律可判断元素原子的失电子能力:比较元素的单质与水(或非氧化性酸)反应置换出氢气的难易程度。置换反应越容易发生,元素原子失电子能力越强。某化学活动小组为了验证上述规律设计了以下实验进行探究,请你填写下表有关内容:
|
实验内容 |
实验现象 |
实验结论 |
|
(1)Na、Mg(条)、K与水反应 |
|
同一周期自左而右元素原子失电子的能力逐渐____________; 同一主族自上而下元素原子失电子能力依次______________。 |
|
(2)Mg、Al与酸 反应 |
|
23.(10分)某课外实验小组利用稀硫酸与金属铁反应探究影响化学反应速率的因素,得到如下实验数据:
|
实验 序号 |
铁的 质量/g |
铁的 形态 |
c(H2SO4) /mol·L 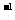 |
V(H2SO4) /mL |
溶液温度/℃ |
金属消失 的时间/s |
|
|
反应前 |
反应后 |
||||||
|
1 |
0.10 |
铁片 |
0.7 |
50 |
20 |
36 |
250 |
|
2 |
0.10 |
铁片 |
0.8 |
50 |
20 |
35 |
200 |
|
3 |
0.10 |
铁粉 |
0.8 |
50 |
20 |
36 |
25 |
|
4 |
0.10 |
铁片 |
1.0 |
50 |
20 |
35 |
125 |
|
5 |
0.10 |
铁片 |
1.0 |
50 |
35 |
50 |
50 |
分析上述数据,回答下列问题:
(1)实验2和3表明,__________________________________对反应速率有影响,影响规律是________________________________;
(2)仅表明反应物浓度对反应速率产生影响的实验有______________(填实验序号);
(3)本实验中影响反应速率的其他因素还有_____________________,能体现该影响因素的实验序号是_____________________;
(4)在实验4中滴入几滴硫酸铜溶液,金属消失的时间小于l25s。
原因是_____________________________________________________________________
____________________________________________;
(5)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,试从反应过程能量的变化角度推测其原因_________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com