
5.元素周期表中全部是金属元素的区域是 ( )
A.d区、ds区、f区 B.s区、d区
C.d区、ds区 D.s区、d区、ds区
4. 下列关于Na2CO3溶液的说法正确的是 ( )
下列关于Na2CO3溶液的说法正确的是 ( )
 A.加入NaOH固体,溶液pH减小 B.稀释溶液,水解平衡常数增大
A.加入NaOH固体,溶液pH减小 B.稀释溶液,水解平衡常数增大
 C.升高温度,
C.升高温度,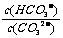 减小 D.通入CO2,水解平衡朝正反应方向移动
减小 D.通入CO2,水解平衡朝正反应方向移动
3.下列能级的能量大小比较,正确的是 ( )
A.E(4s)> E(3d) B.E(6p)> E(5f)
C.E(6s)< E(5p) D.E(4d)< E(5p)
2.有关核外电子运动规律的描述错误的是 ( )
A.核外电子质量很小,在原子核外作高速运动
B.核外电子的运动规律与普通物体不同,不能用牛顿运动定律来解释
C.在电子云示意图中,通常用小黑点来表示电子绕核作高速圆周运动
D.在电子云示意图中,小黑点密表示电子在核外空间单位体积内出现的机会多
1.下图各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是 ( )
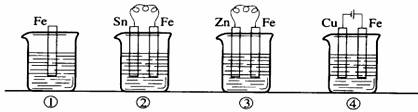
A.④>②>③>① B.②>①>③>④
C.④>②>①>③ D.③>②>④>①
29.(15分)如图装置,浓盐酸与高锰酸钾[KMnO4(s)]不加热就能产生气体单质X,经过A、B两瓶,在C处X与热的白色晶体反应,最后在D瓶内壁有紫黑色晶状物,请回答:
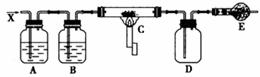
(1)在制取X的反应中,被氧化的盐酸与参与反应的盐酸的物质的量之比为____________。
(2)制取气体X时,需要用到的玻璃仪器有:____________、圆底烧瓶、导管。
(3) 通入C前,要得到纯净的气体X,则A瓶盛有_____________;B瓶盛有____________。
(4) 若C处白色晶体的焰色反应为紫色,且只含有两种元素,则该白色晶体的化学式为______________;D瓶内壁的紫黑色物质可用____________来洗涤。
(5)在C处加热的目的是___________________________________________
(6)E装置中盛有碱石灰,其作用是________________________________
(7)该实验从B以后的装置存在的主要缺点是_____________________________
28.(14分)A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有强氧化性。下述为相关实验步骤和实验现象:
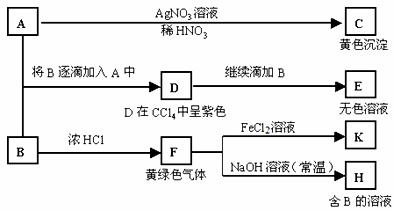
请回答
(1)写出A化学式:
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
, 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
(4)写出由F→H的化学方程式:
2.上述实验装置不够完善,改进方法是 。
1.如何检查装置的气密性: 。
27.(18分)已知①是重要的工业反应,A的焰色反应呈黄色,E中含有两种元素且原子个数比为1∶1。它们之间能实现如下图所示转化(部分产物已略去):
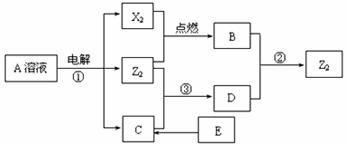
(1)E的电子式是_______________________
(2)1mol气态X2和足量的气态Z2反应时放出184.6KJ的热量,写出该反应的热化学方程式:____________________________________________________________________。
(3)写出反应①的离子方程式是________________________________________________。
(4)写出反应②的离子方程式___________________________________________。
(5)写出E与SO2反应的化学方程式_____________________________________________。
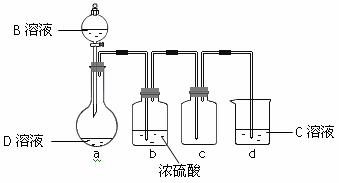
D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,并利用装置C收集Z2,仪器装置下图所示(夹持固定装置的仪器已略去)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com