
9. 某些地区的农民将玉米秸秆粉碎后放在密闭的沼生池内发酵制沼气,发酵后的残余物可做农家肥。沼气的主要成分是甲烷(化学式为CH4),据此化学小组的同学围绕“玉米秸秆主要由哪些元素组成”的问题展开了以下探究活动。
[猜想与假设]根据沼气的成分猜想玉米秸秆中主要含有碳元素、氢元素。
[设计方案进行探究]
|
探究步骤 |
预计现象 |
相关结论 |
|
用坩埚坩夹持一小段烘干的玉米秸秆,点燃后伸入盛有氧气的集气瓶中 |
玉米秸秆剧烈燃烧,火焰熄灭后能够观察到瓶壁上有水珠 |
产物中有______ |
|
向集气瓶中滴入少量____________ |
能够观察到______________ |
产物中有CO2 |
[结论与解释]
⑴将玉米秸秆烘干的目的是:①干燥,使其容易燃烧;②____________________。
⑵根据以上探究,同学们得出结论,秸秆中含有C、H、O三种元素。
[反思与评价]
你认为同学们得出的结论是否正确________,理由是______________________________。
课题2 如何正确书写化学方程式
[考点透视]
8.小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:[提出假设]化学反应中,反应物与生居物的质量 (1) 。
[确定研究方法]分析推理、查阅资料、实验探究。
[设计并进行实验]小刚设计的实验装置和选用药品如A图所示,小洁设计的实装置和选用药品如B图所示,他们在反应前后都进行了规范的操作、准确的称量和细致观察。
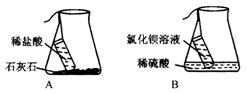 [实验结论]小刚认为:在化学反应中,生成物的总量与反应物的总质量不相等。小洁认为:在化学反应中,生成物的总质量与反应物的总质量不相等。小结认为:在化学反应中,生成物的总质量与反应物的总质量相等。
[实验结论]小刚认为:在化学反应中,生成物的总量与反应物的总质量不相等。小洁认为:在化学反应中,生成物的总质量与反应物的总质量不相等。小结认为:在化学反应中,生成物的总质量与反应物的总质量相等。
你认为 (2) 的结论正确,请谈谈导致另一种结论错误的原因。 (3)
[结论分析]请从原子的角度,简要分析你认为正确的结论。 (4)
[查阅资料]小刚和小洁通过阅资料了解到:法国伟大的科学家拉瓦锡,早在18世纪就围绕这个问题,进行了准确、缜密的研究,并做出了科学结论。
[交流表达]请简要谈一下,你认为这条科学结论有什么重大意义?(不超过30字) (5) 。
[结论]环保部门常用I2O5测定空气受CO污染的程度,发生反应的化学反应方程式为I2O5+5CO═I2+5X根据生成X的多少,可以判断CO的含量,X的化学式是 (6) 。
7.某同学看到方程式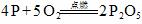 ,即想到以下两点,你能想到更多吗?请把你的想法补充到下面的空格中。
,即想到以下两点,你能想到更多吗?请把你的想法补充到下面的空格中。
(1)磷在氧气中燃烧,同时生成大量的白烟;
(2)反应前后元素的种类不变,都是氧元素和磷元素;(3) ;(4) ;(5) ;(6) ;(7) 。
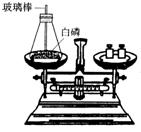
6.如图所示为用加热后的玻璃棒点燃白磷,来测定白磷燃烧前后质量的变化情况,用来验证质量守恒定律的实验。
(1)写出白磷燃烧的化学方程式_____________________________。
(2)白磷在锥形瓶中燃烧时,常常导致瓶塞被冲开,实验失败。导致瓶塞被冲开的原因是_____________________________________。
(3)为了防止瓶塞被冲开,你能将实验作如何的改进?________________。
(4)实验时,用加热后的玻璃棒点燃白磷,你还能找出其他方法点燃瓶内的白磷吗?________________________________________________________。
5.早在17世纪,质量守恒定律被发现之前,英国化学家波义耳曾做过一个实验:在密闭的玻璃容器中燃烧金属,得到了金属灰,然后称量金属灰的质量,发现比原金属质量增加了。
(1)试解释金属灰质量比原金属质量增加的原因。
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量方法,以验证质量守恒定律。
4.在反应中,当1.6g X与Y完全反应后,生成R的质量为4.4g,且反应后生成的R和M的质量之比为11:9,则在此反应中Y和M的质量比是( )
A. 23:9 B. 16:9 C. 32:9 D. 46:9
3.如右图所示,二分子的甲反应生成二分子的乙与一分子的丙,已知甲、乙、丙三者为不
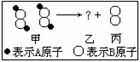 同的纯净物。则从图示中获得的下列信息中错误的是( )
同的纯净物。则从图示中获得的下列信息中错误的是( )
A.分子的种类在化学反应中发生了改变
B.该反应的反应类型为分解反应
C.化学变化中原子的种类没有改变 D.乙分子中含有4个A原子、2个B原子
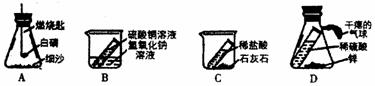
2.下列装置不能用做证明质量守恒定律实验的是( )
1.宣传科学知识,揭露伪科学是我们的义务,下列说法中,属于伪科学的是( )
A.氢气可用作高能燃料 B.以石油为原料可蒸馏出汽油等产品
C.农业上主要施用含氨、磷、钾元素的肥料 D.“气功”能使铜变成金
2.对质量守恒定律的适用范围含糊不清:①必须在化学反应中,如:100g酒精和100g水混合形成200g酒精溶液,并不能用质量守恒定律解释;②在利用质量守恒定律时,一定要注意是参加反应的总质量和生成物的总质量才相等。如:酒精燃烧后,质量逐渐减少,用质量守恒定律来解释的话,参加反应的酒精和氧气的质量总和应该与生成的二氧化碳及水的总质量相等,而二氧化碳和水散失在空气中,无法称得质量,所以质量减少。而铁钉生锈后质量会增加,则是因为参加反应的铁和氧气的质量总和等于生成的铁锈的质量,当然铁锈的质量就会大于原先金属铁的质量。
[基础演练]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com