
2.掌握含一定量杂质(杂质不参加反应)的反应物或生成物的化学方程式计算。
1.掌握由一种反应物(或生成物)的质量求生成物(或反应物)质量的计算。
10.用好化学用语和溶解性表,对日后化学的学习是非常有帮助的。请按要求写出以下反应的化学方程式(所选的反应物在右表的范围内,
|
1) 一种酸和一种碱 ;
2) 一种酸和一种盐 ;
3) 一种碱和一种盐 ;
4) 一种盐和另一种盐 。
课题3 利用化学方程式的简单计算
[考点透视]
9.经过学习我们可以初步认识到:化学反应的快慢、现象、生成物等与反应物量的多少、反应条件有着密切的关系。请各举一例说明:
(1)使用催化剂,能改变化学反应的速率: 。
(2)反应物的量不同,生成物可能不同: 。
(3)反应物的量不同,反应现象可能不同: 。
8.把铁粉和硫粉以适当的质量比均匀混合,堆放在石棉网,然后用烧红的玻璃棒的一端接触混合物。这时部分混合物迅速变成红热状态,移开玻璃棒后,反应继续剧烈进行,全部混合物呈红热状态,冷却后得到黑色的固体化合物--硫化亚铁。
①这一变化的化学方程式是 。
②铁跟硫反应时是吸收热量还是放出热量? 。
③用什么实验可以证实反应中铁已从游离态变成化合态 。
④从理论上计算,为使铁粉和硫粉都能全部反应,两者最佳质量比应是 。
7.在化学反应中,物质所含元素的化合价发生变化的反应就是氧化-还原反应。
例如:2Na +Cl2=2NaCl 反应前后,Na、Cl元素的化合价发生了变化,该反应是氧化-还原反应。(1)根据化合价是否变化分析,下列反应属于氧化-还原反应的是(填序号): 。
A.2Mg + O2 点燃 2MgO B.CaO + H2O= Ca(OH)2 C.2KClO3 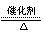 2KCl+3O2
↑
2KCl+3O2
↑
D.CaCO3 高温 CaO + CO2↑ E.H2 + CuO 加热 Cu + H2O F.HCl + NaOH = NaCl +H2O
(2)根据上面的分析和推理,对四种基本反应类型是否属于氧化还原反应,做出恰当概括:
置换反应 ;化合反应 ;
分解反应 ;复分解反应 ;
6.通过学习,我们已经知道了下列反应: ①C+O2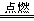 CO2
②2CO+O2
CO2
②2CO+O2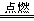 2CO2 ③CH4+2O2
2CO2 ③CH4+2O2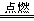 CO2+2H2O ④C2H5OH+3O2
CO2+2H2O ④C2H5OH+3O2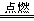 2CO2+3H2O
2CO2+3H2O
通过对上述四个反应的化学方程式的分析,你能总结出哪些规律性的结论?
5.写出下列有关化学方程式:
(1)法医常用马氏试砷法来证明是否为砒霜(As2O3)中毒,其原理是:用锌和盐酸与试样混合在一起,若试样中含有砒霜,则会发生反应,生成砷化氢(AsH3)、氯化锌和水,写出该反应的化学方程式: 。
(2)市售打火机里装的不是汽油,而是液体丁烷(C4H10),丁烷在空气中燃烧后产生二氧化碳和水蒸气,写出丁烷完全燃烧的化学方程式 。(3)二氧化钛(TiO2)是优良的白色颜色。它的生产工艺流程中,有一步反应是用四氯化钛(无色液体)跟空气中的水接触,即产生二氧化钛,并伴有大量酸雾。写出该反应的化学方程式: 。
(4)烧水的铝壶中常结有一层水垢(水垢的主要成分是CaCO3),用适量的稀盐酸可以除去它,反应的化学方程式是 。若盐酸的用量过多,会损坏铝壶,原因是(写化学方程式) 。
4.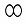
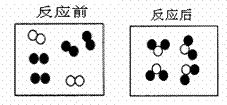
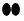 下列图形能形象地表示某化学反应前后反应物、生成物的分子变化,
下列图形能形象地表示某化学反应前后反应物、生成物的分子变化,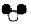 其中“ ”、“ ”、“ ”分别表示三种不同物质的分子。该化学反应的基本类型是( )
其中“ ”、“ ”、“ ”分别表示三种不同物质的分子。该化学反应的基本类型是( )
A.复分解反应 B.分解反应
C.置换反应 D.化合反应
3.科学实验证明,空气中的微量臭氧(O3)可以抵抗阳光中紫外线对人体的危害,空调和冰箱中的致冷剂“氟里昂”是一种氟氯烃(以M代替),它可以破坏臭氧层,其反应过程为:M+ O3 →MO+ O2 MO+O→M+ O2 ,则M在该反应中是( )
 A.氧化剂 B.还原剂 C.催化剂 D.稳定剂
A.氧化剂 B.还原剂 C.催化剂 D.稳定剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com