
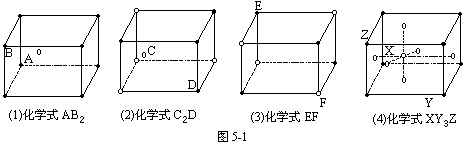
9.根据离子晶体的晶格结构(如图5-1),判断化学式错误的是[ ]
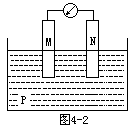
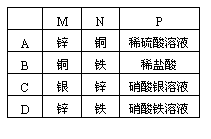
8.如图4-2所示装置中,观察到电流计指针偏转;M棒变粗,N棒变细,由此判断下表中所列M、N、P物质,其中可以成立的是[ ]
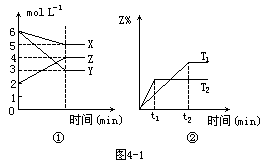
7.符合图4-1的反应是(T1、T2表示不同的温度)[ ]
A.X+3Y 2Z-Q
2Z-Q
B.X+3Y 2Z+Q
2Z+Q
C.X+2Y 3Z+Q
3Z+Q
D.5X+3Y 4Z+Q
4Z+Q
6.常温下pH=2的两种酸溶液A和B,分别加水稀释1000倍,其pH值与所加水的体积变化如图3-1所示。下列结论正确的是 [ ]
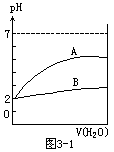
A.酸B比酸A的电离度大
B.A为弱酸,B为强酸
C.酸B的物质的量浓度比A的大
D.A酸比B酸易电离
6.在容积相同的五个密闭容器中分别放人同量的A2和B2,在不同温度下任其发生反应:A2(g)+2B2(g)2 AB2(g),分别在某时刻测得其中AB3所占的体积分数绘成图2-2,不正确的叙述是[ ]
AB2(g),分别在某时刻测得其中AB3所占的体积分数绘成图2-2,不正确的叙述是[ ]
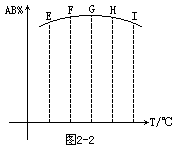
A.反应是放热反应
B.E、F二点尚未达到平衡状态
C.H、I二点尚未达到平衡状态
D.G、H、I三点功能已达平衡状态
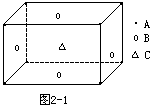
5.某物质的晶体中,含A、B、C三种元素,其排列方式如图2-1所示(其中前后两面心上的B原子不能画出),晶体中A、B、C的原子个数比依次为 [ ]
A.1∶3∶1
B.2∶3∶1
C.2∶2∶1
D.1∶3∶3
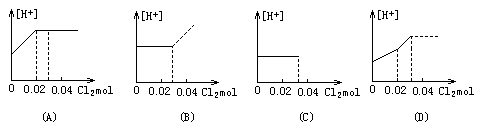
4.将0.03molCl2缓缓通入含0.02mol H2SO3和0.02mol HBr的混合溶液中,在此过程中,溶液的[H+]与Cl2用量的关系示意图是(溶液的体积示为不变)[ ]
3.将物质的量相等的硫酸铝和硫酸铵溶水形成VmL混合溶液,向混合溶液中逐滴加入某氢氧化钠的溶液(其物质的量浓度为混合溶液中两溶质的物质的量浓度之和),直至过量。下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的量(y)的关系示意图中正确的是[ ]
2.常温时,pH=1的两种一元酸溶液A和B,分别加水稀释1000倍,两溶液的pH值与所加水的体积变化如图所示,下列结论中正确的是 [A、D]
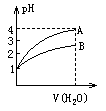
A.B酸比A酸的电离度小
B.B酸比A酸容易电离
C.B是弱酸,A是强酸
D.pH=1时,B酸的物质的量浓度比A酸大
1.下图显示了经济发展与环境质量的关系,根据这种关系,发展中国家应采取的策略是[D]
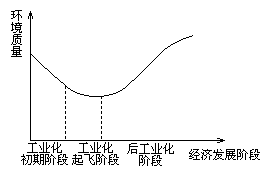
A.环境污染不可避免,只能采取先污染,后治理的策略
B.后工业化阶段环境问题会自然解决
C.保护环境至关重要,必须杜绝兴建大量排污的工业
D.可采取措施减少或避免发展过程中的环境污染
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com