
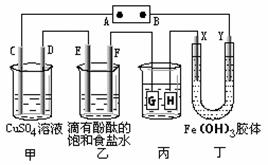
21.(14分)如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
请回答:
(1)B极是电源的 极,一段时间后,甲中溶液颜色 ,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明 ,在电场作用下向Y极移动。
(2)电解一段时间内甲、乙装置中的C、D、E、F电极均分别只有一种单质生成时,对应单质的物质的量之比为 ,乙中发生反应的离子方程式为 ,若要使电解后的甲装置中的溶液恢复到原浓度则需加入一定量的 。(填物质的化学式)
(3)现用丙装置给铜件镀银,则H应该是 (填“镀层金属”或“镀件”),电镀液是 溶液。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为 ,甲中溶液的pH (填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是 。
20.某无色溶液中只可能含有Na+ 、Ba2 +、 Cl一、 Br一、SO32一、SO42一,对该溶液进行下列实验,实验操作和现象如下表:
|
步骤 |
操 作 |
现 象 |
|
(1) |
取少量溶液滴加几滴石蕊试液 |
溶液变蓝 |
|
(2) |
另取少量溶液滴加过量氯水,再加入CCl4振荡,静置 |
上层无色,下层呈橙红色 |
|
(3) |
取(2)上层溶液,加入过量Ba(NO3)2溶液和稀HNO3,过滤 |
有白色沉淀产生 |
|
(4) |
向(3)的滤液中加入过量AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
下列结论正确的是( )
A.可能含有
Cl一、 SO32一、SO42一 B.肯定没有 Ba2 +、Cl一、Br一
C.不能确定 Na+ 、
SO32一、SO42一 D.肯定有含 Na+、
Br一、SO32一

第Ⅱ卷(非选择题 共60分)
19.用一定量的铁与足量的CuO制单质铜,有人设计了以下两种方案:
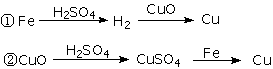

若按实验原则进行操作,则两者制得单质铜的量为( ) A.一样多 B.①多 C.②多 D.无法判断
18.为提纯下列物质(括号中为杂质),所选除杂试剂和分离方法都正确的是( )
|
选项 |
被提纯的物质(杂质) |
除杂试剂 |
分离方法 |
|
A |
NH3(H2O) |
浓硫酸 |
洗气 |
|
B |
乙酸乙酯(乙酸) |
饱和碳酸钠溶液 |
分液 |
|
C |
KCl固体(I2) |
KOH溶液 |
加热 |
|
D |
苯(苯酚) |
浓溴水 |
过滤 |
17. 利用右图装置(瓶口向上)不可行的实验是( )
利用右图装置(瓶口向上)不可行的实验是( )
A.A口进气,B口排气,用于收集H2
B.广口瓶中充满水,从A口进气用于收集O2 
C.广口瓶中盛有浓硫酸,从B口进气用于干燥SO2气体 
D.广口瓶中盛有NaOH水溶液,从B口进气用于除去Cl2中的HCl气体



16. 杠杆AB两端通过导线分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡(如右图),小心地向烧杯中央滴入浓CuSO4溶液,并反应一段时间。下列判断正确的是(不考虑实验过程中导线的反应及两球浮力的变化)( )
杠杆AB两端通过导线分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡(如右图),小心地向烧杯中央滴入浓CuSO4溶液,并反应一段时间。下列判断正确的是(不考虑实验过程中导线的反应及两球浮力的变化)( )
|
选项 |
杠杆材料 |
杠杆偏向 |
|
A |
绝缘体 |
A端高B端低 |
|
B |
绝缘体 |
仍保持平衡 |
|
C |
导体 |
A端高B端低 |
|
D |
导体 |
A端低B端高 |

15.在水中加入等物质的量的Mg2+、Ag+、Na+、SO42-、NO3-、Cl-,将所得溶液放入电解槽中用惰性电极电解片刻,则氧化产物与还原产物的质量之比为:(
)
A.71:216
B.16:207
C.8:1
D.108:35.5
14.用铂作电极电解500 mL含KNO3和Cu(NO3)2的混合溶液一段时间后,在两极均生成11.2 L标准状况下的气体,原溶液中Cu2+的物质的量浓度为( )
A、0.5 mol/L B、1 mol/L C、2 mol/L
D、无法确定
13.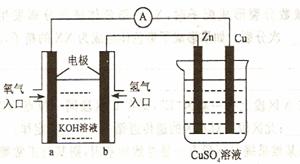 已知外电路中,电子由铜流向a极。有关下
已知外电路中,电子由铜流向a极。有关下
图所示的装置分析合理的一项是( )
A.该装置中Cu极为正极
B.当铜极的质量变化为12.8g时,a极上
消耗的O2在标准状况下的体积为2.24L
C.b极反应的电极反应式为:H2-2e-=2H+
D.KOH溶液中OH-向a电极移动


12. 右图为硫酸工业生产中的某一设备,下列说法正确的是:( )
右图为硫酸工业生产中的某一设备,下列说法正确的是:( )
A. 右图所示设备为吸收塔
B.在该设备中应该尽量增大压强,提高SO2的转化率
C.热交换的目的,一方面使即将参加反应的气体达到一定温度,另一方面降低体系温度有利于生成SO3
D.在A处流出的气体为SO2、SO3、O2

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com