
 本部分共4题,满分l60分。
本部分共4题,满分l60分。
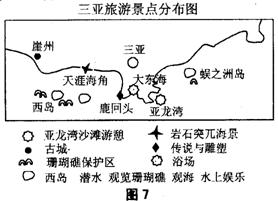
36.(36分)读图7,完成下列问题。
(1)天涯海角和亚龙湾景观区的海岸类型不同,成因也不同,天涯海角是________________作用下形成的地貌。亚龙湾海滨是_________________作用形成的地貌。(4分)
(2)三亚是海南岛最著名的旅游区,简要说明其
旅游资源的优势。(10分)
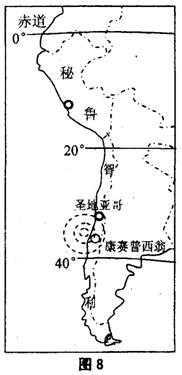
位于板块交界处的智利属于地震多发国家,全球每年约发生地震9000次,其中21%发生在智利.今年2月27日,智利沿海发生8.8级地震,释放的能量是海地7.3级地震的272倍,但人员伤亡却远没有海地惨重.
|
|
海地 |
智利 |
|
震级 |
7.3 |
8.8 |
|
震源深度(km) |
13 |
35 |
|
震中距 |
距首都太子 港15km |
距首都圣地亚哥325km 距康赛普西翁115km |
|
伤亡人数 |
20万人以上 |
700多人 |
(3)试根据上述材料并结合所学知识,说明智利地震人员伤亡远没
有海地地震惨重的原因。(8分)
(4)简述秘鲁沿海形成大渔场的原因。(6分)
(5)厄尔尼诺现象引起的全球气候异常倍受人们关注,回答下列问题。(8分)厄尔尼诺现象是指有的年份,_________________的现象,它常引起太平洋两岸气候异常:在热带太平洋东岸的表现是_______________,在太平洋西岸的表现是_______________,还使秘鲁等国渔业生产受到严重影响,其原因是_________________。
32.(10分)右下图为某反射弧的模式图.已知某化学物质可以阻断反射话动.请完成以下实验设计思路,以研究该化学物质是阻断了兴奋的神经纤维上的传导,还是阻断了兴奋在神经元之间的传递。
 (1)将实验材料分为甲、乙两组.实验开始时在
处
(1)将实验材料分为甲、乙两组.实验开始时在
处
给予适宜的电刺激,如果能引起肌肉收缩,刚说明该
材料符合实验要求。
(2)对甲组材料的处理是将该化学物质放在B处,从l处
给予刺激,观察肌肉是否收缩并记录。对乙组材料的
处理应是将该化学物质放在 处,从
处给予刺激,观察肌肉是否收缩并记录。
(3)预测实验结果和相应结论。
①
②
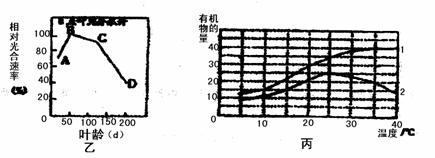
31.(每空2分,共14分)为了提高温室的经济效益;需要调控好室内的光照、温度、气体和湿度。科研人员对温室栽种的作物进行了相关研究,以下是实验测得的有关数据。(甲表所示为特殊的装置内,给予不同强度的光照,测到的该植物的氧气释放量。乙图表示该物光合速率(%)与叶龄的关系,A点表示幼叶成折叠状,B点表示叶充分展开。丙图中曲线1、2分别表示作物实际光合量和净光合量。
|
光照强度 |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
|
O2释放量(uL/cm2叶面·min |
-0.2 |
0 |
0.2 |
0.4 |
0.8 |
1.2 |
1.2 |
1.2 |
根据上述有关数据,回答下列有关问题
(1)从甲表可知在光照强度为4单位时,该作物光合作用的实际产氧量为 uL/cm2叶面。
(2)由乙图分析:
①新形成的嫩叶净光合速率(净光合速率 实际光合速率-呼吸速率)较低,从光合作用的光反应角度分析是由于
;从光合作用暗反应角度分析;可能的原因是
。
②CD段相对光合速率明显下降的原因是 。
(3)由丙图分析:最有利于积累有机物的温度是 ;如植物生活在12小时光照,12小时黑暗的环境中,则在环境温度达到约 时,该植物就不能能正常增长。原因是 。
30.(每空2分,共18分)正常成年人生成尿的过程中,部分液体若干成分的含量如下表所示。请参照图中所提供的信息和表中数据回答以下问题:
|
成分 |
水分 |
蛋白质 |
葡萄糖 |
尿素 |
K+ |
Na+ |
Cl- |
|
血浆/g.dL-1 |
90.0 |
7.0 |
0.1 |
0.03 |
0.02 |
0.32 |
0.37 |
|
原尿/g.dL-1 |
97.0 |
微量 |
0.1 |
0.03 |
0.02 |
0.32 |
0.37 |
|
尿液/g.dL-1 |
95.0 |
0.0 |
0.0 |
2.0 |
0.15 |
0.35 |
0.60 |
(1)通常成年人每天排尿量约1.5L,而原尿生成量可达150L,这-变化说明肾的
部位对水的重吸收能力很强,此过程起重要作用的激素是 ,该激素是由分泌的。遗传性肾源性尿崩症是因为相应结构鸯对激素的作用失去反应造成的,患者的明显症状是 。
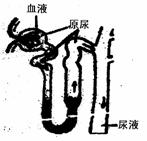 (2)若原尿中出现大量蛋白质,会引起血浆渗透压
(2)若原尿中出现大量蛋白质,会引起血浆渗透压
,从而会导致 症状。
(3)尿液与原尿成分相比,浓度增加量显著的是 。
此物质是由氨基酸经过 作用后转变而成。临
床上发现“血氨过多症Ⅱ”是由于一种酶的缺失导致血
氨的升高。有位男患者的母亲也患有此病,经检查其父
不含此致病基因,而他的姐姐是此基因的携带者,由此
推断控制该酶合成的基因属于 遗传。
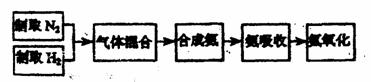
29.(20分)实验室模拟合成氨和氨催化氧化的流程如下:
 已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化
已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化
铵溶液经加热后反应制取氮气。
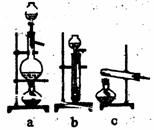
(1)从右图中选择制取气体的合适装置:氮气 、氢
气
(2)氮气和l氢气通过甲装置.甲装置抟作用除了将气体
混合外,还有 、
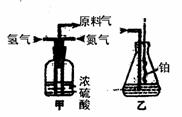 (3)氨合成嚣出来经冷却的气体连续通入乙装置的水中吸
(3)氨合成嚣出来经冷却的气体连续通入乙装置的水中吸
收氨, (“会”或“不会”)发生倒吸,原因
是: 。
(4)用乙装置吸收一段时问氨后,再通入空气,同时将经
加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红
热的原因是: ,锥
形瓶中还可观察到的现象是:
(5)写出乙装置中氨氧化的化学方程式:
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、 、 离子。
28.(15分)由Fe2O3、Fe、CuO、C,Al中的几种物质组成的混合粉末,取样进行下列实验
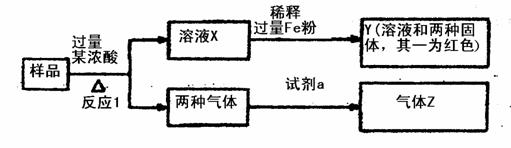 (都分产物略去):
(都分产物略去):
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液.通入CO2,无明显变化,说明样品中不含有的物质是(填化学式) 。
(2)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应I中能同时生成两种气体的化学方程式是 。
②若乙为两种气体的混合物,试剂a为适量的水.则Z中两种气体的化学式是
。
(3)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号) 。
(4)取Y中的溶液,调节pH约为7,加入淀粉KI和H3O2,溶液呈蓝色并有褐色沉淀生成。当消耗2mol时。共转移3mol电子,该反应的离子方程式是
(5)另取原样品,加入足量稀硫酸充分反应,若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中物质用化学式表示)
27.(15分)对从太空某星球外层空间取回的气体样品分析如下:
(1)将样品溶于水,发现其主要成分气体A极易溶于水。水溶液呈酸性
(2)将A的浓溶液与KmnO4反应产生一种黄绿色气体单质B,将B通入石灰乳可生成两种钙盐的混合物D。
(3)A的稀溶液与锌粒反应生成气体C,C与B的气体充分混合经光照发生爆炸又生成气体A,实验测的反应前后气体体积不变。
据此回答下列问题:
(1)写出A、B、C、D的化学式:
A ;B ;C ;D 。
(2)气体B与Ca(OH)2的化学反应方程式 ;混合物D俗名是 ,它的有效成分是 ,其有效成分与空气里的二氧化碳和水蒸气反应的方程式是 。
26.(10分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
 NO3-+4H++3e NO+2H2O
NO3-+4H++3e NO+2H2O
KWnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中硝酸体现了 、 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是 mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加.原因是:
。
25.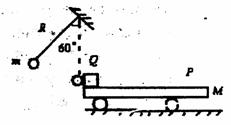 (20分)如图所示,质量为M的平板车p高h,质量为m的小物块Q的大小不计,位于平板车的左端,系统原来静止在光滑水平面地面上。一不可伸长的轻质细绳长为R.一端悬于Q正上方高为R处.另一端系一质量也为m的小球(大小不计).今将小球拉至悬线与竖直位置成60°角,由静止释放,小球到达最低点时与Q的碰撞时间极短,且无机械能损失,已知Q离开平板车时速度大小是平板车速度的两倍,Q与p之间的动摩擦因数为μ,M:m=4:1,重力加速度为g。求:
(20分)如图所示,质量为M的平板车p高h,质量为m的小物块Q的大小不计,位于平板车的左端,系统原来静止在光滑水平面地面上。一不可伸长的轻质细绳长为R.一端悬于Q正上方高为R处.另一端系一质量也为m的小球(大小不计).今将小球拉至悬线与竖直位置成60°角,由静止释放,小球到达最低点时与Q的碰撞时间极短,且无机械能损失,已知Q离开平板车时速度大小是平板车速度的两倍,Q与p之间的动摩擦因数为μ,M:m=4:1,重力加速度为g。求:
(1)小物块Q离开平板车时速度为多大?
(2)平板车p的长度为多少?
(3)小物块Q落地时距小球的水平距离为多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com