
1.下列区域的划分以单一指标为依据的是: ( )
①热量带 ②干湿区 ③我国三大自然区 ④文化区
A.①② B.②③ C.②④ D.③④
新的教育、教学形势下,教材、教学内容以及教学观念的转变,必将带来新的考试形式,考试命题。向往常一样,以章、节为单位,把大量的配套练习印发给学生,让学生从“题海”中吸收养分,弄得学生顾此失彼,晕头转向。这样的训练方式已经过时了。从2003年的全国高考题就足可以证明“题海”只能白白消耗学生的精力,而无助于他的考试。如何保证教师自己的“一桶水”的量和质是新的高考形式和内容,这对长期从事毕业班教学的教师提出了新的要求。我校的做法是:
l 关心并学习化学学科的新发展和新动向
l 教师深入学习新教材,充分理解所涉及的知识在新教材的位置,背景和要求。善于用新教材的教学理念指导高三复习工作。
l 教师苦心钻研考试说明,钻研来自全国各地的试题,信息,从中确定学生练习的题型、数量。学生每做一道题,必有目的,必有收获。教师对业务的深入钻研,时刻保持清醒的头脑,是备考的漫长过程中最困难,但也是至关重要的一步。
值得提出的是,高考的竞争日益激烈,我认为,就2003年高考题来说,各地区,各学校几乎是站在同一起跑线上起跑的,我们没有了以往的优势。这是摆在广大高三教师面前的一个很严峻的事实。短兵相接,鹿死谁手呢?新的教学理念,新的高考,这一切都留待我们用实践去探究,去研究。留待新一轮的开拓者--在座的各位老师们去努力,创造新的佳绩。
1.影响工业区位的因素很多,不同工业部门具有不同的区位指向。回答1-2题。
1.区位宜接近原料产地的是
A.葡萄酒厂、羊毛加工厂、水果罐头厂
B.服装加工厂、羊毛加工厂、水果罐头厂
C.造船厂、飞机制造厂、电子装配厂
D.钢铁厂、时装加工厂、家具厂
(2003年广东大综合高考题第37题)
37、(14分) (1)二氧化碳是共价化合物,它的电子式可表示为①。(2)实验室中检验CO2气体最方便的方法是将CO2气体通入饱和的澄清石灰水中,产生的实验现象是②,相应的反应方程式为③。(3)在宇宙飞船和太空站上工作的宇航员,在密闭的工作舱内需要吸入氧气,呼出CO2,飞船内可以使用一种物质,它能吸收CO2,并产生氧气,该物质是④,其反应方程式为⑤。
2. 高三是否开展研究性学习?怎样开展?
(2003年广东高考题第10题)下列有关纯铁的描述正确的是A.熔点比生铁的低B.与相同浓度的盐酸反应生成氢气的速率比生铁的快C.在潮湿空气中比生铁容易被腐蚀D.在冷的浓硫酸中被钝化
关注考试热点、难点?什么是考试的热点、难点?
在近年高考中重复出现的次数比较多的知识点叫热点。
在近年高考中出现过几次,而且试题有一定区分度的知识点叫热点。
(1)通过热点复习强化学生综合运用化学知识的能力
l 热点的回顾
虽然高考在改革中创新,但各大知识块的命题模式及各科的模型结构,仍有一定的规律可循。例如:将高考考试说明的考试要求作主线贯穿其中,注意有针对性地突破,无疑回增强必胜的信念。
l 题型的回顾
列举几个专题:(在第一阶段的教学中教师应有意识地作好这方面的准备工作)
l 反应物适量与过量的产物判断
l 多元酸的电离及应用规律
l 关于图象题(溶解度、化学平衡、混合物计算)
l 置换反应及其应用
l 喷泉实验的原理及综合应用
l 氧化还原反应原理在化学计算中的应用
l 离子方程式的书写及常见错误
l 原电池与电解池的相互关系
l 溶解平衡、电离平衡、水解平衡、化学平衡应用示例
l 气体净化规律
l 金属与酸反应的计算归纳
l 中学化学的几个实验操作(天平、pH试纸、容量瓶、中和滴定、浓硫酸、稀释、萃取、蒸馏原理)
l 以主族元素和有机官能团特征为主线,构建框图推断题
l 同分异构体的几种命题方法
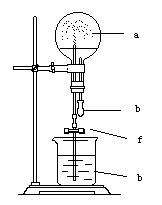 [例题14]:喷泉实验的原理极其综合应用
[例题14]:喷泉实验的原理极其综合应用
实验原理:教材中基于HCl,NH3气体分别以1:500,
1:700体积溶于水的原理设计实验。
|
|
A(干燥气体) |
B(液体) |
|
A |
NO2 |
水 |
|
B |
CO2 |
4mol/LNaOH溶液 |
|
C |
Cl2 |
饱和NaCl水溶液 |
|
D |
NH3 |
1mol/L盐酸 |
条件分析:①改变气体和溶剂对实验有何影响:在如图的装置中,烧瓶充满干燥气体a。将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f。烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
答:BD
②由于实验条件变化产生影响,如压力差不够,漏气等原因。
在标准状况下,体积为1L的干燥烧瓶中,用排空气法充入HCl气体后,测得瓶中气体对氧气的相对密度为1.082。此气体进行喷泉实验,当喷泉停止后,进入瓶中的液体体积是:
A.0.25L B.0.5L C.0.75L D.1L
[解析]用排空气法收集到的HCl常混有空气。根据相对密度可知混合气体平均分子量为34.6,而空气的平均分子量约为29,通过十字交叉法可以求出空气和氯化氢的体积比为1:3,即氯化氢占0.75L。故应选C。
综合应用:
①计算喷泉实验后烧瓶内溶液的浓度
 同温同压下,两个等体积的干燥圆底烧瓶中分别充满a.NH3b.NO2进行喷泉实验。经充分反应后,瓶内溶液的物质的量浓度为:
同温同压下,两个等体积的干燥圆底烧瓶中分别充满a.NH3b.NO2进行喷泉实验。经充分反应后,瓶内溶液的物质的量浓度为:
A.a>b B.a<b C.a=b D.不能确定
[解析]因为氨水的浓度与硝酸的浓度均相等,应选C。
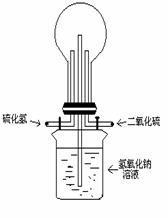
②设计实验:如图装置,(1)常温下将H2S,SO2以1:1
充满烧瓶,不久烧瓶中能观察到的现象是:_________________.
(2)若用Cl2代替SO2,其余同上。观察到现象与(1)相同和不同之处是:_______________.并试用简要文字和化学反应方程式解释原因。
[解析](1)有黄色沉淀,有水珠,溶液喷入烧瓶内2H2S+SO2=S↓+2H2O
(2)有黄色沉淀,没有喷泉现象。原因是:反应前后气体体积没有发生变化,不能产生压强差。Cl2+H2S=S↓+2HCl
研究性学习是以学生的自主性、探究性学习为基础,从学习和生活中选择和确定研究主题,以个人或小组合作的方式进行的一种新的学习模式。通过亲身实践获取直接经验,养成科学精神和科学态度,培养探究能力。高考与研究性学习的关系是怎样的?
1. 环境保护与研究性学习
化学高中新教材中多次出现环境保护的教学内容,环境问题也是目前全球引人关注的问题,配合2008年北京申办奥运会的需要,在化学教学中渗透环境教育显然是基础教育课程的任务。
(2003年上海高考题第2题)
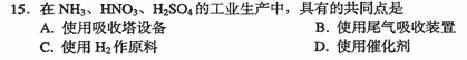
(2003年上海高考题第15题)

(2003年江苏省高考题第1题)

(2003年广东大综合高考题第1题)
2. 元素化合物逻辑推理
元素化合物知识的学习以化学概念的学习为基础,需要用各种化学概念来概括、组织、说明形形色色的物质及其化学现象,用关于物质的概念来概括其全部特征,运用化学概念作出有关的判断和推论。因此,概括的言语信息是元素化合物知识学习的主要形式。
物质之间按照一定规律转化,形成一定特征的转化关系,常见的有:
(1) 直线型转化关系


 金属
O2 碱性氧化物 水 碱 酸 盐
金属
O2 碱性氧化物 水 碱 酸 盐


 非金属
O2 酸性氧化物 水 酸 碱 盐
非金属
O2 酸性氧化物 水 酸 碱 盐
(2) 交叉转化关系
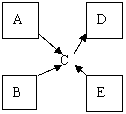
(3) 三角形转换关系
|

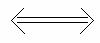
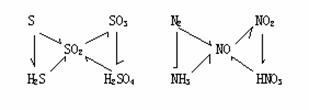
|
|||
|
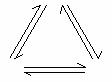
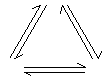
|
||||||||||
|
|
|
 |
|||||||

|

|
|||||||||
|
|
||||||||
|
|
||||||||


|
|
[例题10]在Na2CO3饱和溶液中通入CO2后有NaHCO3沉淀析出,除了NaHCO3溶解度小于Na2CO3这个主要原因外,另外的原因是__________.
[解析]将CO2通入Na2CO3溶液中,发生如下反应:Na2CO3+CO2+H2O=2NaHCO3。反应发生后,一方面水被消耗,溶剂的量减少;另一方面生成的NaHCO3的质量比Na2CO3的质量大,均有利于沉淀析出。
[评注]本题主要考查溶解度的知识。要经过周密思维,认真研究影响物质溶解度的可能因素,完整地答出要点。
[例题11] 设计实验验证由Cu和浓硝酸反应产生的混合气中有NO。已知:NO+NO2+2NaOH==2NaNO2+H2O
[解析] 在反应物中加入碳酸钠,把反应产生的气体通过无水氯化钙,再把气体通过以冰盐水做冷却剂的装置后,剩余气体用集气瓶收集。向集气瓶内鼓入空气,产生红棕色气体,说明反应有NO生成。
解答框图题的过程(甲物质向乙物质转变;丙问题向丁问题转移;反应物向生成物的不断趋进;条件向结论的曲线运动)是一个推理判断过程,具有严密的逻辑规律。因此,在解题过程中要善于逻辑推理,搞清网络中体现的因果关系、顺承关系、递进关系等,善于用合乎逻辑的思维,求得准确答案。
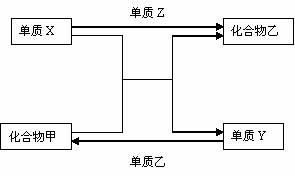 [例题12]X、Y、Z是3种短周期元素的单质,甲、乙是2种常见的化合物。这些单质和化合物之间存在所如图示的关系。据此判断:
[例题12]X、Y、Z是3种短周期元素的单质,甲、乙是2种常见的化合物。这些单质和化合物之间存在所如图示的关系。据此判断:
(1)在甲、乙两种化合物中,不含有组成X的元素的是 ,不含有组成Y的元素的是 (用“甲”、“乙”填写)。
(2)单质X是 (填“金属”、“非金属”或“既可以是金属又可以是非金属”)。
(3)若单质X ,则单质Y、Z分别是 ;若单质X ,则单质Y、Z分别是 ;若单质X ,则单质Y、Z分别是 。
[解析]解答本题需要有严密的推理和丰富的联想。
 (1)由图示:单质Y+单质Z 化合物甲,故甲中不含组成X的元素;单质X+单质Z 化合物乙,乙中不会含组成Y的元素。这种推理属因果关系推导。
(1)由图示:单质Y+单质Z 化合物甲,故甲中不含组成X的元素;单质X+单质Z 化合物乙,乙中不会含组成Y的元素。这种推理属因果关系推导。

 (2)由图示:单质X+化合物甲 单质Y+化合物乙,属置换反应,其类型很多,既可以是金属置换金属或非金属,又可以是非金属置换非金属或金属,因此结论是:既可以是金属又可以是非金属。
(2)由图示:单质X+化合物甲 单质Y+化合物乙,属置换反应,其类型很多,既可以是金属置换金属或非金属,又可以是非金属置换非金属或金属,因此结论是:既可以是金属又可以是非金属。
(3)按以上置换反应进行推理和联想,可得3组答案,分别为:
Mg,C、O2;Al,H2、Cl2;F2,O2、H2。
1. 实验现象的过程
观察能力是化学实验能力的组成部分,仔细观察实验过程所发生的现象,是科学实验的重要环节。
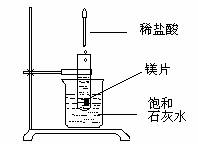 [例题9]把试管放入盛有25℃时饱和石灰水的烧杯中,
[例题9]把试管放入盛有25℃时饱和石灰水的烧杯中,
试管中开始放入几小块镁片,再用滴管滴入5ml
盐酸于试管中。试回答下列问题:
(1) 实验中观察到的现象是_________________.
(2) 产生上述现象的原因是_________________.
(3) 写出有关反应的离子方程式_____________.
(4) 由实验推知,MgCl2溶液和H2的总能量
(填“大于”、“小于”、“等于”)镁片和盐酸的总能量。
[解析](1)①镁片上有大量气泡产生;②镁片逐渐溶解;③烧杯中析出晶体
(2)镁与盐酸反应产生氢气,该反应为放热反应,Ca(OH)2在水中的溶解度随温度升高而减少,故析出Ca(OH)2晶体。
(3)Mg+2H+=Mg2++H2↑。(4)小于
实践证明,化学学习的效果不仅跟化学学习系统的状态有关,而且跟化学学习过程有关。在学习某知识时,学生可以通过记忆、背诵来学习,也可以通过实验、以及分类、比较等方法学习,从表面上看,通过不同的途径都可以达到相同的学习目标;而实际上,其潜在效应、学习迁移的可能性是不同的,研究化学学习过程自然成为考试的热门话题。
1. 实验操作过程
实验操作过程的试题是考查学生对实验操作技能的掌握程度,通过文字表达,检查学生在形成每一个环节技能是否达到熟练的程度。
[例题6]先选择填空,再简要说明作此选择的理由。
(1)某试管内装有约占其容积1/10的溶液,则溶液的体积。
A.约1ml B.约3ml C.约10ml D.无法确定
因为____________________________________。
(2)拟在烧杯中加热下配制其溶液50ml,应选择___________。
A.400ml烧杯 B.250ml烧杯
C.100ml烧杯 D.50ml烧杯
因为____________________________________。
[解析](1)D;题目并没有指明试管的大小规格。(2)C;选用烧杯的容积应比所配溶液的体积大一倍为最佳。
[例题7]回答下面问题
(1)在进行沉淀反应的实验时,如何认定沉淀已经完全?
(2)化学实验中,在过滤器上洗涤沉淀的操作是 。
[解析](1)在上层清液中(或取少量上层清液置于小试管中),滴加沉淀剂,如果不再产生沉淀,说明沉淀完全.(2)向漏斗里注入蒸馏水,使水面没过沉淀物,等水流完后,重复操作数次.
[例题8]实验室有一瓶氢氧化钠,已部分变质(不含水分),某学生设计了下列实验来确定其纯度,根据实验步骤填写有关空白处。
|
|
|
|
|
|
|
|
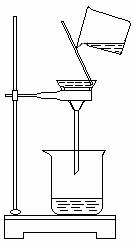







(1)用托盘天平和小烧杯称出一匙样品的质量,其正确操作的顺序为 。
①调零点,调节天平的小螺丝,使指针静止时刚好处于标尺刻度盘零处。 ②将游码拨放在刻度尺最左端零处。 ③称量空的小烧杯。 ④取样品放在小烧杯后再称量。 ⑤将法码放回法码盒。
(2)溶解样品所需仪器有 。
(3)加入的A溶液是 ,加过量试剂的目的是 ,确认B过量的方法是 。
(4)过滤时,某学生用如图所示的操作,其错误处有:① ;② 。
(5)沉淀需洗涤的原因是不是 ,洗涤的方法为 。
(6)若得到的沉淀为MCO3(相对分子质量为M),则样品中NaOH的纯度为 。
[解析](1) ②①③④⑤ (2)烧杯、玻璃棒。(3)CaCl2(或BaCl2、Ca(OH)2等);使CO32-全部生成CaCO3沉淀;可将溶液静置分层后向上层清液中再滴几滴CaCl2溶液,如无沉淀,说明已经沉淀完全。(4)①漏斗下端管口没有紧靠烧杯内壁;②漏斗里的液面高于滤纸的边缘。(5)防止沾上其他溶质而引起误差;再用蒸馏水冲洗沉淀2-3次。
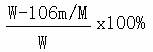 (6)
(6)
3. 化学实验设计及评价的基本思路
不论是实验设计还是对实验方案的评价,均要求学生综合运用所学到得的化学基础知识和实验技能技巧,选择恰当的实验方案来解决问题。因此,它们在化学实验考试目标中属于最高层次,是化学实验能力中应着重培养的重要方面。从近年的高考题分析,它大概包括:仪器连接方案设计、操作顺序设计、新情景下整个操作方案设计、物质提纯设计、验证某个化学原理的实验设计等;对评价的考查则突出学生对实验方案的全面理解和判断,其中大多数要求学生对方案的简便性、可行性作出评价。
2. 理解化学常规操作
化学实验能力表现在学生应具有有较强的“实验意识”,重视并善于通过化学实验来解决问题。能通过对问题的分析,从中提炼出恰当的化学实验课题;能用科学的语言准确、完整、清晰和具体地阐明问题。
[例题5](2003年广东高考试题)无水乙酸又称冰醋酸(熔点16.6℃)。在室温较低时,无水乙酸就会凝结成像冰一样的晶体。请简单说明在实验室中若遇到这种情况时,你将如何从试剂瓶中取出乙酸。
[解析]开放性答案试题。无论用什么方法,都不能出现回引起安全事故或人身伤害的方法。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com