
(五)应用:利用硫元素的价态变化规律,可进行如下判断:
1、判断含硫物质的氧化性、还原性。 2、判断不同价态硫之间能否发生氧化还原反应。
3、判断氧化、还原产物。 4、判断含硫物质发生化学反应可能生成的物质。
[思考感悟]浓H2SO4具有强氧化性,SO2具有还原性,那么浓H2SO4能否干燥SO2气体?
能,虽然浓H2SO4比SO2的S的价态高,但二者之间没有硫的中间价态,故浓H2SO4不能氧化SO2,能够干燥SO2气体。
[基础训练]
1、下列生成二氧化硫的反应中,反应物中的含硫物质被氧化的是( A )
A、硫在空气中燃烧 B、铜片与浓硫酸共热
C、红热的木炭与浓硫酸反应 D、亚硫酸钠与稀硫酸反应
2、将一定量的锌与100mL18.5mol·L-1浓硫酸充分反应后,锌完全溶解,同时生成气体A16.8L(标准状况)。将反应后的溶液稀释到1L,测得溶液的pH=0,则下列叙述中错误的是( C )
A、气体A为SO2和H2的混合物 B、气体A中SO2和H2的体积比为4︰1
C、反应中共消耗锌95.5g D、反应中共转移电子1.5mol
3、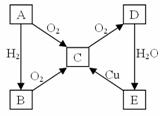 在通常状况下,A为固体单质。根据下图转化关系,回答:
在通常状况下,A为固体单质。根据下图转化关系,回答:
(1)写出A、C、E的化学式:A:S,C:SO2,E:H2SO4。
 (2)写出下列反应的化学方程式:
(2)写出下列反应的化学方程式:
1E→C:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O;

2C→D:2SO2+O2 2SO3。
(3)B与D的浓溶液能发生反应(填“能”或“不能”),若能反应,则反应的化学方程式为H2S+H2SO4(浓)=S↓+SO2↑+2H2O,反应现象为溶液变浑浊,有刺激性气味的气体放出。
(4)将C通入BaCl2溶液中,没有明显现象,但若加入H2O2,则有白色沉淀生成,请分析其原因,并写出有关的化学方程式:H2O2具有强氧化性,能把SO2氧化为H2SO4,H2O2+SO2=H2SO4;H2SO4+BaCl2=BaSO4↓+2HCl。
[高考模拟]4、(2007珠海模拟)根据下列实验事实所得出的相应结论正确的是( C )
|
|
实验事实 |
结论 |
|
A |
NH3的水溶液可以导电 |
NH3是电解质 |
|
B |
SO2通入酸性的硝酸钡溶液出现白色沉淀 |
BaSO3不溶于强酸 |
|
C |
Ca(ClO)2溶液中通入CO2产生白色沉淀 |
酸性:H2CO3>HClO |
|
D |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |
5、(2007江苏高考)工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO2转化为有用的副产品。请按要求回答下列问题:
(1)将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:2H2SO3+O2=2H2SO4、2(NH4)2SO3+O2=2(NH4)2SO4、2NH4HSO3+O2=2NH4HSO4(任填两个)。
(2)在尾气与氨水反应所得到的高浓度溶液中,按一定比例加入氨水或碳酸氢铵,此时溶液的温度会自行降低,并析出晶体。
①导致溶液温度降低的原因可能是反应吸热;
②析出的晶体可用于造纸工业,也可用于照相用显影液的生产。已知该结晶水合物的相对分子质量为134,则其化学式为(NH4)2SO3·H2O;
③生产中往往需要向溶液中加入适量的对苯二酚或对苯二胺等物质,其目的是防止亚硫酸铵被氧化。
(3)能用于测定硫酸尾气中SO2:含量的是BC。(填字母)
A、NaOH溶液、酚酞试液 B、KMnO4溶液、稀H2SO4
C、碘水、淀粉溶液 D、氨水、酚酞试液
(四)有时硫的化合价会发生跳位转化。
如S(-2)、S(0)遇到强氧化剂时,S(0)被氧化成S(+6)、S(-2)遇浓HNO3被氧化成S(+6);又如条件发生改变时:H2S遇冷浓H2SO4时被氧化成S;遇热浓H2SO4时被氧化成SO2。
(三)硫元素相邻价态的微粒不发生氧化还原反应。
如S和H2S、S和SO2、SO2和浓H2SO4之间不发生氧化还原反应。
(二)当硫元素的化合价升高或降低时,一般升高或降低到其相邻的价态。
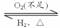
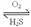

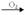 如H2S
S SO2
SO3。请写出各步反应的化学方程式:2H2S+O2(不足)
如H2S
S SO2
SO3。请写出各步反应的化学方程式:2H2S+O2(不足)



S+2H2O;S+O2 SO2;2SO2+O2 2SO3;2H2S+3O2(充足) 2SO2+2H2O;

 S+H2 H2S;SO2+2H2S=3S+2H2O。
S+H2 H2S;SO2+2H2S=3S+2H2O。
 请写出以下反应的方程式:浓硫酸与碳反应:2H2SO4(浓)+C 2SO2↑+CO2↑+2H2O;
请写出以下反应的方程式:浓硫酸与碳反应:2H2SO4(浓)+C 2SO2↑+CO2↑+2H2O;
浓硫酸与硫化氢反应:H2S+H2SO4(浓) S↓+SO2+2H2O。
(一)S(-2)是硫元素的最低价态,只有还原性;S(0)、S(+4)处于中间价态,既有氧化性,又有还原性,但S(+4)以还原性为主;S(+6)是硫元素的最高价,只有氧化性。
(二)硫元素的相互转化
1、实验室除去洒落汞的反应:Hg+S=HgS。
2、实验室制备SO2:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑。
3、Na2SO3变质:2Na2SO3+O2=Na2SO4。
(一)自然界中硫的存在形态
1、游离态:存在于火山喷口附近或地壳的岩层里。
2、化合态
(1)硫化物:如硫铁矿(FeS2)、黄铜矿(CuFeS2)等。
(2)硫酸盐:如石膏、芒硝等。
20. _____ her son has passed the college entrance examination makes her so happy.
A. That B. What C. Since D. Because
19.. _____ the Emei Mountain is famous for its beauty.
A. As is known to all B. It is known to all
C. It is known to us all that D. As we all know that
18. The villager didn’t want to sell the vegetables for _______ he thought was not enough.
A. what B. which C. that D. how
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com