
28、下图每一方框中的字母代表一种反应物或生成物:
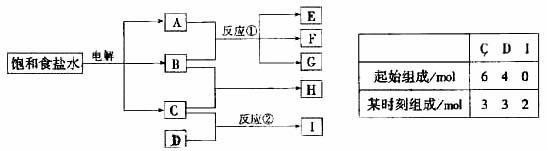

物质A跟B反应生成物质E、F和G;物质C跟D反应生成气体I,I能使湿润的红色石蕊试纸变蓝色.请填写下列空白:
(1)物质H的分子式是___________。
(2)写出电解饱和食盐水的化学方程式,并标出电子转移的方向和数目。
还原剂是___________。检验电解饱和食盐水的产物B的方法是: ________________________________________ 。
(3)反应①的化学方程式是_________________________________________。
(4)气体I你认为是 。
(5)电解食盐水时,通常需要先对食盐精制。为了有效除去泥沙、Ca2+、Mg2+、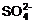 ,加入试剂的合理顺序为
(选填a,b,c)
,加入试剂的合理顺序为
(选填a,b,c)
a. 先加NaOH,后加Na2CO3,再加BaCl2试剂,再过滤后,加入适量盐酸。
b. 先过滤,然后加NaOH,后加BaCl2试剂,再加Na2CO3,加入适量盐酸。
c. 先加BaCl2试剂,后加NaOH,再加Na2CO3,再过滤后,加入适量盐酸。
27、某学习小组通过上网查阅资料得知:实验室可以用KMnO4与浓盐酸在常温下反应制取氯气,其反应的化学方程式为2KMnO4+16HCI(浓)=2KCI+2MnCl2+5Cl2↑+8H2O ,据此,他们设计了以下实验方案探究Cl2的性质。
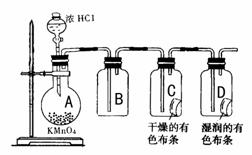

(1)实验时甲同学在B装置中未加入任何试剂,发现C、D中的红色纸条均褪色,由此甲同学得出结论:氯气具有漂白性。
实验时乙同学向B装置中加入了某种试剂,发现C中的红色纸条不褪色而D中的红色纸条褪色,由此乙同学得出结论:氯气没有漂白性。
你认为乙同学向B装置中加入的试剂是
,甲、乙两同学谁的结论合理?

(2)丙同学思考后认为上面的实验装置存在缺陷,并提出了解决方法。
你认为存在的缺陷是
,解决方法是(用化学方程式表示) 
(3)丁同学在B装置中加入滴有酚酞的NaOH溶液,观察到B装置中溶液红色逐渐褪去。他提出两种可能的原因:①氯气与水反应成次氯酸,次氯酸具有强氧化性,将酚酞氧化使溶液褪色;②氯气与NaOH反应使溶液褪色。请你帮他设计一个简单的实验验证褪色原因(简述实验步骤)。 
。
(4)、教材中实验室制取氯气的化学方程式为
,当有36.5克氯化氢被氧化时,生成标况下的氯气体积为
。
26、有A、B、C、D四种化合物,其焰色反应均为黄色。A、B、C与盐酸反应均生成D,B和C反应可生成A,C加热时产物中有A和无色气体E,在B溶液中通入气体E时,适量时可得A,过量时可得C,试回答下列问题:
(1)写出A、B、C、D四种化合物的化学式
A
B
C
D

(2)写出B溶液和C溶液反应生成A溶液的化学反应方程式

25、向NaBr和KI的混合溶液中通入足量Cl2后,将溶液蒸干并灼烧,最后得到的物质是
A.NaBr和KI
B.NaBr和KCl
C.NaCl和KCl D.NaCl、KCl和I2
24、下列关于离子的检验及结论一定正确的是
A.加入稀盐酸有无色气体生成,将气体通入澄清石灰水中溶液变浑浊,则溶液中一定含有
CO32-
B.加入BaCl2溶液有白色沉淀生成,再加盐酸,沉淀不消失,则溶液中一定有SO42-
C.加入氢氧化钠溶液并加热,生成的气体能使湿润的红色石蕊试纸变蓝,则溶液中一定含
有NH4+

D.加入碳酸钠溶液生成白色沉淀,再加盐酸白色沉淀消失,则溶液中一定含有Ba2+
23、将标准状况下的a升氯化氢气体溶于100克水中,得到的盐酸的密度为b克/毫升,则该盐酸的物质的量的浓度是
A、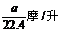 B、
B、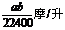 C、
C、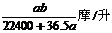 D
D 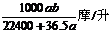

22.我国 “嫦娥”探月工程已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以42He的形式存在。下列说法正确的是:

A.
42He原子核内含有4个质子 B。32He和42He互为同位素
C.32He原子核内含有3个中子 
D.42He的最外层电子数为2,所以42He容易失去电子,有较强的还原性
21、根据以下反应:①H2S + I2
= 2H+ + 2I¯ +S↓;②H2SO3
+ 2H2S = 3S ↓+ 3H2O; 
③2 I¯ +Br2 = 2I2 +
2Br¯;④H2SO3 + I2 +
H2O = H2SO4 + HI 试确定Br-、I-、H2S和H2SO3的还原性由强到弱的顺序 :

A、H2S >
H2SO3 > I ¯ > Br¯ B、Br¯
> I ¯ > H2SO3 > H2S 
C、H2SO3
> H2S > Br¯ > I ¯ D、I ¯
> Br¯> H2S > H2SO3
20.浓盐酸和次氯酸钙能发生下列反应:Ca(ClO)2+4HCl(浓)==CaCl2+Cl2+2H2O 用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的气体是:①CO2
②HCl ③H2O(气) ④O2
A.①②③ B.②③④ C.②③ D.①④
19.下列四组溶液中每组都是三种,其中可用稀硫酸进行鉴别的一组是:
A.BaCl2 溶液 、Ba(NO3)2溶液 、 Na2CO3溶液
B.Na2CO3溶液 BaCl2 溶液 、NaCl溶液 
C.Ba(NO3)2溶液 、KCl 溶液 、MgCl2溶液
D.Na2CO3溶液、K2CO3 溶液 、NaCl溶液 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com