
31、某盐矿井采出的食盐(俗称井盐)中含有CaCl2,为设计除杂方案需测定CaCl2的含量;
准确称量上述井盐22.8g,向其中加入100g质量分数为10.6%的Na2CO3溶液恰好完全
反应,且所得食盐溶液仍为不饱和溶液。求:
(1) 井盐中CaCl2的质量分数(精确到0.1%,下同)
(2) 检测后的溶液中NaCl的质量分数。
2009山东枣庄东方国际学校冲刺中考全真模拟试题1
30、(3分)碳酸钙在高温下煅烧一段时间后,得到白色固体。两研究性学习小组的同学为了确定白色固体的成分,对其可能的组成进行探究。
[提出问题]白色固体的成分是什么?
I组:[作出猜想]白色固体的成分可能是CaCO3和CaO的混合物。
[实验验证](请你写出实验的步骤和现象):(2分)
__________________________________________________________________________
[实验结论]白色固体的成分是CaCO3和CaO的混合物。
II组:[作出猜想]白色固体可能全部是氧化钙。
[设计方案]取试样于试管中,加入少量水,再通入二氧化碳,变浑浊。
II组的方案是否正确?请说明理由______________________________________________
29、(4分)小刚为了解生活中常见的锌锰干电池,做了以下探究:他打
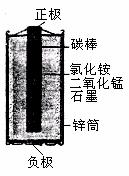 开一节废电池,观察到如下现象:1黑色碳棒完好无损;2电极周围充满黑色粉末;3里面有少量无色晶体;4金属外壳明显破损.
开一节废电池,观察到如下现象:1黑色碳棒完好无损;2电极周围充满黑色粉末;3里面有少量无色晶体;4金属外壳明显破损.
小刚查阅了资料:锌锰干电池的结果如图所示,它以中心的碳棒(石墨)做正极,外围的锌筒做负极,锌筒与碳棒之间填满用氯化铵溶液(做电解质)拌湿的二氧化锰和石墨,石墨不参加化学反应,仅起导电作用,在电池的使用中,锌逐渐变成了氯化锌。请你根据初中学习的知识和小刚的探究活动,填写以下空白。
(1)用碳棒做电极主要利用了石墨的_____________性。
(2)干电池在使用过程中的能量转化是_____________。
(3)以氯化锌为例,写出证明废电池中含有氯化物的化学方程式_____________________。
(4)通过回收废旧锌锰电池可得到的物质有__________________________(至少答2种).
28、(11分)家庭厨房就是一个化学小世界,“锅碗瓢盆”和“柴米油盐酱醋茶”中包含着许多化学知识。
(1)请回想一下自家厨房里的锅、碗、瓢、盆及各种炊具的名称,按材料所属类别填表(各举一例)
|
金属材料 |
无机非金属材料 |
合成材料 |
|
|
|
|
(2)现如今家庭厨房中的“柴”趋向洁净,有电能、煤气、天然气,还有___________气。我们在使用天然气等燃料过程中,有时会闻到一些特殊气味,这是加入的乙硫醇的气味,加入乙硫醇的作用是__________________________,如果厨房中闻到浓烈的乙硫醇的特殊气味,下列应急措施可行的是(填写序号)_____________
A、检查并关闭气源阀门,防止气体进一步泄漏 B、轻轻打开门窗通风
C、立即打开抽排油烟机排气,将泄漏出的气体尽快排出室内
(3)大米、面粉的主要成分都是_____________,它是人体所必需的六大营养素之一。液态的油和固态的动物油合称为油脂,对人体的作用是__________________________。
(4)茶叶、肉松、膨化食品等常采用真空充气包装,所充入的气体可能是_____________。
某些食品包装袋内常有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”。下列物质属于双吸剂的是(填写序号)_____________
A、碳粉 B、铁粉 C、氯化钙 D、生石灰
(5)味精是烹制菜肴的调味品,味精的鲜味与溶液的酸碱度有关,当PH为6-7时鲜味最强;味精的鲜味还与温度有关,其水溶液经120℃以上长时间加热,不仅鲜味消失,而且生成对人体有害的焦谷氨酸钠。据此,下列认识不正确的是(填写字母代号)_____________
A、谷氨酸钠在加热条件下生成谷氨酸钠是物理变化
B、菜烧熟起锅后再放味精比炒菜过程中加入味精更有利于人体健康
C、加入味精时,应避免在酸性或碱性较强的条件下使用
D、研究问题的一种有效方法是通过实验
(二)问题探究:
(1)E中的药品为_____________,E的作用是_____________________________________。
C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是_____________________
__________________________,F的作用是_______________________________________,
G的作用是_______________________________________。
(2)实验步骤②与③能否颠倒_____________(填“能”或“不能”)。若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数__________________________(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是__________________________
(3)据右表数据计算可得:天然碱的化学式中a:b:c=__________________________。
|
反应前 |
反应后 |
|
E的质量为100.0g |
E的质量为102.25g |
|
F的质量为50.0g |
F的质量为51.1g |
(一)实验步骤 ①组装好装置,检查气密性 ②反复推拉注射器 ③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行 ⑤打开弹簧夹,再次反复缓缓推拉注 射器 ⑥再次称量E、F的质量。
24、(1分)下列做法符合操作规范的是_______(填写序号)
①为了节约药品,将实验用剩的药品放回原试剂瓶中
②使用托盘天平称量时,用镊子取放砝码
③给试管中的液体加热时,液体的量不超过试管容积的1/3
④过滤时,为了加快过滤速度,用玻璃棒搅动漏斗里的液体
⑤不慎将浓碱溶液沾在皮肤上,立即用大量的水冲洗,再涂上硼酸溶液
⑥稀释浓硫酸时,先在量筒里加入一定体积的蒸馏水,再沿量筒内壁慢慢加入浓硫酸,并不断搅拌
25、(6分)A为含三种元素的钠盐,C为相对分子质量为100的白色不溶物,请填空:
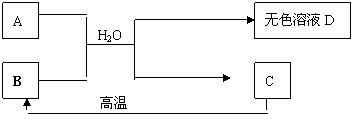
(1)A_____________、B_____________、C_____________。(填写化学式)
(2)D中一定含有的溶质是_____________。理由是(用化学方程式表示)
____________________________________________________。
(3)D还可能含有溶质是__________________________。
26、(2分)现有失去标签的两瓶黄色溶液:碘水和硝酸铁溶液,试鉴别这两种物质,请写出你的鉴别方法(至少填两种,写出三种且正确另加1分)
(1)_________________________________________________________________
(2)_________________________________________________________________
(3)_________________________________________________________________
27、(9分)我国青海湖采集的天然碱样品可表示为aNa2CO3·bNaHCO3·cH2O(a、b、c为最简整数比)。小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验:
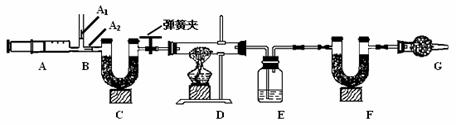
已知:1、碳酸钠比较稳定,加热时不分解 ;
2、2NaHCO3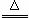 Na2CO3↑+CO2 ↑+H2O
Na2CO3↑+CO2 ↑+H2O
3、图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1
打开进空气,A2关闭。
23、(8分)金属材料在生活中普遍使用。
(1)铁制品表面的锈要及时除去,这是因为铁锈__________________________会加快铁制品的生锈。铝制品不需要除锈,这是因为铝表面能形成__________________________,可以阻止铝进一步氧化。
(2)我国铜陵市是中国著名的“铜都”,铜矿蕴藏丰富,炼铜历史悠久。该地产的一种矿石叫辉铜矿,主要成分为硫化亚铜(Cu2S),其中铜的化合价是______,铜元素与硫元素的质量比为__ ____。当地还产一种矿石叫孔雀石,成分Cu2(OH)2CO3,加热时生成三种氧化物。该反应的化学方程式为__________________________________,反应类型是____________,反应中生成的黑色氧化物在一定条件下能被还原,生成红色固体,在该反应中可加入的还原剂有_____________、_____________等。
22、(3分)举例来证明下列结论是错误的:
(1)金属都能和酸发生置换反应生成盐和氢气__________________________。
(2)生成沉淀的反应一定是复分解反应__________________________。
(3)物质的溶解度随着温度的升高都会增大__________________________。
21、(4分)用化学用语表示:
5个磷原子_____________;硝酸铝_____________;
最高价硫元素的氧化物_____________;不含金属元素的碱_____________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com