
22、1,3-丁二烯和氢气的混合气体5L,在催化剂作用下,经充分反应后得到的气体体积为VL(所有体积均在同温、同压下测定)。
(1)若氢气的体积为1L,计算反应后的体积V。
(2)若氢气在混合气体中的体积比值为x,计算x为不同值时反应后的体积V(以x表示)。
(3)在右图上画出V随x变化的曲线。
(4)在上述混合气体中若混有丙炔,总体积仍为5L,其中氢气及丙炔在混合气体中的体积比值分别为x和y。(i)在下面左图上画出当y=0.2时,V随x变化的曲线;(ii)在下面右图上画出当x=0.15时,V随y变化的曲线。
21、有一包固体混合物中含有硝酸钾和不溶性杂质,把它们放入一定量的水中充分溶解,其结果如下表:
|
温度 |
10℃ |
40℃ |
75℃ |
|
剩余固体 |
261g |
175g |
82g |
硝酸钾溶解度表
|
温度℃ |
10 |
40 |
50 |
55 |
60 |
65 |
75 |
80 |
|
溶解度g |
20.9 |
63.9 |
85.5 |
95 |
110 |
126 |
150 |
169 |
(1)通过计算,所用水的质量是多少?
(2)原固体中含硝酸钾的质量是多少?
(3)若要完全溶解此混合物中的硝酸钾,所必须的最低温度接近多少?
20、已知反应:(1)2Fe3++2I-=2Fe2++I2 (2) 2Fe2++Br2=2Fe3++2Br- (3) 2Br-+ Cl2= Br2+2Cl-。现向含amolFeI2和bmolFeBr2的混合液中逐渐通入cmolCl2,反应随Cl2通入明显分几个阶段进行,试分别填写在C值增大过程中,不同C值范围内,被氧化的离子及被氧化的离子的物质的量(用a、b、c代数式表示)。
|
反应物物质的量之间的关系 |
此阶段被氧化的粒子 |
被氧化的粒子的物质的量 |
|
0<c≤a |
|
|
|
a<c≤(3a+b)/2 |
|
|
|
(3a+b)/2<c≤3 (a+b)/2 |
|
|
19.(10分)聚合硫酸铁硫酸铁(PFS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铁的氧化物为原料来制取PFS,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+。生产步骤如下:
 (1)步骤I能否用HCl代替H2SO4 ?
(填“能”或“不能”)。
(1)步骤I能否用HCl代替H2SO4 ?
(填“能”或“不能”)。
(2)步骤II取样分析溶液中的Fe2+、Fe3+的含量,目的是 。
(3)步骤III所用的还原剂是 。
(4)步骤IV用NaClO3或 HNO3氧化时反应方程式(注意均未配平)如下:
FeSO4 + NaClO3 + H2SO4 → Fe2(SO4)3 + NaCl + H2O
FeSO4 + HNO3 + H2SO4 → Fe2(SO4)3 + NO↑ + H2O
已知1mol HNO3价格0.16元、1mol NaClO3价格0.45元,评价用HNO3代替NaClO3作氧化剂的利弊是 。
(5)产品PFS溶液中SO42-与Fe3+物质的量之比不是3:2。步骤V先加入NaOH溶液和 BaCl2溶液,目的是测定产品中SO42-与Fe3+物质的量之比。测定时需要称量 和 的质量。
18、有甲乙两个容积均为1L的密闭容器,在控制两容器的温度相同且恒定的情况下进行反应:2A(g)+B(g) 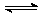 xC(g),①向甲中通入4molAt 2molB,达平衡时测得其中C的体积分数为40%;②向乙中通入1molA、0.5molB和3molC,平衡时测得C的体积分数为W%。试回答:(1)甲平衡时A的体积分数为;
xC(g),①向甲中通入4molAt 2molB,达平衡时测得其中C的体积分数为40%;②向乙中通入1molA、0.5molB和3molC,平衡时测得C的体积分数为W%。试回答:(1)甲平衡时A的体积分数为;
(2)若乙W%=40%,且建立平衡的过程中乙内压强有变化 ,则x= ,乙中建立平衡时压强的变化 为 (填“递增”或“递减”)。
(3)若乙W%=40%,且平衡时甲、乙压强不同,则x= ,平衡时甲的压强 乙的压强(填“大于”或“小于”),乙平衡时c(A)平= 。
(4)若x=4,则W% (填“大于”、“小于”或“等于”,下同);平衡时乙中的c(A) 甲中的c(A)。
17、在一定温度下,在一个固定容积的密闭容器中,可逆反应: A(g) + 2B(g)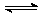 C(g)达到平衡时,c(A)平=2mol/L,c(B)平=7mol/L ,c(C)平=2mol/L。试确定B的起始浓度c(B)的取值范围
;若向容器中继续注入一定量的氦气(不参与反应),足够长的时间后,体系中B的物质的量浓度 (填“增大”、“减小”或“不变”下 同),混合气体的密度 。
C(g)达到平衡时,c(A)平=2mol/L,c(B)平=7mol/L ,c(C)平=2mol/L。试确定B的起始浓度c(B)的取值范围
;若向容器中继续注入一定量的氦气(不参与反应),足够长的时间后,体系中B的物质的量浓度 (填“增大”、“减小”或“不变”下 同),混合气体的密度 。
16、将1.0molCO和1.0mol水蒸气充入固定容积的反应器中,在一定条件下反应:
CO(g)+H2O(g) 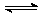 CO2(g)+H2(g)。达到平衡时有2/3的一氧化碳转化为二氧化碳。在相同条件下,将1.0molCO和2.0mol H2O(g)充入同一反应容器中,在相同温度下达到平衡后,平衡混合气体中二氧化碳的体积分数可能是
CO2(g)+H2(g)。达到平衡时有2/3的一氧化碳转化为二氧化碳。在相同条件下,将1.0molCO和2.0mol H2O(g)充入同一反应容器中,在相同温度下达到平衡后,平衡混合气体中二氧化碳的体积分数可能是
A、22.2% B、28.2% C、33.3% D、37.8%
15、在一恒定的容器中充入2molA和1molB发生反应:2A(g)+B(g) 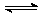 xC(g),达到平衡后,C的体积分数为ω%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol;C:1.4mol充入容器,达到平衡后,C的体积分数仍为ω%,则x的值可能为
xC(g),达到平衡后,C的体积分数为ω%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol;C:1.4mol充入容器,达到平衡后,C的体积分数仍为ω%,则x的值可能为
A、2 B、3 C、4 D、无法判断
14、用质量均为100g的Cu作电极电解AgNO3溶液,电解一段时间后,两电极质量相差28g,此时两电极质量分别是(
)
A.阳极93.6g,阴极121.6g  B.阳极100 g,阴极128.0g
B.阳极100 g,阴极128.0g
C.阳极91.0g,阴极119.0g  D.阳极86.0g,阴极114.0g
D.阳极86.0g,阴极114.0g 
13、铜与1mol/L的硝酸反应,如果硝酸根的浓度下降0.2mol/L,则溶液中的c(H+)同时下降( )
A.0.2mol/L B. 0.4mol/L C. 0.6mol/L D. 0.8mol/L
C. 0.6mol/L D. 0.8mol/L 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com