
 化合价降低(得ne―)被还原
化合价降低(得ne―)被还原
(较强)(较强) (较弱) (较弱)
氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
盐类水解,水被弱解;有弱才水解,无弱不水解;越弱越水解,都弱双水解;谁强呈谁性,同强呈中性。
电解质溶液中的守恒关系
⑴电荷守恒:电解质溶液中所有阳离子所带有的正电荷数与所有的阴离子所带的负电荷数相等。如NaHCO3溶液中:n(Na+)+n(H+)=n(HCO3-)+2n(CO32-)+n(OH-)推出:[Na+]+[H+]=[HCO3-]+2[CO32-]+[OH-]
⑵物料守恒:电解质溶液中由于电离或水解因素,离子会发生变化变成其它离子或分子等,但离子或分子中某种特定元素的原子的总数是不会改变的。如NaHCO3溶液中:n(Na+):n(c)=1:1,推出:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
⑶质子守恒:(不一定掌握)电解质溶液中分子或离子得到或失去质子(H+)的物质的量应相等。例如:在NH4HCO3溶液中H3O+、H2CO3为得到质子后的产物;NH3、OH-、CO32-为失去质子后的产物,故有以下关系:c(H3O+)+c(H2CO3)=c(NH3)+c(OH-)+c(CO32-)。

 氧化剂 +还原剂= 还原产物+氧化产物
氧化剂 +还原剂= 还原产物+氧化产物


 化合价升高(失ne―)被氧化
化合价升高(失ne―)被氧化
白磷的分子结构为正四面体,一个白磷分子中含有6个P-P共价键,所以,0.25mol白磷中含有1.5NA个P-P共价键。
⑽不正确,Fe3+在溶液中水解。
本题答案为⑴⑵⑹⑺
升失氧还还、降得还氧氧
(氧化剂/还原剂,氧化产物/还原产物,氧化反应/还原反应)
⑼不正确,白磷分子的分子式为P4,其摩尔质量为124g/mol,31g白磷相当于0.25mol,
⑻不正确,标准状况下,辛烷是液体,不能使用标准状况下气体的摩尔体积22.4L/mol这一量,所以1L辛烷的物质的量不是1/22.4mol。
少于1mol,标准状况下,其体积小于22.4L
⑸不正确,重水分子(D2O)中含有10个中子,相对分子质量为 20,18g重水所含中子数为:10×18g/20g? mol-1=9mol。
⑹正确,1个氦原子核外有4个电子,氦气是单原子分子,所以1mol氦气含有4mol
电子,这与外界温度和压强无关。
⑺正确,不论在任何条件下,2g氢气都是1mol,无论什么金属生成氢气的反应均可表示为:2H++2e=H2↑,因此,生成1mol氢气一定转移 2mol电子。
⑷不正确,因为存在以下平衡:2NO2 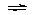 N2O4(放热),降温,平衡正向移动,分子数
N2O4(放热),降温,平衡正向移动,分子数
⑵正确,任意比例混合的甲烷和丙烷混合气体 22.4L,气体的总物质的量为1mol,因此含有NA个分子。
⑶不正确,因为NO和氧气一接触就会立即反应生成二氧化氮。
⑻标准状况下,1L辛烷完全燃烧后,所生成气态产物的分子数为
⑼31g白磷分子中,含有的共价单键数目是NA个
⑽1L1 mol•L-1的氯化铁溶液中铁离子的数目为NA
【点拨】⑴正确,1mol氮气的分子数与是否标准状况无关。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com