
8.(07江苏卷)阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是( )
(A)2.24 L CO2中含有的原子数为0.3×6.02×1023
(B)0.1 L 3 mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023
(C)5.6 g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023
(D)4.5 g SiO2晶体中含有的硅氧键数目为0.3×6.02×1023
7.(07广东卷)下列叙述正确的是( )
(A)48 g O3气体含有6.02×1023个O3分子
(B)常温常压下,4.6 g NO2气体含有1.81×1023个NO2分子
(C)0.5 mol·L-1 CuCl2溶液中含有3.01×1023个Cu2+
(D)标准状况下,33.6 L H2O含有9.03×1023个H2O分子
6.(08山东卷)NA代表阿伏加德罗常数,下列叙述错误的是( )
A.10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8%
B.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D.一定温度下,1 L 0.50 mol·L-1 NH4Cl溶液与2 L 0.25 mol·L-1 NH4Cl溶液含NH+4物质的量不同
5.(08江苏卷)用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA
B.标准状况下,22.4L己烷中共价键数目为19NA
C.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
D.1L浓度为1mol·L-1的Na2CO3溶液中含有NA个CO32-
4.(08广东卷)设阿伏加德罗常数(NA)的数值为nA,下列说法正确的是( )
A.1molCl2与足量Fe反应,转移的电子数为3nA
B.1.5 mol NO2与足量H2O反应,转移的电子数为nA
C.常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3nA
D.0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10nA
3.(08上海卷)设NA为阿伏加德罗常数,下列说法正确的是( )
A.23gNa在氧气中完全燃烧失电子数为0.5NA
B.1L2mol·L-1的MgCl2溶液中含Mg2+数为2NA
C.标准状况下,11.2LSO3所含分子数为0.5NA
D.室温下,8g甲烷含有共价键数为2NA
2.(08海南卷)设NA为阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,5.6L四氯化碳含有的分子数为0.25NA
B.标准状况下,14g氮气含有的核外电子数为5NA
C.标准状况下,22.4L任意比的氢气和氯气的混合气体中含有的分子总数均为NA
D.标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA
1.(08广东卷)能表示阿伏加德罗常数数值的是( )
A.1mol金属钠含有的电子数
B.标准状况下22.4L苯所含的分子数
C.0.012kg12C所含的原子数
D.1L1mol·L-1的硫酸溶液所含的H+数
28. (1)124.2。
(2)C3H8+5O2===3CO2+4H2O;负。
(3)4.2×10-7 mol·L-1。
(4)> ;HCO3-+H2O CO32-+H3O+(或HCO3-
CO32-+H3O+(或HCO3- CO32-+H+)。
CO32-+H+)。
HCO3-+H2O H2CO3+OH-、HCO3-的水解程度大于电离程度
H2CO3+OH-、HCO3-的水解程度大于电离程度
(3)P(S)+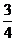 O2(g) =
O2(g) = 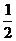 P2O3(S);△H=-(20X-Y)KJ/mol
P2O3(S);△H=-(20X-Y)KJ/mol
27.(1)P(s)+Cl2(g)===PCl3(g);△H=-306kJ·mol-1。
(2)PCl5(g)===PCl3(g)+Cl2(g);△H=93kJ·mol-1。25%;大于。
(3)两步反应均为放热反应,降低温度有利于提高产率,防止产物分解。
(4)-399kJ·mol-1;等于。
(5)PCl5+4H2O===H3PO4+5HCl。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com