
2£®(08¹ã¶«¾í)ÔªËØX¡¢YºÍZ¿É½áºÏÐγɻ¯ºÏÎïXYZ3£»X¡¢YºÍZµÄÔ×ÓÐòÊýÖ®ºÍΪ26£»YºÍZÔÚͬһÖÜÆÚ¡£ÏÂÁÐÓйØÍƲâÕýÈ·µÄÊÇ(¡¡ )
A£®XYZ3ÊÇÒ»ÖÖ¿ÉÈÜÓÚË®µÄËᣬÇÒXÓëY¿ÉÐγɹ²¼Û»¯ºÏÎïXY
B£®XYZ3ÊÇÒ»ÖÖ΢ÈÜÓÚË®µÄÑΣ¬ÇÒXÓëZ¿ÉÐγÉÀë×Ó»¯ºÏÎïXZ
C£®XYZ3ÊÇÒ»ÖÖÒ×ÈÜÓÚË®µÄÑΣ¬ÇÒYÓëZ¿ÉÐγÉÀë×Ó»¯ºÏÎïYZ
D£®XYZ3ÊÇÒ»ÖÖÀë×Ó»¯ºÏÎÇÒYÓëZ¿ÉÐγÉÀë×Ó»¯ºÏÎïYZ3
1£®(08È«¹ú¢ñ¾í)ÏÂÁи÷×é¸ø¶¨Ô×ÓÐòÊýµÄÔªËØ£¬²»ÄÜÐγÉÔ×ÓÊýÖ®±ÈΪ1¡Ã1Îȶ¨»¯ºÏÎïµÄÊÇ(¡¡¡¡ )
A£®3ºÍ17¡¡¡¡¡¡ ¡¡¡¡ B£®1ºÍ8¡¡¡¡ ¡¡¡¡ C£®1ºÍ6¡¡¡¡ ¡¡¡¡¡¡ D£®7ºÍ12
33£®(04ÉϺ£¾í)ϱíÊÇÔªËØÖÜÆÚ±íµÄÒ»²¿·Ö¡£
|
×å¡¡¡¡ ÖÜÆÚ |
¢ñA |
¢òA |
¢óA |
¢ôA |
¢õA |
¢öA |
¢÷A |
|
1 |
¢Ù |
¡¡ |
|||||
|
2 |
¢Ú |
¢Û |
¢Ü |
¡¡ |
¢Ý |
¢Þ |
¡¡ |
|
3 |
¡¡ |
¢ß |
¢à |
¡¡ |
¡¡ |
¢á |
¢â |
(1)±íÖÐÔªËØ¢âµÄÇ⻯ÎïµÄ»¯Ñ§Ê½Îª¡¡¡¡¡¡¡¡¡¡ £¬´ËÇ⻯ÎïµÄ»¹ÔÐÔ±ÈÔªËØ¢áµÄÇ⻯ÎïµÄ»¹ÔÐÔ¡¡ ¡¡¡¡¡¡¡¡¡¡(ÌîÇ¿»òÈõ)¡£
(2)ijԪËØÔ×ӵĺËÍâ×îÍâ²ãµç×ÓÊý±È´ÎÍâ²ãµç×ÓÊý¶à3£¬Ôò¸ÃÔªËصÄÔªËØ·ûºÅÊÇ¡¡¡¡¡¡ £¬Æäµ¥Öʵĵç×ÓʽΪ¡¡¡¡¡¡¡¡ ¡£
(3)Ë׳ÆΪ¡°·¯¡±µÄÒ»À໯ºÏÎïͨ³£º¬Óй²Í¬µÄÔªËØÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(4)ÒÑ֪ijЩ²»Í¬×åÔªËصÄÐÔÖÊÒ²ÓÐÒ»¶¨µÄÏàËÆÐÔ£¬ÈçÔªËØ¢ÛÓëÔªËØ¢àµÄÇâÑõ»¯ÎïÓÐÏàËƵÄÐÔÖÊ¡£Ð´³öÔªËØ¢ÛµÄÇâÑõ»¯ÎïÓëNaOHÈÜÒº·´Ó¦µÄ»¯Ñ§·½³Ìʽ
¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£
ÓÖÈç±íÖÐÓëÔªËآߵÄÐÔÖÊÏàËƵIJ»Í¬×åÔªËØÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ (ÌîÔªËØ·ûºÅ)¡£
32£®(06È«¹ú¾í)X¡¢Y¡¢ZºÍW´ú±íÔ×ÓÐòÊýÒÀ´ÎÔö´óµÄËÄÖÖ¶ÌÖÜÆÚÔªËØ£¬ËüÃÇÂú×ãÒÔÏÂÌõ¼þ£º
¢ÙÔÚÔªËØÖÜÆÚ±íÖУ¬ZÓëYÏàÁÚ£¬ZÓëWÒ²ÏàÁÚ£»
¢ÚY¡¢ZºÍWÈýÖÖÔªËصÄÔ×Ó×îÍâ²ãµç×ÓÊýÖ®ºÍΪ17¡£
ÇëÌî¿Õ£º
(1)Y¡¢ZºÍWÈýÖÖÔªËØÊÇ·ñλÓÚͬһÖÜÆÚ(Ìî¡°ÊÇ¡±»ò¡°·ñ¡±)£º¡¡¡¡¡¡¡¡ £¬ÀíÓÉÊÇ
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(2)YÊÇ ¡¡¡¡¡¡£¬ZÊÇ¡¡¡¡¡¡ £¬WÊÇ¡¡¡¡¡¡ £»
(3)X¡¢Y¡¢ZºÍW¿É×é³ÉÒ»»¯ºÏÎÆäÔ×Ó¸öÊýÖ®±ÈΪ8¡Ã2¡Ã4¡Ã1¡£Ð´³ö¸Ã»¯ºÏÎïµÄÃû³Æ¼°»¯Ñ§Ê½¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
31£®(06È«¹ú¾í)ÒÑÖªX¡¢Y¡¢Z¶¼ÊǶÌÖÜÆÚµÄÔªËØ£¬ËüÃǵÄÔ×ÓÐòÊýÒÀ´ÎµÝÔö£¬XÔ×ӵĵç×Ó²ãÊýÓëËüµÄºËÍâµç×Ó×ÜÊýÏàͬ£¬¶øZÔ×ÓµÄ×îÍâ²ãµç×ÓÊýÊÇ´ÎÍâ²ãµÄÈý±¶£¬YºÍZ¿ÉÒÔÐγÉÁ½ÖÖÒÔÉÏÆø̬»¯ºÏÎÔò
(1)XÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ £¬YÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ £¬ZÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)ÓÉYºÍZ×é³É£¬ÇÒYºÍZµÄÖÊÁ¿±ÈΪ7¡Ã20µÄ»¯ºÏÎïµÄ»¯Ñ§Ê½(·Ö×Óʽ)ÊÇ¡¡¡¡¡¡ ¡£
(3)ÓÉX¡¢Y¡¢ZÖеÄÁ½ÖÖÔªËØ×é³É£¬ÇÒÓëX2Z·Ö×Ó¾ßÓÐÏàͬµç×ÓÊýµÄÁ½ÖÖÀë×ÓÊÇ¡¡¡¡¡¡
ºÍ¡¡¡¡¡¡¡¡ ¡£
(4)X¡¢Y¡¢Z¿ÉÒÔÐγÉÒ»ÖÖÑΣ¬´ËÑÎÖÐX¡¢Y¡¢ZÔªËصÄÔ×ӵĸöÊý±ÈΪ4©U2©U3£¬¸ÃÑεĻ¯Ñ§Ê½(·Ö×Óʽ)ÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
29£®(06ÉϺ£¾í)ϱíÖеÄʵÏß±íʾԪËØÖÜÆÚ±íµÄ²¿·Ö±ß½ç¡£¢Ù£¢Ý·Ö±ð±íʾԪËØÖÜÆÚ±íÖжÔӦλÖõÄÔªËØ¡£
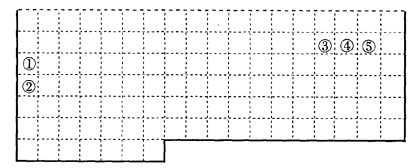
(1)ÇëÔÚÉϱíÖÐÓÃʵÏß²¹È«ÔªËØÖÜÆÚ±í±ß½ç¡£
(2)ÔªËØ¢Ü-°ãÔÚ»¯ºÏÎïÖÐÏÔ¡¡¡¡ ¼Û£¬µ«Óë¡¡¡¡ Ðγɻ¯ºÏÎïʱ£¬ËùÏÔʾµÄ¼Û̬ÔòÇ¡ºÃÏà·´¡£
(3)ÔÚÔªËآٵĵ¥ÖÊ¡¢ÔªËآڵĵ¥ÖʺÍÔªËآ٢ÚÐγɵĺϽðÕâÈýÖÖÎïÖÊÖУ¬ÈÛµã×îµÍµÄÊÇ¡¡¡¡¡¡ ¡£
¡¡¡¡ a£®ÔªËآٵĵ¥ÖÊ¡¡ b£®ÔªËآڵĵ¥ÖÊ¡¡¡¡ c£®ÔªËآ٢ÚÐγɵĺϽ𡡠d£®ÎÞ·¨ÅжÏ
(4)ÔªËØÖÜÆÚ±íÌåÏÖÁËÔªËØÖÜÆÚÂÉ£¬ÔªËØÖÜÆÚÂɵı¾ÖÊÊÇÔ×ÓºËÍâµç×ÓÅŲ¼µÄ__________£¬Çëд³öÔªËØÔÚÔªËØÖÜÆÚ±íÖеÄλÖÃÓëÔªËØÔ×ӽṹµÄ¹Øϵ£º
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£
¡¡ 30£®(05ÉϺ£¾í)
|
|||||||
|
|
||||||
|
|||||||
(1)ÔÚÉÏÃæÔªËØÖÜÆÚ±íÖÐÈ«²¿ÊǽðÊôÔªËصÄÇøÓòΪ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
¡¡¡¡ ¡¡¡¡ (a)A ¡¡¡¡ (b)B ¡¡¡¡ (c)C¡¡ ¡¡¡¡¡¡ (d)D
(2)ÓÐÈËÈÏΪÐγɻ¯ºÏÎï×î¶àµÄÔªËز»ÊÇIVA×åµÄ̼ԪËØ£¬¶øÊÇÁíÒ»ÖÖ¶ÌÖÜÆÚÔªËØ£¬ÇëÄã¸ù¾Ýѧ¹ýµÄ»¯Ñ§ÖªÊ¶ÅжÏÕâÒ»ÔªËØÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(3)ÏÖÓмס¢ÒÒÁ½ÖÖ¶ÌÖÜÆÚÔªËØ£¬ÊÒÎÂÏ£¬¼×ÔªËص¥ÖÊÔÚÀäµÄŨÁòËá»ò¿ÕÆøÖУ¬±íÃ涼Éú³ÉÖÂÃܵÄÑõ»¯Ä¤£¬ÒÒÔªËØÔ×ÓºËÍâMµç×Ó²ãÓëKµç×Ó²ãÉϵĵç×ÓÊýÏàµÈ¡£
¢ÙÓÃÔªËØ·ûºÅ½«¼×¡¢ÒÒÁ½ÔªËØÌîдÔÚÉÏÃæÔªËØÖÜÆÚ±íÖжÔÓ¦µÄλÖá£
¢Ú¼×¡¢ÒÒÁ½ÔªËØÏà±È½Ï£¬½ðÊôÐÔ½ÏÇ¿µÄÊÇ¡¡¡¡¡¡¡¡¡¡ (ÌîÃû³Æ)£¬¿ÉÒÔÑéÖ¤¸Ã½áÂÛµÄʵÑéÊÇ¡¡¡¡¡¡¡¡¡¡ ¡£
¡¡¡¡ ¡¡(a)½«ÔÚ¿ÕÆøÖзÅÖÃÒѾõÄÕâÁ½ÖÖÔªËصĿé×´µ¥ÖÊ·Ö±ð·ÅÈëÈÈË®ÖÐ
(b)½«ÕâÁ½ÖÖÔªËصĵ¥ÖÊ·ÛÄ©·Ö±ðºÍͬŨ¶ÈµÄÑÎËá·´Ó¦
(c)½«ÕâÁ½ÖÖÔªËصĵ¥ÖÊ·ÛÄ©·Ö±ðºÍÈÈË®×÷Ó㬲¢µÎÈë·Ó̪ÈÜÒº
(d)±È½ÏÕâÁ½ÖÖÔªËصÄÆø̬Ç⻯ÎïµÄÎȶ¨ÐÔ
28£® (07È«¹ú¾íI)W¡¢X¡¢YºÍZ¶¼ÊÇÖÜÆÚ±íÖÐÇ°20ºÅÔªËØ£¬ÒÑÖª£º
¢ÙWµÄÑôÀë×ÓºÍYµÄÒõÀë×Ó¾ßÓÐÏàͬµÄºËÍâµç×ÓÅŲ¼£¬ÇÒÄÜÐγÉ×é³ÉΪWYµÄ»¯ºÏÎ
¢ÚYºÍZÊôͬ×åÔªËØ£¬ËüÃÇÄÜÐγÉÁ½ÖÖ³£¼û»¯ºÏÎ
¢ÛXºÍZÊôͬһÖÜÆÚÔªËØ£¬ËüÃÇÄÜÐγÉÁ½ÖÖÆø̬»¯ºÏÎ
¢ÜWºÍXÄÜÐγÉ×é³ÉΪWX2µÄ»¯ºÏÎ
¢ÝXºÍY²»ÔÚͬһÖÜÆÚ£¬ËüÃÇÄÜÐγÉ×é³ÉΪXY2µÄ»¯ºÏÎï¡£
Çë»Ø´ð£º
(1)WÔªËØÊÇ________£»ZÔªËØÊÇ_________¡£
(2)»¯ºÏÎïWYºÍWX2µÄ»¯Ñ§Ê½·Ö±ðÊÇ__________ºÍ___________¡£
(3)YºÍZÐγɵÄÁ½ÖÖ³£¼û»¯ºÏÎïµÄ·Ö×ÓʽÊÇ_________ºÍ_________¡£
(4)д³öXºÍZÐγɵÄÒ»ÖÖÆø̬»¯ºÏÎï¸úWZ·´Ó¦µÄ»¯Ñ§·½³Ìʽ____________________________________¡£
27£®(07º£ÄϾí) ϱíΪԪËØÖÜÆÚ±íµÄÒ»²¿·Ö£¬Çë»Ø´ðÓйØÎÊÌ⣺
|
¡¡ |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
¡¡ |
¡¡ |
¡¡ |
¡¡ |
¢Ù |
¡¡ |
¢Ú |
¡¡ |
|
3 |
¡¡ |
¢Û |
¢Ü |
¢Ý |
¡¡ |
¢Þ |
¢ß |
¢à |
|
4 |
¢á |
¡¡ |
¡¡ |
¡¡ |
¡¡ |
¡¡ |
¢â |
¡¡ |
(1)¢ÝºÍ¢àµÄÔªËØ·ûºÅÊÇ______ºÍ_______£»
(2)±íÖÐ×î»îÆõĽðÊôÊÇ______£¬·Ç½ðÊôÐÔ×îÇ¿µÄÔªËØÊÇ______£»(ÌîдԪËØ·ûºÅ)
(3)±íÖÐÄÜÐγÉÁ½ÐÔÇâÑõ»¯ÎïµÄÔªËØÊÇ_______£¬·Ö±ðд³ö¸ÃÔªËصÄÇâÑõ»¯ÎïÓë¢Þ¡¢¢áµÄ×î¸ß¼ÛÑõ»¯Îï¶ÔӦˮ»¯Îï·´Ó¦µÄ»¯Ñ§·½³Ìʽ£º_______________________________________£¬__________________________________________£»
(4)ÇëÉè¼ÆÒ»¸öʵÑé·½°¸£¬±È½Ï¢ß¡¢¢âµ¥ÖÊÑõ»¯ÐÔµÄÇ¿Èõ£º______________________________________________________________________________¡£
26£®(08Ìì½ò¾í)W¡¢X¡¢Y¡¢ZÊÇÔ×ÓÐòÊýÒÀ´ÎÔö´óµÄͬһ¶ÌͬÆÚÔªËØ£¬W¡¢XÊǽðÊôÔªËØ£¬Y¡¢ZÊǷǽðÊôÔªËØ¡£
(1)W¡¢X¸÷×ÔµÄ×î¸ß¼ÛÑõ»¯Îï¶ÔÓ¦µÄË®»¯Îï¿ÉÒÔ·´Ó¦ÉúÑκÍË®£¬¸Ã·´Ó¦µÄÀë×Ó·½³ÌʽΪ____________________¡£
(2)WÓëY ¿ÉÐγɻ¯ºÏÎïW2Y£¬¸Ã»¯ºÏÎïµÄµç×ÓʽΪ______________¡£
(3)XµÄÏõËáÑÎË®ÈÜ¡¡ÒºÏÔ______ÐÔ£¬ÓÃÀë×Ó·½³Ìʽ½âÊÍÔÒò___________________________________________¡£
(4)YµÄµÍ¼ÛÑõ»¯ÎïͨÈëZµ¥ÖʵÄË®ÈÜÒºÖУ¬·¢Éú·´Ó¦µÄ»¯Ñ§·½³ÌʽΪ____________________________¡£
(5)±È½ÏY¡¢ZÆø̬Ç⻯ÎïµÄÎÈ¡¡¶¨ÐÔ_____£¾_______(Ó÷Ö×Óʽ±íʾ)
(6)W¡¢X¡¢Y¡¢ZËÄÖÖÔªËؼòµ¥Àë×ÓµÄÀë×Ӱ뾶ÓÉ´óµ½Ð¡µÄ˳ÐòÊÇ£º_____£¾_____£¾______£¾______¡£
(7)ZµÄ×î¸ß¼ÛÑõ»¯ÎïΪÎÞÉ«ÒºÌ壬0.25 mol¸ÃÎïÖÊÓëÒ»¶¨Á¿Ë®»ìºÏµÃµ½Ò»ÖÖÏ¡ÈÜ¡¡Òº£¬²¢·Å³öQkJµÄÈÈÁ¿¡£Ð´³ö¸Ã·´Ó¦µÄÈÈ»¯Ñ§·½³Ìʽ£º_______________________¡£
25£®(04½ËÕ¾í)X¡¢YÊÇÔªËØÖÜÆÚ±í¢÷A×åÖеÄÁ½ÖÖÔªËØ¡£ÏÂÁÐÐðÊöÖÐÄÜ˵Ã÷XµÄ·Ç½ðÊôÐÔ±ÈYÇ¿µÄÊÇ(¡¡¡¡ )
¡¡ ¡¡ A£®XÔ×ӵĵç×Ó²ãÊý±ÈYÔ×ӵĵç×Ó²ãÊý¶à
¡¡¡¡ B£®XµÄÇ⻯ÎïµÄ·Ðµã±ÈYµÄÇ⻯ÎïµÄ·ÐµãµÍ
¡¡ ¡¡ C£®XµÄÆø̬Ç⻯Îï±ÈYµÄÆø̬Ç⻯ÎïÎȶ¨
¡¡¡¡ D£®YµÄµ¥ÖÊÄܽ«X´ÓNaXµÄÈÜÒºÖÐÖû»³öÀ´
¿¼µã2¡¡ ÔªËØÍƶÏ
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com