
题目列表(包括答案和解析)
3.由CH3CH3→CH3CH2Cl→CH2=CH2→CH3CH2OH的转化过程中,经过的反应是
A.取代→加成→氧化 B.裂解→取代→消去
C.取代→消去→加成 D.取代→消去→水解
2.下列的晶体中,化学键种类相同,晶体类型也相同的是
A.SO2与SiO2 B.CO2与H2O C.NaCl与HCl D.CCl4与KCl
1.下列说法中正确的是( )
A.处于最低能量的原子叫做基态原子 B.3p2表示3p能级有两个轨道
C.同一原子中,1s、2s、3s电子的能量逐渐减小
D. 同一原子中,2p、3p、4p能级的轨道数依次增多
25.(10分)Ⅰ.有机物A的质谱图和红外光谱图分别如下:

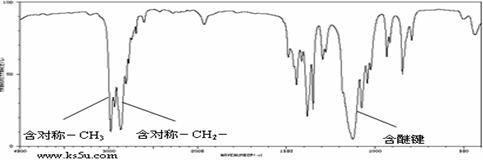
(1)A的结构简式为:___________________________________。
Ⅱ.相对分子质量不超过100的有机物B, 既能与金属钠反应产生无色气体,又能与碳酸钠反应产生无色气体,还可以使溴的四氯化碳溶液褪色。 B完全燃烧只生成CO2和H2O。经分析其含氧元素的质量分数为37.21%。经核磁共振检测发现B的氢谱如下:
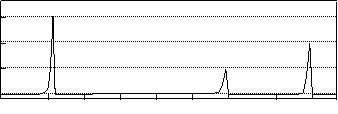
(2)B的结构简式为:___________________________________。
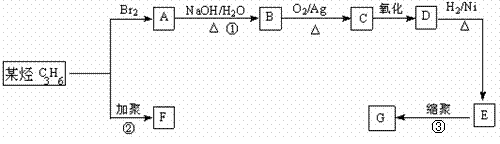 Ⅲ.塑料是常用的合成高分子材料,常用塑料F、G均可由某烃经下列反应得到:
Ⅲ.塑料是常用的合成高分子材料,常用塑料F、G均可由某烃经下列反应得到:
(3)写出反应①的化学方程式:_________ ____________________;
(4)写出反应②的化学方程式:_____ ________________________;
(5)写出反应③的化学方程式:_____ ________________________。
24.(6分)人们对苯的认识有一个不断深化的过程。
(1)1834年德国科学家米希尔里希,通过蒸馏安息香酸(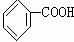 )和石灰的混合物得到液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式:
)和石灰的混合物得到液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式:
。
(2)由于苯的含碳量与乙炔相同,人们认为它是一种不饱和烃,写出C6H6的一种含叁键且无支链链烃的结构简式: 。
苯不能使溴水褪色,性质类似烷烃,任写一个苯发生取代反应的化学方程式:
(3)烷烃中脱水2 mol氢原子形成1 mol双键要吸热,但1,3-环己二烯(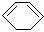 )脱去2 mol氢原子变成苯却放热,可推断苯比1,3-环己二烯 (填稳定或不稳定)。
)脱去2 mol氢原子变成苯却放热,可推断苯比1,3-环己二烯 (填稳定或不稳定)。
 (4)1866年凯库勒(右图)提出了苯的单、双键交替的
(4)1866年凯库勒(右图)提出了苯的单、双键交替的
正六边形平面结构,解释了苯的部分性质,但还有一些问题
尚未解决,它不能解释下列 事实(填入编号)
a.苯不能使溴水褪色 b.苯能与H2发生加成反应
c.溴苯没有同分异构体 d.邻二溴苯只有一种
(5)现代化学认为苯分子碳碳之间的键是 。
23.(10分)多巴是一种用于治疗帕金森氏综合症的药物,它是由C、H、O、N等四种元素形成的有机物,其相对分子质量195<Mr<200,且O的质量分数为32.49%,N的质量分数为7.11%。经分析,药物多巴具有如下性质和结构特征:
①遇FeCl3溶液显紫色;
②1mol多巴和1molHCl或者和3molNaOH均能正好完全反应;
③光谱分析显示,多巴分子中不存在甲基,但含有一个苯环,且苯环上有两个处于邻位的相同取代基A和另一个不与A处于邻位的取代基B;
④两分子多巴缩去两分子水,能形成含有3个六元环的有机物。试回答下列问题:
(1)多巴的摩尔质量是 ,结构简式为 ,
多巴中含有的官能团的名称是 。
(2)多巴有多种同分异构体,请写出一种符合下列条件的同分异构体的结构简式 。
a.官能团的种类和数目、碳链结构均和多巴相同
b.苯环上有两个取代基
c.遇FeCl3溶液不显紫色
(3)两分子多巴缩去两分子水后形成的含有3个六元环的有机物结构简式为 。
22.(8分)(1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准)。
|
烯类化合物 |
相对速率 |
|
(CH3)2C=CHCH3 |
10.4 |
|
CH3CH=CH2 |
2.03 |
|
CH2=CH2 |
1.00 |
|
CH2=CHBr |
0.04 |
依据表中的数据,总结烯类化合物与溴发生加成反应时,反应速率与C=C上取代基的种类、个数的关系① ,
② [来源:高&考%资(源#网]
③
(2)下列化合物与HCl加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是 (填代号)。
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH3 C.CH2=CH2 D.CH2=CHCl
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3(主要产物)+CH3CH2CH2Br(次要产物)
CH2=CHCH2CH3+H2O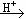 CH3CH(OH)CH2CH3(主要产物)+CH3CH2CH2CH2OH(次要产物)
CH3CH(OH)CH2CH3(主要产物)+CH3CH2CH2CH2OH(次要产物)
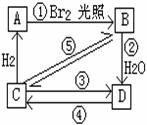 在下图中B、C、D都是相关反应中的主要产物(部分反应条件、试剂被省略),且化合物B中仅有4个碳原子、1个溴原子、9个氢原子。右图框中B的结构简式
在下图中B、C、D都是相关反应中的主要产物(部分反应条件、试剂被省略),且化合物B中仅有4个碳原子、1个溴原子、9个氢原子。右图框中B的结构简式
为 ;属于取代反应的有
(填框图中的序号,下同),属于消去反应的有 ;
写出反应③的化学方程式(只写主要产物,并写反应条件) 。
21. (6分)(1)按构造原理写出33号元素的基态原子的电子排布式: ;写出其元素名称和符号 ,其价电子层排布式为 。
(2)NH3中N原子的杂化轨道类型是 。根据等电子体原理,写出一种NH4+是等电子体的微粒的化学式 。N与O同属第二周期,N的第一电离能比O大的原因是 。
20.按电子排布,可把周期表里的元素划分成5个区,以下元素属于P区的是: ( )
A. Fe B. Mg C. P D. La
19.下列关于能层与能级的说法中正确的是: ( )
A.原子核外电子的每一个能层最多可容纳的电子数为2n2
B.任一能层的能级总是从s能级开始,而且能级数等于该能层序数
C.同是s能级,在不同的能层中所能容纳的最多电子数是不相同的
D.1个原子轨道里最多只能容纳2个电子,但自旋方向相同。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com