
题目列表(包括答案和解析)
11、Na2S2O3溶液跟稀H2SO4反应的化学方程式为:
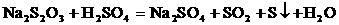 下列各组实验中,溶液中最先变浑浊的是
下列各组实验中,溶液中最先变浑浊的是
|
|
反应 温度℃ |
反 应 物 |
H2O |
|||
|
Na2S2O3 |
H2SO4 |
V(mL) |
||||
|
v(mL) |
c(mol×L-1) |
v(mL) |
c(mol×L-1) |
|||
|
A |
10 |
5 |
0.1 |
10 |
0.1 |
5 |
|
B |
10 |
5 |
0.1 |
5 |
0.1 |
10 |
|
C |
30 |
5 |
0.1 |
5 |
0.1 |
10 |
|
D |
30 |
5 |
0.2 |
5 |
0.2 |
10 |
10、在同温同压下,下列各组热化学方程式中,Q1>Q2的是( )
A. 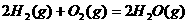
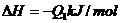
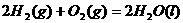
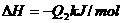
B. 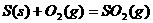
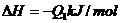
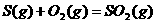
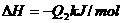
C. 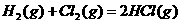
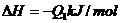
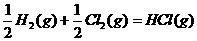
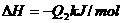
D. 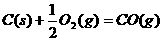
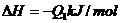
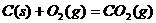
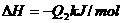
9、 C(s) + H2O(g) == CO(g) + H2(g); △H = +131.3 KJ/mol。它表示
A.碳与水反应吸收131.3 KJ的热量
B.1mol固态焦炭与1mol水蒸气反应产生一氧化碳和氢气,吸收131.3 KJ的热量
C.1mol碳和1mol水反应吸收131.3 KJ的热量
D.固态碳和气态水各1mol反应,放出131.3 KJ的热量
8、已知CH4(g)+2O2(g)== CO2(g)+2H2O(l); ΔH1=–Q1kJ·mol-1 ,
2H2(g)+O2(g)=2H2O(g); △H2=–Q2 kJ·mol-1 ,
H2O(l)=H2O(g); △H3= Q3 kJ·mol-1。
取体积比4∶1的甲烷和氢气的混合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为( )
A. 0.4Q1+0.1Q3 +0.1 Q2 B. 0.4 Q1+0.05 Q2+0.1 Q3
C. 0.4 Q1+0.1 Q3-0.05 Q2 D. ―0.4 Q1―0.05 Q2―0.1 Q3
7、已知在25℃,101kPa下1g C8H18(辛烷液体)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是( )
A C8H18(l)+ 25/2O2(g)=8CO2(g)+9H2O(g)△H=–48.40kJ/mol
B C8H18(l)+ 25/2O2(g)=8CO2(g)+9H2O(l)△H=–-5518kJ/mol
C C8H18(l)+ 25/2O2(g)=8CO2(g)+9H2O(g)△H=+5518kJ/mol
D C8H18(l)+ 25/2O2(g)=8CO2(g)+9H2O(l)△H=+48.40kJ/mol
6、将4molA气体和2molB气体在2L的容器中混合并在一定的条件下发生如下反应,2A(g)+B(g)=2C(g),若经2s后测得C的浓度为0.6mol.L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3mol/(L.s)
②用物质B表示的反应的平均速率为0.6mol/(L.s)
③2s时物质A的转化率为70%,
④2s时物质B的浓度为0.7mol/L , 其中正确的是( )
A.①③ B.①④ C.②③ D.③④
5、下列关于化学反应速率的说法,不正确的是( )
A、化学反应速率是衡量化学反应进行快慢程度的物理量
B、单位时间内某物质的浓度变化越大,则该物质反应就越快
C、化学反应速率可以用单位时间内生成某物质的质量的多少来表示
D、化学反应速率常用单位有mol·L-1·s-1和mol·L-1·min-1
4、某反应X+3Y=2Z+2P在甲、乙、丙、丁四种不同条件下测得的反应速率为:
甲: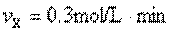 乙:
乙: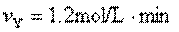
丙: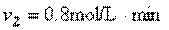 丁:
丁: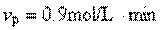 则反应进行最快的是( )
则反应进行最快的是( )
A.甲 B.乙 C.丙 D.丁
3、在10L 密闭容器里发生: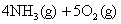

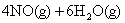 反应半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率
反应半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率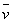 可表示为
可表示为
A.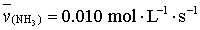 B.
B.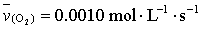
C.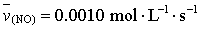 D.
D.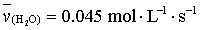
2、在一定条件下,在体积为VL的密闭容器中发生反应:mA + nB=pC。t秒末,A减少了1 mol,B减少了1.25 mol,C增加了0.5 mol。则m ∶ n ∶ p应为( )
A.4∶ 5∶ 2 B.2∶ 5∶ 4
C.1∶ 3∶ 2 D.3∶ 2∶ 1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com