
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
17°¢ƒÐ’˝»∑±Ì 本¡–∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «
°° A£ÆΩ ÙÕ≠»Ð”⁄FeCl3»Ð“∫÷–£∫Cu + Fe3+ = Cu2+ + Fe2+
°° B£ÆúÀ·–ø»Ð”⁄œ°œıÀ·÷–£∫CO32-+ 2H+ = H2O + CO2°¸
°° C£Æ±Ω∑”ƒ∆ÀƻГ∫÷–Õ®»Î…Ÿ¡øCO2£∫2C6H5O- + CO2 + H2O°˙2C6H5OH + CO32-
°° D£Æ…Ÿ¡øCl2Õ®»ÎFeI2»Ð“∫÷–£∫Cl2+ 2I- = 2C1-+ I2
16°¢≥£Œ¬œ¬£¨œ¬¡–∏˜◊È¿Î◊”‘⁄÷∏∂®»Ð“∫÷–ƒÐ¥Û¡øπ≤¥Êµƒ «
°° A£ÆpH=1µƒ»Ð“∫÷–£∫Fe2+°¢NO3-°¢SO42-°¢Na+
°° B£Æ”…ÀƵÁ¿Îµƒc(H+)=1°¡10-14mol°§L-1µƒ»Ð“∫÷–£∫Ca2+°¢K+°¢Cl-°¢HCO3-
°° C£Æc(H+)/c(OH-)=1012µƒ»Ð“∫÷–£∫NH4+°¢Al3+°¢NO3-°¢Cl-
°° D£Æc(Fe3+)=0.1mol°§L-1µƒ»Ð“∫÷–£∫K+°¢ClO-°¢SO42-°¢SCN-
15°¢»Ù(NH4)2SO4‘⁄«ø»» ±∑÷Ω‚µƒ≤˙ŒÔ «SO2°¢N2°¢NH3∫ÕH2O£¨‘Ú∏√∑¥”¶÷–ªØ∫œº€∑¢…˙±‰ªØ∫ÕŒ¥∑¢…˙±‰ªØµƒN‘≠◊” ˝÷Ʊ»Œ™
°° A£Æ1:4°°°°°°°°°°°°°°°° B.°° 1:2°°°°°°°°°°°°°°°° C.°° 2:1°°°°°°°°°°°° D. 4:1
14°¢œ¬√Êæ˘ «’˝∂°ÕȔΗı∆¯∑¥”¶µƒ»»ªØ—ß∑Ω≥à Ω(25°Ê£¨101kPa)£∫
¢ŸC4H10(g)+13/2O2(g)=4CO2(g)+5H2O(l)£ª¶§H=-2878kJ/mol
¢⁄C4H10(g)+13/2O2(g)=4CO2(g)+5H2O(g)£ª¶§H=-2658kJ/mol
¢€C4H10(g)+9/2O2(g)=4CO(g)+5H2O(l)£ª¶§H=-1746kJ/mol
¢ÐC4H10(g)+9/2O2(g)=4CO(g)+5H2O(g)£ª¶§H=-1526kJ/mol
”…¥À≈–∂œ£¨’˝∂°Õȵƒ»º…’»» «
°° A.-2878kJ/mol°°°° B. -2658kJ/mol°°°° C. -1746kJ/mol°°°° D. -1526kJ/mol
13°¢Ω´±•∫ÕFeCl3»Ð“∫∑÷±µŒ»Îœ¬ ˆ“∫ÃÂ÷–£¨ƒÐ–Œ≥…Ω∫õƒ «
°° A°° ¿‰ÀÆ°°°° B°° ∑–ÀÆ°°°° C°° NaOH≈®»Ð“∫°°°° D°° NaCl≈®»Ð“∫
12°¢œ¬√Êπÿ”⁄SiO2æßÃÂÕ¯◊¥Ω·π𵃖 ˆ’˝»∑µƒ «
°° A£Æ√ø∏ˆSi‘≠◊”÷ÐŒßΩ·∫œ2∏ˆO‘≠◊”°° B£ÆSiO2 «∆‰∑÷◊” Ω
°° C£Æ1molSiO2∫¨2molSi−Oº¸°°°°°°°°°° D£Æ◊Ó–°µƒª∑…œ£¨”–6∏ˆSi‘≠◊”∫Õ6∏ˆO‘≠◊”
11°¢œ¬Õº Œ™÷±¡˜µÁ‘¥£¨
Œ™÷±¡˜µÁ‘¥£¨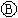 Œ™Ω˛Õ∏±•
Œ™Ω˛Õ∏±• ∫Õ¬»ªØƒ∆»Ð“∫∫Õ∑”Ù ‘“∫µƒ¬À÷Ω£¨
∫Õ¬»ªØƒ∆»Ð“∫∫Õ∑”Ù ‘“∫µƒ¬À÷Ω£¨ Œ™µÁ∂∆≤€£ÆΩ”Õ®µÁ¬∑∫Û∑¢œ÷
Œ™µÁ∂∆≤€£ÆΩ”Õ®µÁ¬∑∫Û∑¢œ÷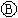 …œµƒcµ„œ‘∫Ï…´£ÆŒ™ µœ÷Ã˙
…œµƒcµ„œ‘∫Ï…´£ÆŒ™ µœ÷Ã˙ …œ∂∆Õ≠£¨Ω”Õ®
…œ∂∆Õ≠£¨Ω”Õ®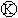 ∫Û£¨ πc°¢d¡Ωµ„∂ì∑£Æœ¬¡–– ˆ’˝»∑µƒ «(°° ∏þ°Óøº°·◊ °‚‘¥*Õ¯°°
)
∫Û£¨ πc°¢d¡Ωµ„∂ì∑£Æœ¬¡–– ˆ’˝»∑µƒ «(°° ∏þ°Óøº°·◊ °‚‘¥*Õ¯°°
)
°° A£ÆaŒ™÷±¡˜µÁ‘¥µƒ∏∫º´°°°° B£Æcº´∑¢…˙µƒ∑¥”¶Œ™2H++2e£≠£ΩH2°¸
°° C£ÆfµÁº´Œ™Õ≠∞°°°°°°°°°° D£Æeº´∑¢…˙ªπ‘≠∑¥”¶
10°¢œ¬¡–Àµ∑®’˝»∑µƒ «
°° A£Æ‘≠◊”◊ÓÕ‚≤„µÁ◊” ˝Œ™2µƒ‘™Àÿ“ª∂®¥¶”⁄÷Ð∆⁄±Ì¢ÚA◊°° °°
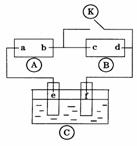 °° B£Æ÷˜◊‘™ÀÿX°¢YƒÐ–Œ≥…XY2–ÕªØ∫œŒÔ£¨‘ÚX”ÎYµƒ‘≠◊”–Ú ˝÷Æ≤Óø…ƒÐŒ™2ªÚ5°°
°° B£Æ÷˜◊‘™ÀÿX°¢YƒÐ–Œ≥…XY2–ÕªØ∫œŒÔ£¨‘ÚX”ÎYµƒ‘≠◊”–Ú ˝÷Æ≤Óø…ƒÐŒ™2ªÚ5°°
°° C£Æ¬»ªØ«‚µƒ∑–µ„±»∑˙ªØ«‚µƒ∑–µ„∏þ
°° D£ÆÕ¨÷˜◊‘™Àÿ–Œ≥…µƒ—ıªØŒÔµƒæßÿý–Õæ˘œýÕ¨
9°¢”–X°¢Y°¢Z°¢W°¢MŒÂ÷÷∂Ã÷Ð∆⁄‘™Àÿ£¨∆‰÷–X°¢Y°¢Z°¢WÕ¨÷Ð∆⁄£¨ Z°¢MÕ¨÷˜◊£ª X+”ÎM2-æþ”–œýÕ¨µƒµÁ◊”≤„Ω·ππ£ª¿Î◊”∞Îæ∂£∫Z2-£æW-£ªYµƒµ•÷ æßû€µ„∏þ°¢”≤∂»¥Û£¨ «“ª÷÷÷ÿ“™µƒ∞εºÃÂ≤ƒ¡œ°£œ¬¡–Àµ∑®÷–£¨’˝»∑µƒ «
°° A.X°¢M¡Ω÷÷‘™Àÿ÷ªƒÐ–Œ≥…X2M–ÕªØ∫œŒÔ
°° B.”…”⁄W°¢Z°¢M‘™Àÿµƒ«‚∆¯ªØŒÔœý∂‘∑÷◊”÷ ¡ø“¿¥Œºı–°£¨À˘“‘∆‰∑–µ„“¿¥ŒΩµµÕ
°° C.‘™ÀÿY°¢Z°¢Wµƒµ•÷ æßàٔ⁄Õ¨÷÷¿ý–ÕµƒæßÃÂ
°° D.‘™ÀÿW∫ÕMµƒƒ≥–©µ•÷ ø…◊˜Œ™ÀÆ¥¶¿Ì÷–µƒœ˚∂溡
8°¢ƒÐº¯±MgI2, AgNO3, Na2CO3,NaAlO2£¨Àƒ÷÷»Ð“∫µƒ ‘º¡ «
°° A. HNO3°°°° B.KOH°°°°°° C. BaCl2°°°° D. NaClO°°
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com