
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
6£®ĻĀĮŠ×ö·ØÕżČ·µÄŹĒ””””””””””””””””””””””””””””””””””””””””””””””
A£®ĪŖĮĖŹ¹»šĶČ³¦ŃÕÉ«øüĻŹŗģ£¬æɶą¼ÓŅ»Š©ŃĒĻõĖįÄĘ
B£®ĪŖĮĖŹ¹Ó¤¶ł¶ŌŹ³Ę·ÓŠÅØŗńŠĖȤ£¬ĪŅĆĒæÉŅŌŌŚÓ¤¶łŹ³Ę·ÖŠ¼ÓÉŁĮæ×ÅÉ«¼Į
C£®Ź³ŃĪ¼ÓµāŹĒ·ĄÖ¹ČĖĢåȱµā¶ų¼ÓµÄÓŖŃųĒæ»Æ¼Į£¬ÄÜŌ¤·ĄµŲ·½ŠŌ¼×דĻŁÖדó
D£®ĪŖ±£Ö¤ČĖĢåĖłŠč×ć¹»µ°°×ÖŹĪŅĆĒŅŖ¶ą³ŌČā£¬ÉŁ³ŌŹß²ĖŗĶĖ®¹ū
5£®ĀČĘųÓŠ¶¾£¬Ōų±»·ØĪ÷Ė¹ÖĘ³É¶¾ĘųµÆÓĆÓŚĒÖĀŌÕ½Õł”£µ±·¢ÉśĀČĘųŠ¹Ā©Ź±£¬Ķس£æÉÓƵķĄÓł·½·ØŹĒ”””” ””””””””””””””””””””””””””””””””””””””””””””””””””””
””A£®ČĖ”¢ŠóÓ¦¶ćµ½µĶĶŻµÄµŲ·½”” ””””B£®ČĖ”¢ŠóÓ¦ĻņĖ³·ēµÄµŲ·½Č„
””C£®ČĖ”¢ŠóÓ¦¶ąŅū¶¹½¬ŗĶÅ£Čé”” ””””D£®æÉÓĆ·ŹŌķĖ®»ņÄņ½žŹŖČķ²¼ĆÉĆę
4£®ĪŖĮĖ±£»¤³ōŃõ²ć£¬æɲÉČ”µÄÓŠŠ§“ėŹ©ŹĒ””””””””””””””””””””””””””””
A£®¼õÉŁ¶žŃõ»ÆĮņµÄÅÅ·Å”””””” ””””B£®¼õÉŁŗ¬Ē¦·ĻĘųµÄÅÅ·Å
C£®¼õÉŁ·śĀČ“śĢžµÄÅÅ·Å”””””” ””””D£®¼õÉŁ¶žŃõ»ÆĢ¼µÄÅÅ·Å
3£®ŌŚĪŅĆĒµÄČÕ³£Éś»īÖŠ³öĻÖĮĖ”°¼ÓµāŹ³ŃĪ”±”¢”°ŌöĢś½“ÓĶ”±”¢”°øßøĘÅ£ÄĢ”±”¢”°ø»Īų²čŅ¶”±”¢”°ŗ¬·śŃĄøą”±µČÉĢĘ·”£ÕāĄļµÄµā”¢Ģś”¢øĘ”¢Īų”¢·śÓ¦Ąķ½āĪŖ””””””””””””
A£®ŌŖĖŲ”””””” B£®µ„ÖŹ”””””” C£®·Ö×Ó”””””””” D£®Ńõ»ÆĪļ
2£®ŹŅÄŚæÕĘųĪŪČ¾µÄÖ÷ŅŖĄ“Ō“Ö®Ņ»ŹĒÅŻÄ¾ųŌµĖÜĮĻ”¢»ÆĻĖµŲĢŗ”¢Źé±Ø”¢ÓĶĘįµČ²»Ķ¬³Ģ¶ČŹĶ·Å³öµÄĘųĢ壬øĆĘųĢåŹĒ”””” ””””””””””””””””””””””””””””””””””””””
A£®¼×Ķé”” ””””B£®¼×Č©”” ””””C£®Ņ»Ńõ»ÆĢ¼”””” D£®¶žŃõ»ÆĢ¼
1£®ÄæĒ°ĪŅ¹śŠķ¶ą³ĒŹŠŗĶµŲĒų¶ØĘŚ¹«²¼æÕĘųÖŹĮæ±Øøę£¬ŌŚæÕĘųÖŹĮæ±ØøęÖŠ£¬Ņ»°ć²»Éę¼°µÄŹĒ
A£®SO2”””””” B£®NO2”””””” C£®CO2”””” ””””D£®æÉĪüČėæÅĮ£Īļ
24£®(10·Ö)A-GŹĒ֊ѧ»Æѧ³£¼ūµÄĘßÖÖĪļÖŹ£¬¾łÓɶĢÖÜĘŚŌŖĖŲ×é³É£¬³£ĪĀ”¢³£Ń¹ĻĀ CĪŖĪŽÉ«ŅŗĢ壬D”¢EĪŖĘųĢåµ„ÖŹ£¬BĪŖ½šŹōµ„ÖŹ”£A-GæÉ·¢ÉśČēĻĀ×Ŗ»Æ£ŗ
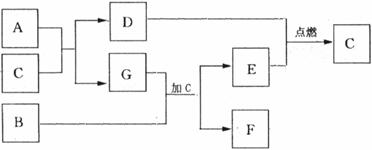
”””” ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ
”””” (1)CÖŠŗ¬ÓŠµÄ»Æѧ¼üĄąŠĶ__________£¬GµÄµē×ÓŹ½__________”£
”””” (2) 5.4gBÓėGĶźČ«·“Ó¦£¬×ŖŅʵĵē×ÓŹżÄæŹĒ__________”£
(3)ĻņFµÄĖ®ČÜŅŗÖŠĶØČė×ćĮæµÄ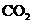 ĘųĢ壬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£ŗ
ĘųĢ壬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£ŗ
________________________________________________________________________
(4)8gDµ„ÖŹĶźČ«Č¼ÉÕÉś³ÉĘųĢ¬C£¬·Å³ö967£®2kJČČĮ棬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ŹĒ£ŗ
________________________________________________________________________
2010-2011ѧğµŚŅ»Ń§ĘŚĘŚÖŠæ¼ŹŌø߶ž
23£®(14·Ö)»Æ¹¤Éś²śÖŠ³£³£ÓƵ½”°ČżĖį”±”°Į½¼ī”±£¬ĘäÖŠ£¬”°ČżĖį”±ŹĒÖøŃĪĖį”¢ĮņĖįŗĶĻõĖį£¬”°Į½¼ī”±ŹĒÖøÉÕ¼īŗĶ“æ¼ī”£
(1)“ÓĪļÖŹ·ÖĄąŃ§µÄ½Ē¶Čæ“£¬·ÖĄą²»Ē”µ±µÄŅ»ÖÖĪļÖŹŹĒ_________”£
(2)”°ČżĖį”±Óė”°Į½¼ī”±Ö®¼ä¾łæÉ·¢Éś·“Ó¦£¬æÉŅŌŠ“³öŗܶą»Æѧ·½³ĢŹ½£¬¶ų·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹżÄæŅŖÉŁµĆ¶ą£¬ĒėŠ“³öĻĀĮŠĄė×Ó·½³ĢŹ½”£
¢ŁÉÕ¼īÓė”°ČżĖį”±·“Ó¦______________________”£
 ¢Ś½«ÉŁĮæµÄ”°ČżĖį”±ÓėµĪČė“æ¼īČÜŅŗÖŠ
______________________£»
¢Ś½«ÉŁĮæµÄ”°ČżĖį”±ÓėµĪČė“æ¼īČÜŅŗÖŠ
______________________£»
(3)”°ČżĖį”±³£ÓĆÓŚČܽā½šŹō»ņ½šŹōŃõ»ÆĪļ£¬Š“³öĻĀĮŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½”£
¢Ł½šŹōĢśÓėĻ”ĮņĖį·“Ó¦______________________________”£
¢Ś½šŹōĶÓėÅØĮņĖį¹²ČČ_____________________________”£
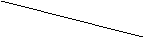
(4)ÓÉ”°Į½¼ī”±×é³ÉµÄ»ģŗĻĪļČōøÉ£¬½«ĖüČÜÓŚĖ®Åä³ÉČÜŅŗ£¬ĻņČÜŅŗÖŠµĪ¼Ó0.1mol”¤L-1Ļ”ŃĪĖį”£¼ÓČėŃĪĖįµÄĢå»żŗĶÉś³ÉCO2µÄĪļÖŹµÄĮæµÄ¹ŲĻµČēÓŅĶ¼±ķŹ¾”£
ŌņŌ»ģŗĻĪļÖŠŗ¬NaOH_____g£¬Na2CO3 ______g”£
22£®(20·Ö)ijĶ¬Ń§ŌŚÓĆĻ”ĮņĖįÓėŠæÖĘČ”ĒāĘųµÄŹµŃéÖŠ£¬·¢ĻÖ¼ÓČėÉŁĮæĮņĖįĶČÜŅŗæɼÓæģĒāĘųµÄÉś³ÉĖŁĀŹ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ÉĻŹöŹµŃéÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ÓŠ
___________________________Ӣ_______________________________
(2)ĮņĖįĶČÜŅŗæÉŅŌ¼ÓæģĒāĘųÉś³ÉĖŁĀŹµÄŌŅņŹĒ________________________________
______________________
(3)ŅŖ¼ÓæģÉĻŹöŹµŃéÖŠĘųĢå²śÉśµÄĖŁĀŹ£¬»¹æɲÉČ”µÄ“ėŹ©ÓŠ______________________
_________________________________________(ČĪŅā“šŅ»ÖÖ)”£
(4)ĪŖĮĖ½ųŅ»²½ŃŠ¾æĮņĖįĶµÄĮæ¶ŌĒāĘųÉś³ÉĖŁĀŹµÄÓ°Ļģ£¬øĆĶ¬Ń§Éč¼ĘĮĖČēĻĀŅ»ĻµĮŠŹµŃ锣½«±ķÖŠĖłøųµÄ»ģŗĻČÜŅŗ·Ö±š¼ÓČėµ½6øöŹ¢ÓŠ¹żĮæZnĮ£µÄ·“Ó¦ĘæÖŠ£¬ŹÕ¼Æ²śÉśµÄĘųĢ唣¼ĒĀ¼»ńµĆĻąĶ¬Ģå»żµÄĘųĢåĖłŠčŹ±¼ä”£
 ””””””””
ŹµŃé ””””””””
ŹµŃé»ģŗĻČÜŅŗ |
A |
B |
C |
D |
E |
F |
|
4 mol”¤L£1 H2SO4/mL |
30 |
V1 |
V2 |
V3 |
V4 |
V5 |
|
±„ŗĶCuSO4ČÜŅŗ/mL |
0 |
0.5 |
2.5 |
5 |
V6 |
20 |
|
H2O/mL |
V7 |
V8 |
V9 |
V10 |
10 |
0 |
¢ŁĒėĶź³É“ĖŹµŃéÉč¼Ę£¬ĘäÖŠ£ŗV1£½______£¬V6£½______£¬V9£½______”£
¢Ś·“Ó¦Ņ»¶ĪŹ±¼äŗó£¬AÖŠ½šŹō±ķĆęŹĒ³Ź_______É«£¬EÖŠµÄ½šŹō±ķĆę³Ź_______É«”£
¢ŪøĆĶ¬Ń§×īŗóµĆ³öµÄ½įĀŪĪŖ£ŗµ±¼ÓČėÉŁĮæCuSO4ČÜŅŗŹ±£¬Éś³ÉĒāĘųµÄĖŁĀŹ»į“ó“óĢįøߣ»µ«µ±¼ÓČėµÄCuSO4ČÜŅŗ³¬¹żŅ»¶ØĮæŹ±£¬Éś³ÉĒāĘųµÄĖŁĀŹ·“¶ų»įĻĀ½µ”£
Ēė·ÖĪöµ±¼ÓČėµÄCuSO4ČÜŅŗ³¬¹żŅ»¶ØĮæŹ±£¬ĒāĘųÉś³ÉĖŁĀŹĻĀ½µµÄÖ÷ŅŖŌŅņŹĒ______
_________________________________________ӣ
21£®(10·Ö)ij»ÆѧŠĖȤŠ”×éµÄѧĻ°Ā±ĖŲŅŌŗó£¬×öĮĖĻĀĮŠŹµŃé£ŗ
ĻņµĪÓŠµķ·ŪµÄKIČÜŅŗÖŠµĪ¼ÓĀČĖ®£¬ČÜŅŗ³öĻÖĄ¶É«£»¼ĢŠųµĪ¼ÓĀČĖ®£¬ČÜŅŗĄ¶É«Öš½„±äĒ³×īŗó±äĪŖĪŽÉ«”£
(1)µĪ¼ÓĀČĖ®Ź±ČÜŅŗ³öĻÖĄ¶É«µÄĄė×Ó·½³ĢŹ½ŹĒ____________________________”£
(2)¶ŌÓŚ¼ĢŠųµĪ¼ÓĀČĖ®£¬ČÜŅŗĄ¶É«Öš½„±äĒ³×īŗó±äĪŖĪŽÉ«µÄŌŅņ£¬ĒėĶź³ÉŅŌĻĀŹµŃéĢ½¾æ¹ż³Ģ”£
¢ń”¢Ģį³ö¼ŁÉč
¼ŁÉč1£ŗI2±»Ńõ»Æ”£
¼ŁÉč2£ŗµķ·ŪŗĶI2¶¼±»Ńõ»Æ”£
¼ŁÉč3£ŗ__________”£
¢ņ”¢ŹµŃéÉč¼Ę
|
ŹµŃé²½Öč |
Ō¤ĘŚĻÖĻóÓė½įĀŪ |
|
”” |
”” |
|
”” |
”” |
¢ó”¢ĪŹĢāÓėĢÖĀŪ
ŹµŃé±ķĆ÷I2±»Ńõ»ÆŹĒĄ¶É«ĻūŹ§µÄŌŅņ£¬»Æѧ·½³ĢŹ½ŹĒ£ŗ_____+____+____== HIO3+_____”£
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com