
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
5ЃЎдквЛИіУмБеЩеЦПжаЃЌдк25ЁцЪБДцдкзХЦНКтЃК2NO2 N2O4ЁЁ
ЁїH<0ЃЌШчАбЩеЦПжУгк100ЁцЕФЗаЫЎжаЃЌдђЯТСаМИЯюаджЪжаЃКЂйбеЩЋЁЁ ЂкЦНОљЗжзгСПЁЁ ЂлжЪСПЁЁ ЂмбЙЧПЁЁ ЂнУмЖШЃЌЦфжаВЛЛсИФБфЕФЪЧ(ЁЁ )
N2O4ЁЁ
ЁїH<0ЃЌШчАбЩеЦПжУгк100ЁцЕФЗаЫЎжаЃЌдђЯТСаМИЯюаджЪжаЃКЂйбеЩЋЁЁ ЂкЦНОљЗжзгСПЁЁ ЂлжЪСПЁЁ ЂмбЙЧПЁЁ ЂнУмЖШЃЌЦфжаВЛЛсИФБфЕФЪЧ(ЁЁ )
AЃЎЂйКЭЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂлКЭЂнЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂмКЭЂнЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂкКЭЂм
4ЃЎдквбОДІгкЛЏбЇЦНКтзДЬЌЕФЬхЯЕжаЃЌШчЙћЯТСаСПЗЂЩњБфЛЏЃЌЦфжавЛЖЈФмБэУїЦНКтвЦЖЏЕФЪЧ
AЃЎЗДгІЛьКЯЮяЕФХЈЖШЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЗДгІЮяЕФзЊЛЏТЪ
CЃЎе§ЁЂФцЗДгІЫйТЪЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЗДгІЛьКЯЮяЕФбЙЧП
3ЃЎвбжЊ2NO(g) + O2(g) 2NO2(g)ЕФЦНКтГЃЪ§ЮЊK1ЃЌ2NO2(g)
2NO2(g)ЕФЦНКтГЃЪ§ЮЊK1ЃЌ2NO2(g) N2O4(g)ЕФЦНКтГЃЪ§ЮЊK2ЃЌдђЗДгІ2NO(g) + O2(g)
N2O4(g)ЕФЦНКтГЃЪ§ЮЊK2ЃЌдђЗДгІ2NO(g) + O2(g) N2O4(g)ЕФЦНКтГЃЪ§KЪЧ(ЁЁ )
N2O4(g)ЕФЦНКтГЃЪ§KЪЧ(ЁЁ )
AЃЎK1+K2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎK1/K2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎK1ЁСK2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎK1ЃK2
2ЃЎвбжЊH2(g)+Br2(l)=2HBr(g)ЃЛЁїH=Ѓ72KJ/molЃЌеєЗЂ1mol Br2(l)ашвЊЮќЪеЕФФмСПЮЊ30KJЃЌЦфЫћЕФЯрЙиЪ§ОнШчЯТБэЃК

дђБэжаaЮЊ
AЃЎ404ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ260 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎ230ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ200
1ЃЎвбжЊШмвКжаДцдкCr2O72-
+ H2O 2CrO42- + 2H+ЕФЦНКтЃЌЦфжаCr2O72-ГЪГШЩЋЃЌCrO42-ГЪЛЦЩЋЃЌЯђИУЦНКтЬхЯЕжаЕЮМгБЅКЭNaOHШмвКЪБЃЌбеЩЋЕФБфЛЏЧщПіЪЧ(ЁЁ )
2CrO42- + 2H+ЕФЦНКтЃЌЦфжаCr2O72-ГЪГШЩЋЃЌCrO42-ГЪЛЦЩЋЃЌЯђИУЦНКтЬхЯЕжаЕЮМгБЅКЭNaOHШмвКЪБЃЌбеЩЋЕФБфЛЏЧщПіЪЧ(ЁЁ )
AЃЎГШЩЋМгЩюЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЛЦЩЋМгЩюЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎбеЩЋВЛБфЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎбеЩЋЭЪШЅ
29. 25.00mlЮДжЊХЈЖШЕФHNO3ШмвКгы24.18ml 0.6120mol/LЕФKOHШмвКЧЁКУЭъШЋжаКЭЃЌ
ЪдМЦЫуHNO3ЕФЮяжЪЕФСПХЈЖШЁЃ25.00mlетжжШмвКРяКЌHNO3ЕФжЪСПЪЧЖрЩйПЫЃП
2010ЈD2011бЇФъЖШЕквЛбЇЦкЦкжаПМЪд
28ЃЎЪдЪіЪЕбщЪвжЄУїХЈЖШЖдЛЏбЇЦНКтгАЯьЪЕбщЙ§ГЬЁЃ
ЁЁ ЁЁЗДгІдРэ(гУРызгЗНГЬЪНБэЪО)ЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ ЁЁВйзїВНжшМАЯжЯѓЃК
|
ЪЕбщВНжш |
ЪЕбщЯжЯѓ |
НтЪЭКЭНсТл |
|
(1)дкаЁЩеБжаМгШы0.1mol/LFeCl3ШмвК2mLКЭ0.1mol/LNH4SCNШмвК2mL.ЁЃМгЫЎ10mlЃЌЛьдШКѓЗжзАгк3жЇЪдЙмжаЁЃ |
ЗДгІКѓаЮГЩКьЩЋШмвКЁЃ |
ЁЁ |
|
(2) ЁЁ ЁЁ ЁЁ |
ЁЁ |
ЁЁ |
|
(3) ЁЁ ЁЁ ЁЁ |
ЁЁ |
ЁЁ |
|
(4)БШНЯЩЯЪіШ§жЇЪдЙмЕФбеЩЋЁЃ ЁЁ ЁЁ ЁЁ |
ЁЁ |
ЁЁ |
ЁЁ
27ЃЎЪЕбщЪвГЃгУБЅКЭNaNO2КЭNH4ClШмвКЗДгІжЦШЁДПОЛЕФЕЊЦјЁЃЗДгІЪНЮЊЃК
NaNO2 + NH4Cl == NaCl + N2Ёќ + 2H2OЁќ + QЃЌЪЕбщзАжУШчЯТЭМЪОЃЌЪдЛиД№ЃК
 ЁЁ
ЁЁ
(1)зАжУжаAВПЗжЕФЗжвКТЉЖЗгыеєСѓЩеЦПжЎМфСЌНгЕФЕМЙмЫљЦ№ЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)BВПЗжЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ ЁЁЁЁИЩдяЙмФкзАга_____ЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ____ ЁЃ
(3)МгШШЧАБиаыНјаавЛИіВйзїВНОлЪЧЃК________________ЃЛМгШШЦЌПЬКѓЃЌ
МДгІвЦШЅОЦОЋЕЦвдЗРЗДгІЮяГхГіЃЌЦфдвђЪЧЃК__ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ____ ЁЃ
(4)ЪеМЏN2ЧАБиаыНјааЕФВНОлЪЧЃК_______ЁЁЁЁЁЁЁЁ _____ ЃЛ
ЪеМЏN2зюЪЪвЫЕФЗНЗЈЪЧ_____ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ____ ЁЃ
26. МиЪЧ-жжЛюЦУЕФН№ЪєЃЌЙЄвЕЩЯЭЈГЃгУН№ЪєФЦКЭТШЛЏМидкИпЮТЯТЗДгІжЦШЁЁЃИУЗДгІЮЊЃК
Na(l)+KCl(l) NaCl(l)+K(g)ЃЌ(е§ЗДгІЮќШШ)
NaCl(l)+K(g)ЃЌ(е§ЗДгІЮќШШ)
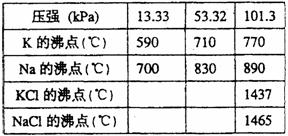 Ђй дкГЃбЙЯТН№ЪєМизЊБфЮЊЦјЬЌДг
Ђй дкГЃбЙЯТН№ЪєМизЊБфЮЊЦјЬЌДг
ЗДгІЛьКЯЮяжаЗжРыЕФзюЕЭЮТЖШ
дМЮЊЁЁЁЁЁЁЁЁ ЃЌЖјЗДгІЕФзюИп
ЮТЖШгІЕЭгкЁЁЁЁЁЁ ЁЃ
Ђк дкжЦШЁМиЕФЙ§ГЬжаЃЌЮЊСЫЬсИпдСЯЕФзЊЛЏТЪПЩвдВЩШЁЕФДыЪЉЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
25. бРГнБэУцЪмЕНвЛВугВЕФЁЂзщГЩЮЊCa5(PO4)3OHЕФЮяжЪЕФБЃЛЄЃЌЫќдкЭйвКжаДцдкЯТ
СаЦНКтЃКCa5(PO4)3OH 5Ca2++3PO43Ѓ+OHЃЃЌНјЪГКѓЯИОњКЭУИзїгУгкЪГЮяВњ
5Ca2++3PO43Ѓ+OHЃЃЌНјЪГКѓЯИОњКЭУИзїгУгкЪГЮяВњ
ЩњгаЛњЫсЃЌетЪБбРГнОЭЛсЪмЕНИЏЪДЃЌЦфдвђЪЧ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com