
题目列表(包括答案和解析)
14.一定条件下,合成氨气反应达到平衡时,测得混合气体中氨气的体积分数为20.0% ,反应后混合气体总体积与反应前的总体积之比是( )
A.1∶6 B.6∶1 C.5∶6 D.6∶5
13.在一定温度下,恒容密闭容器中,充入一定量的NO和O2,发生2NO+ O2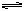 2NO2,
2NO2,
反应达到平衡的标志是( )
①. NO、O2、NO2分子数目比是2:1:2 ②反应混合物中各组分物质的浓度相等
③. 混合气体的颜色不再变 ④. 混合气体的密度不再改变
⑤混合气体的平均相对分子质量不再变化 ⑥ 2 V [O2(正)]= V [NO2(逆)]
A .② B. ①② C .②③④ D. ③ ⑤⑥
12.在2 L密闭容器中充有2 mol SO2和一定量的O2,发生下列反应:2SO2 (g)+ O2 (g) 
 2SO3(g)。当反应进行到4 min时,测得此时SO2为0.4 mol,那么反应进行到2 min时,密闭容器中SO2的物质的量是( )
2SO3(g)。当反应进行到4 min时,测得此时SO2为0.4 mol,那么反应进行到2 min时,密闭容器中SO2的物质的量是( )
A.1.6 mol B.1.2mol C.大于1.6mol D.小于1.2mol
11.下列措施对增大反应速率明显有效的是( )
A.Al在氧气中燃烧生成A1203,将Al片改成Al粉
B.Fe与稀硫酸反应制取H2时,改用浓硫酸
C.在K2S04与BaCl2两溶液反应时,增大压强
D.Na与水反应时增大水的用量
10.在一定条件下,反应mA(g)+nB(g)  pC(g)+qD(g)在一个密闭容器中进行,测得平均反应速率v(C)=2v(B)。若反应达到平衡后,保持温度不变,加大体系压强平衡不移动,则m、n、p、q的数值可以是( )
pC(g)+qD(g)在一个密闭容器中进行,测得平均反应速率v(C)=2v(B)。若反应达到平衡后,保持温度不变,加大体系压强平衡不移动,则m、n、p、q的数值可以是( )
A.2、6、3、5 B.3、1、2、2 C.3、1、2、1 D.1、3、2、2
9.在密闭容器中,反应:CH4(g)+H2O(g)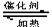 CO(g)+3H2(g)
△H>0 达到平衡。下列叙述不正确的是( )
CO(g)+3H2(g)
△H>0 达到平衡。下列叙述不正确的是( )
A.增加甲烷的量,上式中△H增大 B.增大水蒸气的量,可提高甲烷的转化率
C.升高温度,逆反应速率增大 D.增大体系压强,该反应的化学平衡常数不变
8.
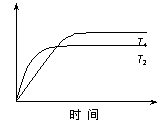 在密闭的容器中进行如下的反应:H2(g)+I2(g)
在密闭的容器中进行如下的反应:H2(g)+I2(g) 2HI(g),在温度T1和T2时,产物的量与时间的关系如下图所示,符合图象的正确的判断是( )
2HI(g),在温度T1和T2时,产物的量与时间的关系如下图所示,符合图象的正确的判断是( )
A.T1>T2,△H>0 B.T1>T2,△H<0
C.T1<T2,△H>0 D.T1<T2,△H<0
7.下列有关工业生产的叙述正确的是( )
A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.合成氨工业中,使用铁催化剂可加快正反应速率,提高N2、\H2的转化率
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室
D.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
6.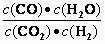 高温下,某反应达平衡,平衡常数K =
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
高温下,某反应达平衡,平衡常数K =
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
A.该反应的焓变为正值 B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小 D.该反应化学方程式为CO+H2O  CO2+H2
CO2+H2
5.将两个铂电极插人KOH溶液中,向两极分别通人CH4和O2,构成甲烷燃料电池。已知:。通人CH4的一极,其电极反应式是:CH4 + 10OH- - 8e-=CO32-+7 H2O;通入O2的另一极,其电极反应式是:2O2 + 4H2O + 8e- = 8OH-。下列叙述不正确的是( )。
A.通人CH4的电极为负极
B.正极发生氧化反应
C.燃料电池工作时,溶液中的OH-向负极移动
D.该电池使用一段时间后应补充KOH
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com