
题目列表(包括答案和解析)
6、一个真空恒容密闭容器中盛有1molPCl5,加热到200℃时发生了反应:PCl5(g) PCl3(g)+Cl2(g),反应达到平衡时PCl5的分解率为M %,若在同一温度和同样容器中最初投入的是2molPCl5,反应达到平衡时PCl5的分解率为N %。M与N的关系是 ( )
PCl3(g)+Cl2(g),反应达到平衡时PCl5的分解率为M %,若在同一温度和同样容器中最初投入的是2molPCl5,反应达到平衡时PCl5的分解率为N %。M与N的关系是 ( )
A.M>N B.M<N C.M=N D.无法比较
5、下列说法正确的是 ( )
A.HCl溶液中无OH-
B.酸的溶液显酸性,碱的溶液显碱性,盐的溶液显中性。
C.PH=2的醋酸溶液加水稀释后c(H+)和c(OH-)都减小
D.常温下,PH=6的水溶液一定显酸性。
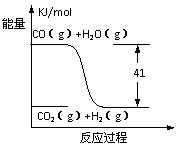
4、根据下列图式,下列热化学方程式书写正确的是( )
A.CO + H2O = CO2 + H2 ΔH = -41 KJ/mol
B.CO(g)+H2O(g)= CO2(g)+H2(g) ΔH =+ 41 KJ/mol
C.CO2(g)+H2(g)= CO(g)+H2O(g) ΔH = + 41 KJ/mol
D.CO2(g)+H2(g) = CO(g)+H2O(g) ΔH = -41 KJ/mol
3、在密闭容器中有可逆反应nA (g)+mB(g)  pC(g) △H>0 处于平衡状态(知n+m>p)下列说法正确的是( )
pC(g) △H>0 处于平衡状态(知n+m>p)下列说法正确的是( )
①升高温度时,c(B)/c(C)的比值减小 ②降温时,体系内混合气体平均式量减小
③加入B,A的转化率变大 ④加入催化剂,气体的总物质的量不变
⑤充入C,则A,B的物质的量增大
 A
③④ B ①②⑤ C ②③⑤ D 全部
A
③④ B ①②⑤ C ②③⑤ D 全部
2、用pH试纸测定溶液pH的正确操作是 ( )
A.将一小块试纸用蒸馏水润湿后放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照
B.将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照
C.将一小条试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照
D.将一小条试纸先用蒸馏水润湿后,在待测液中蘸一下,取出后与标准比色卡对照
1、下列说法中正确的是( )
A.在化学反应过程中,发生物质变化的同时不一定发生能量变化
B.生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,
反应为吸热反应
C.为了提高煤的利用率,常将煤气化或直接液化后燃烧。煤气化或直接液化属于物理变化
D.反应产物的总焓大于反应物的总焓时,反应吸热,ΔH>0
27、将6mol A气体和5mol B气体混合放入4L密闭容器中,发生下列反应:
 3A (g) + B (g)
2C (g) + xD (g) ,经过5min达到化学平衡,此时生成C为2mol,
3A (g) + B (g)
2C (g) + xD (g) ,经过5min达到化学平衡,此时生成C为2mol,

26.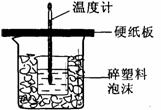 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是________,烧杯间填满碎塑料泡沫的作用是________________。
(2) 大烧杯上如不盖硬纸板,则求得的中和热数值_______(填“偏大”、“偏小’、“无影响”)
(3) 实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L 的NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),理由是___________________;所求中和热的数值会________(填“相等”或“不相等”),理由是__________________。
的NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),理由是___________________;所求中和热的数值会________(填“相等”或“不相等”),理由是__________________。
25.将镁带投入盛有盐酸的敞口容器里,产生H2的速率与时间的
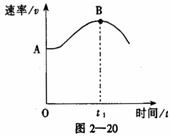 关系可由图2-20表示。 在下列因素中①盐酸的浓度
关系可由图2-20表示。 在下列因素中①盐酸的浓度
②镁带的表面积 ③溶液的温度 ④Cl-的浓度
(1)能影响此反应速率的因素有__________(选择);
(2)解释图中AB段形成的原因是 ;
(3)解释图中t1时刻后速率变小的原因是 。
24.在一小烧杯里混合10ml 0.01mol/L FeC13溶液和10ml 0.01mol/L KSCN溶液,溶液立即变为红色。
(1)再向溶液中滴入1mol/LFeC13溶液,现象 ,平衡向 反应方向移动,KSCN浓度会 。
(2)在烧杯中加入KC1固体,颜色 ,平衡 移动。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com