
题目列表(包括答案和解析)
11、 等物质的量的SO2和O2混合, 在一定条件下发生反应, 达到平衡状态时, SO2的转化率为a%, O2的转化率为b%, 则二者的关系为( )
A. a% > b% B. a% < b% C. a% = b% D. 不能确定
10、在恒温下的密闭容器中, 有可逆反应: 2NO + O2  2NO2 (正反应为放热反应), 不能说明已经达到平衡状态的是( )
2NO2 (正反应为放热反应), 不能说明已经达到平衡状态的是( )
A. 正反应生成 NO2 的速率和逆反应生成 O2 的速率相等
B. 反应容器中压强不随时间的变化而变化
C. 混合气体颜色深浅保持不变
D. 混合气体的平均分子量不随时间变化而变化
9、在室温下,pH=13的强碱与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱与强酸
的体积比为 ( )
A.9:1 B.1:11 C.1:9 D.11:1
8、盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是( )
A. 在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO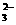 和OH-
和OH-
B. NaHCO3溶液中:c (H+)+ c (H2CO3)=c( OH- )
C. 10 mL0.10mol·L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c( CH3COO- )>c(OH-)>c(H+)
D. 中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同
7、甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
 ①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H= + 49.0 kJ·mol-1
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H= + 49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9 kJ·mol-1
下列说法正确的是( )
A.CH3OH的燃烧热为192.9 kJ·mol-1
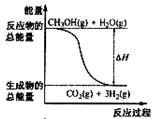
B.反应①中的能量变化如右图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ·mol-1
6、恒温恒压,不做功时,反应A+B==C+D,在下列哪种情况下,一定能自发进行( )
A.△H<0 △S>0 B.△H>0 △S>0 C.△H<0 △S<0 D.△H>0 △S<0
5、


 H2(g)+I2(g)
H2(g)+I2(g)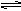 2HI(g) (正反应为放热反应),可逆反应已达化学平衡,下列图象中正确的是( )
C(I2)
C(I2) H2%
H2转化率
2HI(g) (正反应为放热反应),可逆反应已达化学平衡,下列图象中正确的是( )
C(I2)
C(I2) H2%
H2转化率
P P T T
A B C D
4、向0.lmol/L 氨水中逐渐加入一定量的水,始终保持增大趋势的是( ) A. NH3·H2O B.OH-浓度 C. H+的浓度 D.NH4+的浓度
3、下列说法中正确的是( )
A.0.1mol/LHCl和0.1mol/LH2SO4与相同形状和大小的大理石反应速率相同
B.大理石块与大理石粉分别同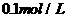 盐酸反应速率相同
盐酸反应速率相同
C.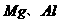 在相同条件下分别与
在相同条件下分别与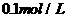 盐酸反应,其反应速率相同
盐酸反应,其反应速率相同
D.0.1mol/LHCl和0.1mol/LHNO3与相同形状和大小的大理石反应,速率相同
2、水的电离过程为H2O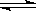 H++OH-,在不同温度下其离子积为Kw(25℃)=1.0×10-14,Kw(100℃)=1×10-12。则下列叙述正确的是( )
H++OH-,在不同温度下其离子积为Kw(25℃)=1.0×10-14,Kw(100℃)=1×10-12。则下列叙述正确的是( )
A.c(H+)随温度的升高而降低 B.100℃时,c(H+)>c(OH-) C.100℃时,水的pH=6 D.水的电离是放热过程
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com