
题目列表(包括答案和解析)
8. 对于任何一个化学平衡体系,采用以下措施,一定会使平衡移动的是( )
A. 加入一种反应物 B. 升高温度
C. 对平衡体系增加压强 D. 使用催化剂
7. 已知2mol H2 燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
A. H2O(l) ==H2(g)+ 1/2 O2(g); △H = +242 kJ·mol-1
B. 2H2(g)+O2(g)==2H2O(l); △H = - 484 kJ·mol-1
C. H2(g)+ 1/2 O2(g) ==H2O(g); △H = +242 kJ·mol-1
D. 2H2(g)+O2(g)==2H2O(g); △H =- - 484 kJ·mol-1
6. 某无色溶液与NH4HCO3作用能产生气体,此溶液中一定能大量共存的离子组是( )
A. Cl- 、、 Mg2+、 H+ 、Ba2+ 、 SO42-
B. Na+ 、 Ba2+、 NO3- 、 OH-、 Al3+
C . MnO4- 、 K+ 、 Cl- 、 H+ 、 SO42-
D. K+ 、 NO3- 、 SO42- 、 Cl- 、Na+
5. 已知可充电电池在充电时作电解池,放电时作原电池。镍氢可充电电池上有两极(如图所示),一极旁标有“+”,另一极旁标有“-”。下列关于标有“-”的一极的说法中正确的是( )

|

 B. 充电时作阳极,发生氧化反应
B. 充电时作阳极,发生氧化反应


|
 C. 充电时作阴极,发生还原反应
C. 充电时作阴极,发生还原反应
D. 充电时作阴极,放电时作正极
4. 常温时,将V1ml c1mol/L的氨水滴加到V2ml c2mol/L的盐酸中,下列结论中正确的是( )
A. 若混合溶液的PH=7。则c1V1= c2V2
B. 若 V1=V2, c1=c2 , 则混合溶液中c(NH4+) = c(Cl-)。
C. 若混合溶液的PH=7,则混合溶液中c(NH4+) = c(Cl-)。
D. 若V1=V2, 且混合溶液的PH<7,则一定是c1<c2
3. 向三份0.1mol/LCH3COONa溶液中分别加入少量的 NH4NO3、 Na2CO3、 FeCl3固体
(忽略溶液体积变化),则CH3COO-浓度的变化依次为 ( )
A. 减小、增大、减小 B. 增大、减小、减小
C . 减小、增大、增大、 D . 增大、减小、增大、
2. 下列实验方案合理的是 ( )
A. 在镀件上电镀铜时,可用金属铜做阳极,用盐酸做电解质溶液
B. 往碘化银沉淀中滴加氯化钠溶液,使碘化银沉淀转化为氯化银
C. 制备FeCl3 溶液时,先将固体溶于较浓的盐酸,再加水稀释
D. 用湿润的PH试纸测量某酸溶液的PH,测出溶液的酸碱性
1.柠檬水中的c (OH-) =10-11 mol/L,则其PH是 ( )
A. 11 B. 7 C. 5 D. 3
31、常温常压下,断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为KJ/mol)。下表是一些键能数据:
|
化学键 |
C-H |
C-F |
H-F |
F-F |
H-H |
H-N |
|
键 能 |
414 |
489 |
565 |
158 |
436 |
391 |
(1)根据键能数据计算以下反应的反应热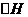 :
:
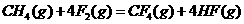 ;
;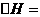 。
。
(2)根据键能和反应热化学方程式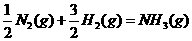 ;
;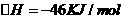 ,则N=N的键能为
。
,则N=N的键能为
。
30、由金红石(TiO2)制取单质Ti,涉及的步骤为: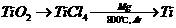
已知:①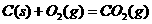 ;
;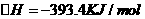
②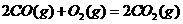 ;
;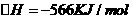
③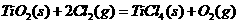 ;
;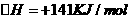
则: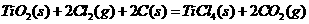 ;
;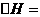 。
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com