
题目列表(包括答案和解析)
8.2007 年诺贝尔化学奖得主--德国科学家格哈德·埃特尔对一氧化碳在铂表面氧化过程的研究,催生了汽车尾气净化装置。净化装置中催化转化器可将CO.NO.NO2等转化为无害物质。下列有关说法不正确的是
A.催化转化器中的铂催化剂可加快CO的氧化
B.铂表面做成蜂窝状更有利于提高催化效果
C.在铂催化下,NO.NO2可被CO还原成N2
D.使用铂催化剂,可以提高CO.NO.NO2的转化率
7.金属镍有广泛的用途。粗镍中含有少量Fe.Zn.Cu.Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)
A.阳极发生还原反应,其电极反应式:Ni2+ + 2e- == Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+ 和Zn2+
D.电解后,电解槽底部的阳极泥中金属只有Cu和Pt
6.下列说法正确的是
A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
D.催化剂不影响反应活化能,但能增大单位体积内活化分子百分数,从而增大反应速率
5.强酸与强碱在稀溶液发生中和反应的热化学方程式为H+(aq)+OH-(aq)=H2O(l);
△H=-57.3 KJ/mol,向3份同体积0.2 mol/L的NaOH溶液中分别加入适量的稀醋酸.浓硫酸.稀硝酸,恰好完全反应的热效应△H1.△H2.△H3.的关系正确的是
A. △H1>△H2>△H3 B.△H1>△H3>△H2
C. △H2>△H1>△H3 D.△H2>△H3>△H1
4.下列说法中正确的是
A.凡是放热反应都是自发的,吸热反应都是非自发的
B.自发反应一定是熵增大,非自发反应一定是熵减小或不变
C.熵增加且放热的反应不一定是自发反应
D.非自发反应在一定条件下可能实现自发进行
3.下列对弱电解质判断的方法正确的是:
A.电解质在熔融状态下不能完全电离 B.电解质在水中的导电能力较弱
C.电解质在水溶液中不能完全电离 D.它不一定是共价化合物
2.已知0.1mol/L的醋酸溶液中存在电离平衡: CH3COOH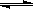 CH3COO-+H+ 要使溶液中c(H+)/c(CH3COOH)比值增大,可以采取的措施是
CH3COO-+H+ 要使溶液中c(H+)/c(CH3COOH)比值增大,可以采取的措施是
A.加少量CH3COONH4固体 B.降低温度
C.加少量NaCl固体 D.升高温度
1.下列属于强电解质的是
①NaOH ②NH3·H2O ③CaCO3 ④CH3COOH ⑤CH3COONH4
A.①②③ B.②③④ C.①③⑤ D.①④⑤
38. 维生素C(分子式为C6H8O6)能防治坏血病,又称为抗坏血酸。右表是某品牌柠檬汁饮料标签的部分内容。
(1)该饮料中维生素C的物质的量浓度为多少mol·L-1?
(2)维生素C有较强的还原性,能与I2发生氧化还原反应,其反应方式为: C6H8O6 + I2 → C6H6O6 + 2HI。
某课外学习小组利用该反应测定某维生素C药片中维生素C的含量。取1片质量为0.1g的维生素C药片碾碎后配成溶液并与碘溶液反应(假定该药片中的其它成分不与碘反应)。反应完全后,共消耗0.02mol·L-1的碘溶液25mL,则该药片中维生素的质量分数为多少?
苍南中学高二第一学期期中考化学(文科)
37. 煤是一种常用的燃料,由于煤燃烧产生的废气含有SO2、NO2和NO等多种有害气体和烟尘会对环境造成污染,因此需要对煤进行加工后再燃烧,或将废气净化后再排放
(1)将煤直接进行燃烧,造成环境污染的主要方面之一是形成硝酸型酸雨
①写出有关物质转化为硝酸的化学方程式
, 。
②以下是对硝酸型酸雨的若干项评价,其中正确的是 (多选)
A.杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
B.对电线、铁轨、桥梁、房屋等均会造成严重损害
C.导致臭氧层空洞
D.硝酸与土壤中的矿物质发生作用转化为硝酸盐,向植物提供氮肥
(2)对煤用石灰石进行脱硫处理,脱硫后,在废气中含有的不良气体是 ,它对环境的负面影响是 。
(3)检验脱硫后废气中是否含有SO2的简单方法是 。
|
Nutrition Facts 营养成分 500mL含量 |
|
|
热量 710kJ |
碳水化合物 42g |
|
蛋白质 0g |
脂肪酸 0g |
|
维生素C 100mg |
|
|
中国居民膳食营养素日推荐摄入量(RNI): 维生素C 100mg |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com