
题目列表(包括答案和解析)
16.下列有关水的电离的说法正确的是
A.将水加热,KW增大,pH不变
B.向水中加入少量NaHSO4固体,恢复到原温度,水的电离程度增大
C.向水中加入少量NH4Cl固体,恢复到原温度,水的电离程度减小
D.向水中加入少量NaOH固体,恢复到原温度,水的电离被抑制,c(OH-)增大
15. 1L0.1mol/LAgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极增重2.16g时。下列判断(设电解按理论进行,溶液不蒸发) 正确的是:
A. 溶液的浓度变为0.08mol/L
B. 阳极上产生112mLO2(标准状况)
C. 转移的电子数是1.204×1022个
D. 反应中有0.01mol的Ag被氧化
14. 将标况下的2.24LCO2通入150mL 1mol•L-1NaOH溶液中,下列说法正确的是( )
A. c(HCO3-) 略大于c(CO32-) B. c(HCO3-) 等于c(CO32-)
C. c(Na+)等于c(CO32-)与c(HCO3-)之和 D. c(HCO3-) 略小于c(CO32-)
13.温度相同、浓度均为0.2 mol L-1的①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4NO3、
⑤CH3COONa溶液,它们的pH值由小到大的排列顺序是 ( )
A.③①④②⑤ B.①③④②⑤ C.③②①④⑤ D.⑤②④①③
12. 以铁为阳极、铜为阴极,对足量的NaOH溶液进行电解,一段时间后得到2mol
 Fe(OH)3沉淀,此时消耗水的物质的量共为
Fe(OH)3沉淀,此时消耗水的物质的量共为
A. 2mol B. 3mol C. 4mol D. 5mol
11. 现有常温时pH=1的某强酸溶液10mL,下列操作能使溶液的pH变成2的是( )
A.加入10mL 0.01mol·L-1的NaOH溶液 B.加入10mL 的水进行稀释
C.加水稀释成100mL D.加入10mL 0.01mol·L-1的盐酸溶液
10. 下列叙述正确的是( )
A. 将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+)
B. 两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C. pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D. 向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中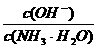 增大
增大
9. 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
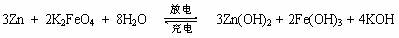
下列叙述不正确的是
A. 放电时负极反应为:Zn - 2e- + 2OH- == Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3 - 3e- + 5OH- == FeO42- + 4H2O
C. 放电时每转移3moL电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
8. 下列操作中,能使电离平衡H2O H++OH-,向右移动且溶液呈酸性的是( )
H++OH-,向右移动且溶液呈酸性的是( )
A.向水中加入NaHSO4溶液 B.向水中加入Al2(SO4)3固体
C.向水中加入Na2CO3溶液 D.将水加热到100℃,使pH=6
7. 在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有( )
A. 滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、I-
B. pH值为1的溶液:Cu2+、Na+、Mg2+、NO3-
C. 水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+
D. 所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com